广东省广州市2025年中考化学试题
试卷更新日期:2025-08-12 类型:中考真卷
一、选择题:本题包括14小题,每小题3分,共42分。每小题给出的四个选项中,只有一项最符合题意。错选、不选、多选或涂改不清的,均不给分。
-
1. 中华文明源远流长,汉字居功至伟。下列汉字载体属于有机合成材料的是( )




A.兽骨 B.蚕丝 C.宣纸 D.塑料 A、A B、B C、C D、D2. “水的沸腾”实验过程中,属于化学变化的是( )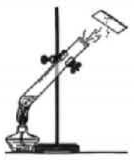 A、酒精汽化 B、酒精燃烧 C、液态水沸腾 D、水蒸气液化3. 健康生活需要平衡膳食。下列食物中富含蛋白质的是( )A、马铃薯 B、鸡蛋 C、荔枝 D、芹菜4. 开发和利用新能源已成为人类的迫切需求。下列属于新能源的是( )A、煤 B、石油 C、天然气 D、风能5. 化学试剂应规范存放,存放浓硫酸的试剂柜须张贴的标志是( )A、
A、酒精汽化 B、酒精燃烧 C、液态水沸腾 D、水蒸气液化3. 健康生活需要平衡膳食。下列食物中富含蛋白质的是( )A、马铃薯 B、鸡蛋 C、荔枝 D、芹菜4. 开发和利用新能源已成为人类的迫切需求。下列属于新能源的是( )A、煤 B、石油 C、天然气 D、风能5. 化学试剂应规范存放,存放浓硫酸的试剂柜须张贴的标志是( )A、 B、
B、 C、
C、 D、
D、 6. 地球上可利用的淡水资源是有限的,下列措施不利于水资源保护的是( )A、生活污水直接排放到河流中 B、城市绿化采用节水灌溉方式 C、农业生产中合理使用化肥 D、工业废水净化后重复利用7. 劳动创造美好生活。下列劳动项目涉及的化学知识正确的是( )
6. 地球上可利用的淡水资源是有限的,下列措施不利于水资源保护的是( )A、生活污水直接排放到河流中 B、城市绿化采用节水灌溉方式 C、农业生产中合理使用化肥 D、工业废水净化后重复利用7. 劳动创造美好生活。下列劳动项目涉及的化学知识正确的是( )选项
劳动项目
化学知识
A
使用洁厕灵清洗马桶
洁厕灵显酸性是因为含有OH
B
在树木上涂刷石灰浆
石灰浆中含有未溶解的 Ca(OH)2
C
用活性炭制作净水器
活性炭有很强的消毒杀菌作用
D
炖汤炒菜时加盐调味
NaCl在水溶液中以分子形式存在
A、A B、B C、C D、D8. 下列宏观事实的微观解释,不正确的是( )A、金块制成金箔面积增大:金原子数目增多 B、干冰升华:二氧化碳分子间的间隔增大 C、泡茶时香气四溢:分子在不断运动 D、品红在热水中扩散更快:受热时分子运动加快9. “绿色化学”提倡从源头避免有害物质的使用与排放,在科学研究和工业生产中选择环境友好的化学反应过程。下列措施中,不符合“绿色化学”理念的是( )
A、产生有害废弃物后再进行治理 B、选择无毒无害的物质作为反应物 C、选择水作为反应物的溶剂 D、使用无毒无害的催化剂10. 下列各物质的性质和用途没有直接联系的是( )选项
性质
用途
A
不锈钢抗腐蚀性好
制造医疗器械
B
水在通电条件下有氢气生成
用于生产氢气
C
氮气化学性质不活泼
用于生产氮肥
D
金刚石导热性好
用于集成电路基板散热
A、A B、B C、C D、D11. 农业生产中,用质量分数为16%的氯化钠溶液选种。关于该溶液的说法正确的是( )A、溶液中溶质与溶剂质量之比为16:100 B、从100g该溶液中取出50g,剩余溶液溶质质量分数为8% C、任取10g该溶液都含有 1.6g氯化钠 D、将16gNaCl 固体完全溶解在100g水中,可配成该溶液12. 除去粗盐中难溶性杂质的实验流程如下,其中不涉及的操作是( )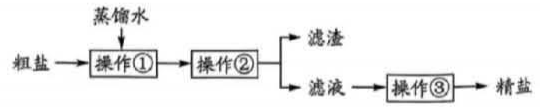 A、溶解 B、蒸馏 C、蒸发 D、过滤13. 下列实验方案中,能达到目的的是( )A、除去 Na2CO3溶液中的 NaCl:加入适量的盐酸 B、除去 CuSO4溶液中的H2SO4:加入铜粉后过滤 C、鉴别棉纤维和羊毛纤维:取少量样品,点燃闻气味 D、鉴别稀盐酸和稀硫酸:取少量样品,加入镁条观察现象14. 关于下列实验的说法,正确的是( )
A、溶解 B、蒸馏 C、蒸发 D、过滤13. 下列实验方案中,能达到目的的是( )A、除去 Na2CO3溶液中的 NaCl:加入适量的盐酸 B、除去 CuSO4溶液中的H2SO4:加入铜粉后过滤 C、鉴别棉纤维和羊毛纤维:取少量样品,点燃闻气味 D、鉴别稀盐酸和稀硫酸:取少量样品,加入镁条观察现象14. 关于下列实验的说法,正确的是( )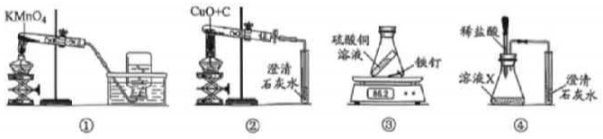 A、实验①:用排水法收集氧气,说明氧气的密度比空气大 B、实验②:试管中黑色固体变成红色,说明反应生成了二氧化碳 C、实验③:反应前后天平读数不变,说明消耗的铁和生成的铜质量相等 D、实验④:澄清石灰水变浑浊,说明溶液X中可能含有HCO3
A、实验①:用排水法收集氧气,说明氧气的密度比空气大 B、实验②:试管中黑色固体变成红色,说明反应生成了二氧化碳 C、实验③:反应前后天平读数不变,说明消耗的铁和生成的铜质量相等 D、实验④:澄清石灰水变浑浊,说明溶液X中可能含有HCO3二、非选择题:本题包括6小题,共48分。
-
15. 徐光宪院士是国际著名的中国化学家,为我国从稀土资源大国向生产强国转变作出了杰出贡献。稀土元素有“工业维生素”之称,是指钪、钇等17种储量较少的金属元素。元素周期表中元素的相关信息如图所示。
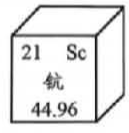 (1)、钪的相对原子质量为。(2)、华南地区稀土矿中含有较多的Sc2O3 , 其中Sc元素的化合价为。(3)、Sc(NO3)2是一种制备石油化工催化剂的原料,根据化合物的分类,Sc(NO3)2属于 。(4)、一些冶金厂的粉尘中含有ScCl3 , 经回收分离后,与金属钙在700~800℃下发生置换反应得到金属,化学方程式为。钪和钙都是活泼金属,进行该置换反应时应注意。16. 阅读下列短文并回答问题。
(1)、钪的相对原子质量为。(2)、华南地区稀土矿中含有较多的Sc2O3 , 其中Sc元素的化合价为。(3)、Sc(NO3)2是一种制备石油化工催化剂的原料,根据化合物的分类,Sc(NO3)2属于 。(4)、一些冶金厂的粉尘中含有ScCl3 , 经回收分离后,与金属钙在700~800℃下发生置换反应得到金属,化学方程式为。钪和钙都是活泼金属,进行该置换反应时应注意。16. 阅读下列短文并回答问题。建设美丽广州,打造美丽中国城市样板。近年来,广州市环境空气质量持续改善。
广州市环境空气主要污染物浓度
污染物种类
PM2.5
(μg/m3)
PM10
(μg/m3)
二氧化氮
(μg/m3)
二氧化硫
(μg/m3)
臭氧
(μg/m3)
一氧化碳
(mg/m3)
2024年
21
37
27
6
146
0.9
2023年
23
41
29
6
159
0.9
浓度限值
二级
35
70
40
60
160
4.0
浓度限值
一级
15
40
40
20
100
4.0
注:PM2.5指粒径小于等于2.5μm的颗粒物、PM10指粒径小于等于10μm的颗粒物。
--摘录自2023年、2024年《广州市生态环境状况公报》
臭氧(O3)气味强烈,即使浓度很低,也会损伤人的肺功能,引起打喷嚏、咳嗽、胸痛和肺水肿等,它还会影响植物的生长。地表附近臭氧的生成,与二氧化氮、PM2.5等多种污染物有关,在阳光作用下,一种生成臭氧的原理如下:
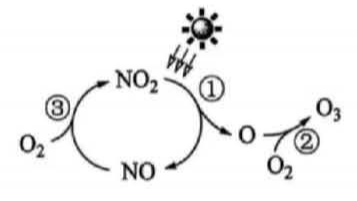
臭氧不仅存在于地表附近,还存在于距离地球表面20~35km的平流层,它能吸收太阳光中绝大部分的紫外线,使地球上的生物免受紫外线的伤害。
(1)、2024年广州市环境空气主要污染物中,浓度高于一级限值的有。(2)、空气中二氧化硫的浓度为6μg/m3 , 则1m3空气中至少含硫元素μg。(3)、结合上述生成臭氧的原理图:①图中属于化合物的分子有种。
②随着O3分子的数目不断增加,分子的数目不断减少。
(4)、臭氧既保护了人类,也可能给人类带来伤害。请举出一种类似的化学物质,谈谈你对它的认识。17. 青铜铸文明,文脉传千秋。四千多年前,华夏民族就能够冶炼青铜合金。(1)、《周礼·考工记》中记载了春秋时期的六种青铜合金,其中两种的性质如下表:名称
钟鼎之齐(含锡16.7%)
戈戟之齐(含锡25.0%)
熔点/℃
980
800
布氏硬度(数值越大越硬)
90
290
它们在古代分别用于制作礼器和兵器。用“戈戟之齐”制作兵器,利用的物理性质是。【答案】
(2)、赤铜矿中 Cu2O的质量分数为72%,炼铜时发生反应Cu2O+CO=2Cu+CO2 , 理论上1吨赤铜矿能冶炼出吨铜。(3)、一些古老的铜器“纯青如铺翠、而莹如玉”。在自然环境中,铜器受腐蚀生成“无害锈”,不仅增加美观度还有一定的保护作用。在氯离子、氧气和潮湿环境的影响下,“无害锈”也会转化为质地疏松易脱落的“有害锈”,加快铜器腐蚀。
锈蚀类型
主要成分
无害锈
Cu(OH)2CO3、CuO、Cu2O
有害锈
Cu(OH)2Cl
①根据组成预测, Cu2(OH)2CO3和Cu2(OH)3Cl都能溶于盐酸, 生成(填化学式) 溶
液。
②某小组刮取少量铜器表面锈蚀物于试管中,加入足量稀盐酸,锈蚀物溶解得到蓝色溶液,并有气泡冒出,再向试管中滴加几滴硝酸银溶液,出现白色浑浊。
反思与评价:锈蚀物中含“无害锈”,依据是;不能确定是否含“有害锈”,理由是。(查阅资料:Ag2CO3、AgCl均为白色固体且不溶于水)
③考古学家从海底打捞出青铜文物后,立即用蒸馏水清洗,主要目的是。
埋藏在海底的青铜文物历经多年仍保存相对完好,原因是。
18. 化学在“低碳行动”中发挥着重要作用。一种用K2CO3溶液对燃煤电厂排放的二氧化碳进行捕集和利用的方案如下: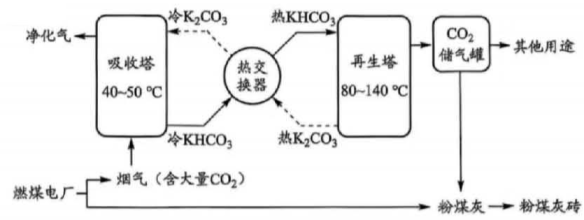
注:“再生”是指KHCO3释放CO2后又变回K2CO3的过程。(1)、燃煤发电是将化学能最终转化为。(2)、吸收塔中K2CO3溶液发生反应的化学方程式是。(3)、上述方案的相关举措中,体现低碳、循环发展理念的有____。A、使用高硫煤发电 B、设置热交换器 C、K2CO3循环再生 D、用粉煤灰制砖(4)、甲酸是一种重要的化工原料,分子微观示意图如下。请你设计一个由二氧化碳合成甲酸的化合反应,写出化学方程式。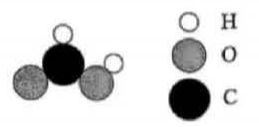 (5)、某粉煤灰的主要成分如下表:
(5)、某粉煤灰的主要成分如下表:粉煤灰组成
MgO
CaO
Al2O3
SiO2
含量(质量分数)
2.0%
5.6%
20.4%
72.0%
往粉煤灰中加水制得湿料,再与CO2反应,制成粉煤灰砖以实现CO2的封存。该粉煤灰砖可看作是碳酸镁、碳酸钙、氧化铝、二氧化硅的混合物,其组成可表示为MgCO3·2CaCO3·4Al2O3·24SiO2。理论上100 吨粉煤灰可以封存吨CO2。
(相对分子质量: MgO40 CaO56 Al2O3 102 SiO260)
19. 碳酸钡 (BaCO3) 广泛用于制造光学玻璃、陶瓷、塘瓷、颜料等,工业上用重晶石 (BaSO4)碳化法生产碳酸钡的流程如下: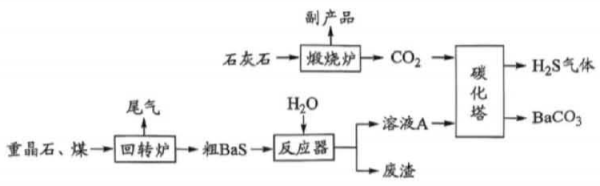 (1)、煅烧炉得到的副产品是(写化学式)。(2)、粗BaS中的杂质不参与反应,反应器中生成的 Ba(OH)2和 Ba(HS)2均进入溶液A在碳化塔中与CO2反应完全转化为BaCO3沉淀。
(1)、煅烧炉得到的副产品是(写化学式)。(2)、粗BaS中的杂质不参与反应,反应器中生成的 Ba(OH)2和 Ba(HS)2均进入溶液A在碳化塔中与CO2反应完全转化为BaCO3沉淀。①BaS与H2O反应的化学方程式是。
②如果参加反应的BaS质量是338kg,理论上碳化塔中参加反应的CO2质量是kg。
(3)、结合上述工艺,设计吸收碳化塔产生的酸性气体H2S的合理方案:(4)、 BaCO3可用于制备其他钡的化合物。已知BaCl2、 Ba(OH)2的溶解度如下表:温度/℃
0
20
40
60
80
溶解度/g
BaCl2
31.6
35.7
40.7
46.4
52.4
溶解度/g
Ba(OH)2
1.7
3.9
8.2
20.9
101.4
①描述两种物质的溶解度特点:
BaCl2:0~80℃范围内溶解度均较大,随温度升高而增大。
Ba(OH)2:。
②以BaCO3为原料制备 Ba(OH)2固体,简述操作过程:在加热条件下,将BaCO3固体溶于浓盐酸,。
20. 化学反应需要一定的条件,调控化学反应具有重要意义。(1)、将食品置于冰箱中保存可减缓变质,原理是能影响化学反应。(2)、某小组按下列实验方案探究过氧化氢分解的影响因素,实验用到的H2O2溶液浓度为30%,催化剂的用量均相同,0~100秒广口瓶中压强的变化用△p表示。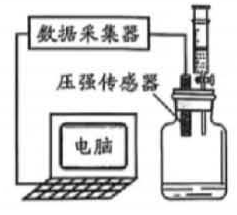
编号
H2O2溶液的体积/mL
水的体积/mL
溶液pH
催化剂种类
△p /kPa
1
15
15
5
FeCl3
49
2
10
20
5
FeCl3
26
3
5
25
5
FeCl3
20
4
5
25
5
CuCl2
10
5
5
25
5
CuSO4
7
①实验1、2、3用于探究对过氧化氢分解快慢的影响。
②依据实验(填编号) 的数据, 得出催化能力: FeCl3>CuCl2。
③在上述实验的基础上,提出一个可继续探究的问题:
(3)、研究和调控燃烧能提升化学反应的应用价值。①将蜡烛置于空气中,测定从点燃到熄灭过程中气体浓度(体积分数)的变化,结果如图。
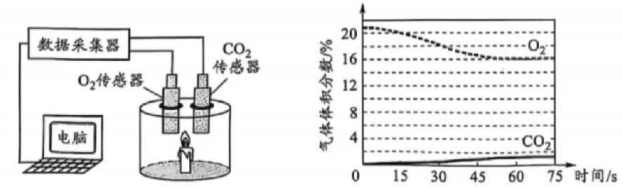
为了探究蜡烛熄灭的原因,用空气占95%、CO2占5%的混合气体重做实验,观察到蜡烛(填“能”或“不能”)点燃,说明氧气浓度降低是蜡烛熄灭的原因。
②用红磷燃烧探究空气中氧气的含量,装置如图,排除装置与操作误差后,发现实验结果总是低于氧气的真实含量,原因可能是。
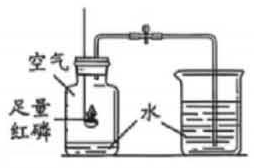
③煤矿井下的空气通常含有甲烷,不断鼓入新鲜空气是防止发生燃烧或爆炸的举措之一,其原理是通过使甲烷燃烧无法达到所需的条件。