湖北省武汉市2025年中考化学试卷
试卷更新日期:2025-07-15 类型:中考真卷
一、选择题
-
1. 汉字是中华文化的瑰宝,曾书于竹帛、镂于金石、琢于盘盂。兽骨、青铜、丝绸、竹木都曾为汉字的记录载体,其中属于合金的是( )


A.兽骨
B.青铜


C.丝绸
D.竹木
A、A B、B C、C D、D2. 以下是进行“粗盐中难溶性杂质的去除”实验的部分操作,其中错误的是( )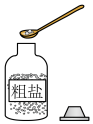
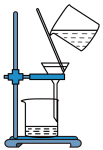
A.取粗盐
B.过滤混合物

C.取下蒸发皿
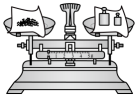
D.称量精盐
A、A B、B C、C D、D3. 劳动有利于知行合一、下列有关劳动项目的解释错误的是( )选项
劳动项目
解释
A
用铅笔绘制宣传画
利用了石墨的导热性
B
设置森林防火隔离带
隔离可燃物,预防火灾
C
洗净铁锅并用抹布擦干
铁与氧气、水等接触易生锈
D
用熟石灰处理含硫酸的污水
熟石灰与硫酸发生中和反应
A、A B、B C、C D、D4. 汽车安全气囊系统如图所示,其中气体发生器内产气药剂的信息如资料卡片所示。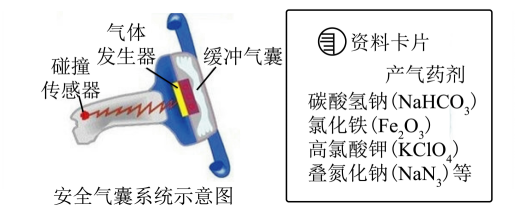
下列说法错误的是( )
A、俗称小苏打 B、属于氧化物 C、中钾离子的符号为 D、由三种元素组成5. 利用捕集的生产低碳、零碳燃料,既可缓解能源危机,又可助力实现“双碳”目标。我国科研人员研制出的新型催化剂,可催化转化为甲醇,其转化过程如图所示。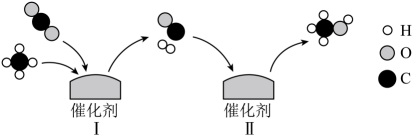
下列说法正确的是( )
A、 与
与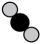 的化学性质相同
B、Ⅰ中反应前后存在元素化合价的改变
C、Ⅱ中反应前后原子和分子的数目均保持不变
D、Ⅰ和Ⅱ中反应前后催化剂的质量均发生改变
6. 某同学绘制了物质的转化关系如图所示(图中“→”表示一种物质可以转化为另一种物质,部分反应物、生成物及反应条件已略去)。下列说法错误的是( )
的化学性质相同
B、Ⅰ中反应前后存在元素化合价的改变
C、Ⅱ中反应前后原子和分子的数目均保持不变
D、Ⅰ和Ⅱ中反应前后催化剂的质量均发生改变
6. 某同学绘制了物质的转化关系如图所示(图中“→”表示一种物质可以转化为另一种物质,部分反应物、生成物及反应条件已略去)。下列说法错误的是( )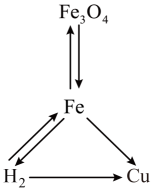 A、Fe能在空气中剧烈燃烧生成红色的 B、转化为Fe的反应可以是置换反应 C、可与CuO反应生成Cu,也可与反应生成Fe D、将Cu浸入溶液中可比较Fe和Cu的金属活动性7. 将可燃物与过量氧气在密闭容器中用电火花引燃,除生成二氧化碳外,还可能生成水。充分反应后,容器内氧气减少了。实验过程中生成二氧化碳的质量随时间的变化关系如图所示。下列说法正确的是( )
A、Fe能在空气中剧烈燃烧生成红色的 B、转化为Fe的反应可以是置换反应 C、可与CuO反应生成Cu,也可与反应生成Fe D、将Cu浸入溶液中可比较Fe和Cu的金属活动性7. 将可燃物与过量氧气在密闭容器中用电火花引燃,除生成二氧化碳外,还可能生成水。充分反应后,容器内氧气减少了。实验过程中生成二氧化碳的质量随时间的变化关系如图所示。下列说法正确的是( )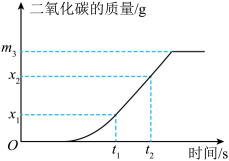 A、图中时刻,容器内氧气的质量为 B、图中时刻,容器内碳元素的质量为 C、若 , 则该可燃物一定含有碳、氧元素 D、若 , 则该可燃物一定含有碳、氢、氧元素8. 项目小组为探究金属的化学性质进行图1所示实验,充分反应后,甲试管内的溶液只含一种溶质。然后将甲、乙两支试管内的物质倒入烧杯,如图2所示。充分反应后过滤,得到滤渣和滤液。
A、图中时刻,容器内氧气的质量为 B、图中时刻,容器内碳元素的质量为 C、若 , 则该可燃物一定含有碳、氧元素 D、若 , 则该可燃物一定含有碳、氢、氧元素8. 项目小组为探究金属的化学性质进行图1所示实验,充分反应后,甲试管内的溶液只含一种溶质。然后将甲、乙两支试管内的物质倒入烧杯,如图2所示。充分反应后过滤,得到滤渣和滤液。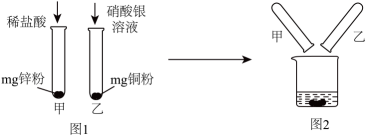
下列说法错误的是( )
A、若滤液呈无色,则滤渣中可能存在3种物质 B、若滤液呈蓝色,则滤渣中可能存在2种物质 C、若滤渣为混合物,则其质量可能小于2mg D、若滤渣为纯净物,则滤液中可能存在3种金属离子二、填空与简答
-
9. 便携式供氧器广泛用于医疗急救、航空航天、水下作业等领域。某项目小组从制氧剂选择和装置优化等方面开展简易供氧器设计和制作的跨学科实践活动。
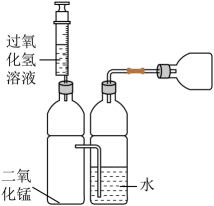
制氧剂
制氧原理
生产1kg氧气所需成本
30%过氧化氢溶液
约13元
氯酸钠
约11元
高锰酸钾
约148元
回答下列问题:
(1)、上表中生产1kg氧气所需成本最低的制氧剂是____(填标号)。A、30%过氧化氢溶液 B、氯酸钠 C、高锰酸钾(2)、某同学设计的简易供氧器如图所示,制取氧气的化学方程式为。(3)、上表中三种制氧原理均属于(填基本反应类型)。10. 是配制无土栽培营养液常用的三种物质,它们在不同温度时的溶解度如下表所示。温度/℃
0
20
40
60
80
100
溶解度/g
29.4
37.2
45.8
55.2
65.6
77.3
41.6
53.8
70.5
75.4
71.1
60.5
13.3
31.6
63.9
110
169
246
(1)、的溶解度随温度的升高而(填“增大”“减小”或“不变”)。(2)、配制营养液时,为加快在水中的溶解,可采用的一种方法是。(3)、配制某无土栽培营养液需补充钾元素195g,则需的质量为。(4)、对上表中某一种物质的溶液进行如图所示实验。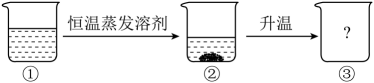
编号①、②、③的溶液中溶质质量分数的大小关系可能是____(填标号)。
A、①<②<③ B、①=②=③ C、①>②>③ D、③<①<②11. 氯化镁产品大多数是黄褐色或白色固体,习惯称为卤片。某卤片的主要成分为 , 还含少量、NaCl和 , 以该卤片为原料生产的工艺流程示意图如下所示。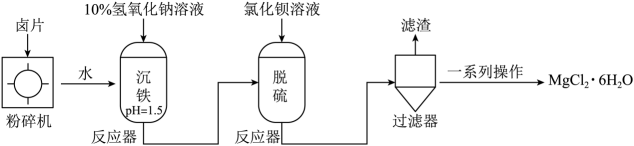
已知:①。
②时,氢氧化铁开始沉淀;时,氢氧化铁沉淀完全。
③时,氢氧化镁开始沉淀;时,氢氧化镁沉淀完全。
(1)、配制50g质量分数为10%的氢氧化钠溶液,下图中的仪器不会用到的是____(填标号)。A、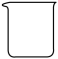 B、
B、 C、
C、 (2)、“沉铁”时,调节溶液 , 该溶液呈性。(3)、加入适量氯化钡溶液可实现“脱硫”,反应的化学方程式为。(4)、“滤渣”的成分为。(5)、为制备 , “一系列操作”中宜采用降温结晶,而不宜采用蒸发结晶,其原因是(答两点)。
(2)、“沉铁”时,调节溶液 , 该溶液呈性。(3)、加入适量氯化钡溶液可实现“脱硫”,反应的化学方程式为。(4)、“滤渣”的成分为。(5)、为制备 , “一系列操作”中宜采用降温结晶,而不宜采用蒸发结晶,其原因是(答两点)。三、科学探究题
-
12. 一氧化碳与氧化铜反应除生成二氧化碳外,还生成铜、氧化亚铜中的一种或两种。项目小组取4.00g氧化铜,对一氧化碳还原氧化铜的反应展开系列探究。
Ⅰ.利用下图所示装置制取一氧化碳并还原氧化铜
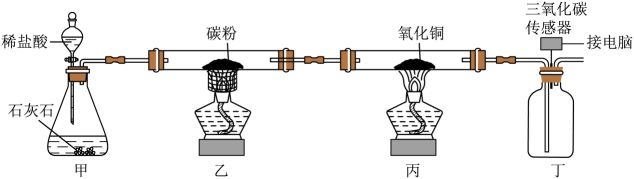 (1)、以下为与实验有关的图标,其中提示实验中会用到加热操作的是____(填标号)。A、
(1)、以下为与实验有关的图标,其中提示实验中会用到加热操作的是____(填标号)。A、 B、
B、 C、
C、 (2)、装置甲锥形瓶内反应的化学方程式为。(3)、实验中部分操作及现象如下:
(2)、装置甲锥形瓶内反应的化学方程式为。(3)、实验中部分操作及现象如下:a.加入稀盐酸,观察到二氧化碳传感器示数不断增大至稳定;
b.点燃酒精灯;加热碳粉;
c.点燃酒精灯,加热氧化铜;
d.观察到氧化铜处黑色粉末全部变红;停止加热,收集尾气。
①从安全环保的角度考虑,以上操作正确的顺序为:(填标号)。
②二氧化碳传感器示数不断增大至稳定,说明装置内已充满二氧化碳。若无二氧化碳传感器,检验装置内已充满二氧化碳的实验方法是(简述实验操作和现象)。
Ⅱ.探究装置丙硬质玻璃管内剩余固体的性质并测定其组成
查阅资料:氧化亚铜为红色粉末,可与稀硫酸反应生成铜、硫酸铜和水。
实验Ⅰ结束后将装置丙硬质玻璃管内的剩余固体全部移至烧杯中,加入足量稀硫酸,充分反应,滤出烧杯中的红色固体,洗涤、干燥、称量,其质量为2.56g。
(4)、装置丙硬质玻璃管内剩余固体中铜单质的质量分数为(结果精确到0.1%)。四、计算题
-
13. 项目小组利用如图所示装置电解水并收集干燥的氢气和氧气。
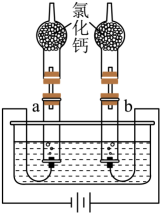 (1)、接通电源,收集a气体,靠近火焰,观察到气体燃烧,发出淡蓝色火焰,说明该气体是(填“氢气”或“氧气”)。(2)、一段时间后断开电源,实验前后整个装置的质量减少了0.9g,写出通电过程中反应的化学方程式并计算生成氧气的质量(不考虑水的蒸发)。
(1)、接通电源,收集a气体,靠近火焰,观察到气体燃烧,发出淡蓝色火焰,说明该气体是(填“氢气”或“氧气”)。(2)、一段时间后断开电源,实验前后整个装置的质量减少了0.9g,写出通电过程中反应的化学方程式并计算生成氧气的质量(不考虑水的蒸发)。
-