广东省深圳市蛇口育才教育集团育才三中2025年中考三模化学试卷
试卷更新日期:2025-06-19 类型:中考模拟
一、选择题(共10小题,每小题1.5分,共15分。在每小题给出的四个选项中,只有一项符合题目要求)
-
1. 2025年6月5日是第54个“世界环境日”。下列做法对保护环境不利的是A、大量使用化肥和农药,增加产量 B、提倡使用可降解塑料袋 C、将废旧电池统一回收并处理 D、绿色出行2. 下列化学用语表达正确的是A、氢氧根: B、铝元素:AL C、:2个亚铁离子 D、氧化钠:3. 我国著名化学家张青莲为相对原子质量测定作出卓越贡献。下图是元素周期表的一部分,说法正确的是
 A、两种元素都属于非金属元素 B、锑原子的核外电子数为51 C、铟原子由质子和中子构成 D、锑的原子质量是121.84. 下列劳动实践与所述化学知识不相符的是
A、两种元素都属于非金属元素 B、锑原子的核外电子数为51 C、铟原子由质子和中子构成 D、锑的原子质量是121.84. 下列劳动实践与所述化学知识不相符的是选项
劳动实践
化学知识
A
用加碘盐调味
碘元素预防甲状腺肿大
B
燃气灶火焰呈黄色时调大进风口
氧气充足可使燃料充分燃烧
C
自来水厂明矾净水
明矾杀菌消毒
D
硫酸铜溶液识别假黄金(Cu-Zn合金)
锌能与硫酸铜反应
A、A B、B C、C D、D5. 如图为初中化学常见的五种物质之间的关系,图中“—”表示两种物质能够发生反应,“→”表示两种物质间可转化,下列说法错误的是 A、反应①中M若为酚酞试液,观察到溶液变红 B、反应③可加入氯化镁溶液实现反应 C、俗称纯碱、苏打,可用于洗涤剂的生产 D、②属于中和反应,反应④产生白色沉淀6. 甲醇被誉为“液态阳光”。利用太阳能制甲醇的微观图示如下,下列说法正确的是
A、反应①中M若为酚酞试液,观察到溶液变红 B、反应③可加入氯化镁溶液实现反应 C、俗称纯碱、苏打,可用于洗涤剂的生产 D、②属于中和反应,反应④产生白色沉淀6. 甲醇被誉为“液态阳光”。利用太阳能制甲醇的微观图示如下,下列说法正确的是 A、步骤①中,产生氢气与氧气的质量比 B、步骤②中生成物的分子个数比 C、图中所示的转化过程中有3种氧化物 D、甲醇由碳、氢、氧三个元素组成7. 下列实验方案设计合理的是A、
A、步骤①中,产生氢气与氧气的质量比 B、步骤②中生成物的分子个数比 C、图中所示的转化过程中有3种氧化物 D、甲醇由碳、氢、氧三个元素组成7. 下列实验方案设计合理的是A、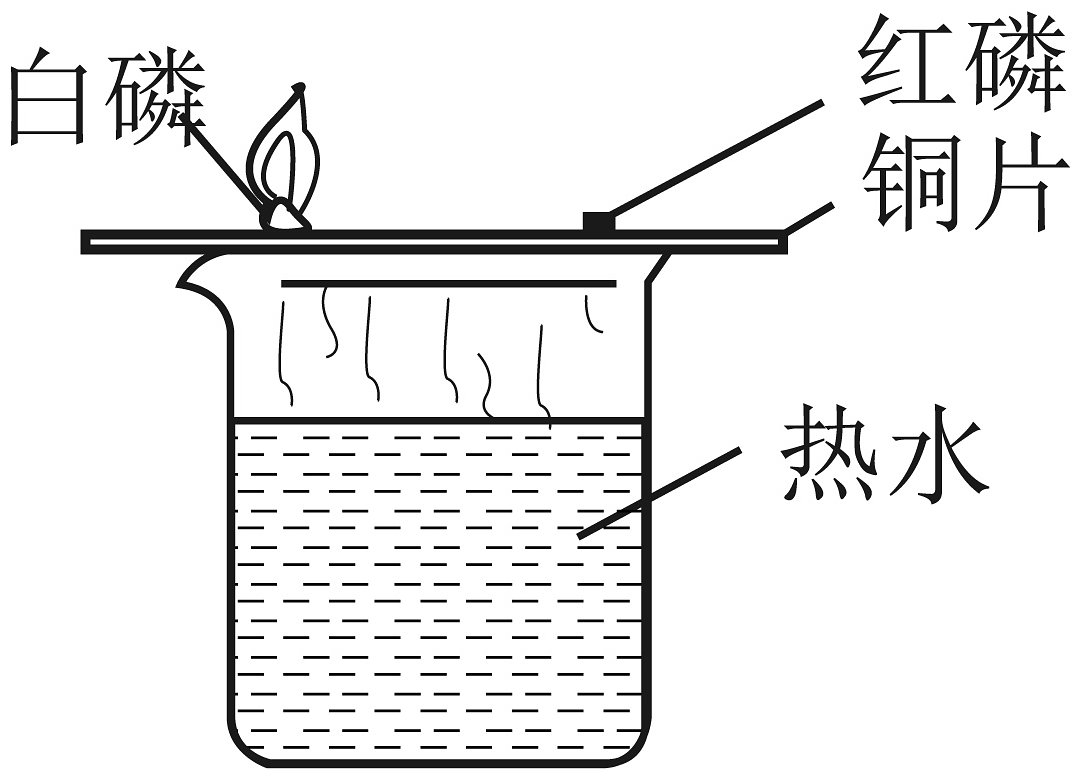 探究燃烧需要氧气
B、
探究燃烧需要氧气
B、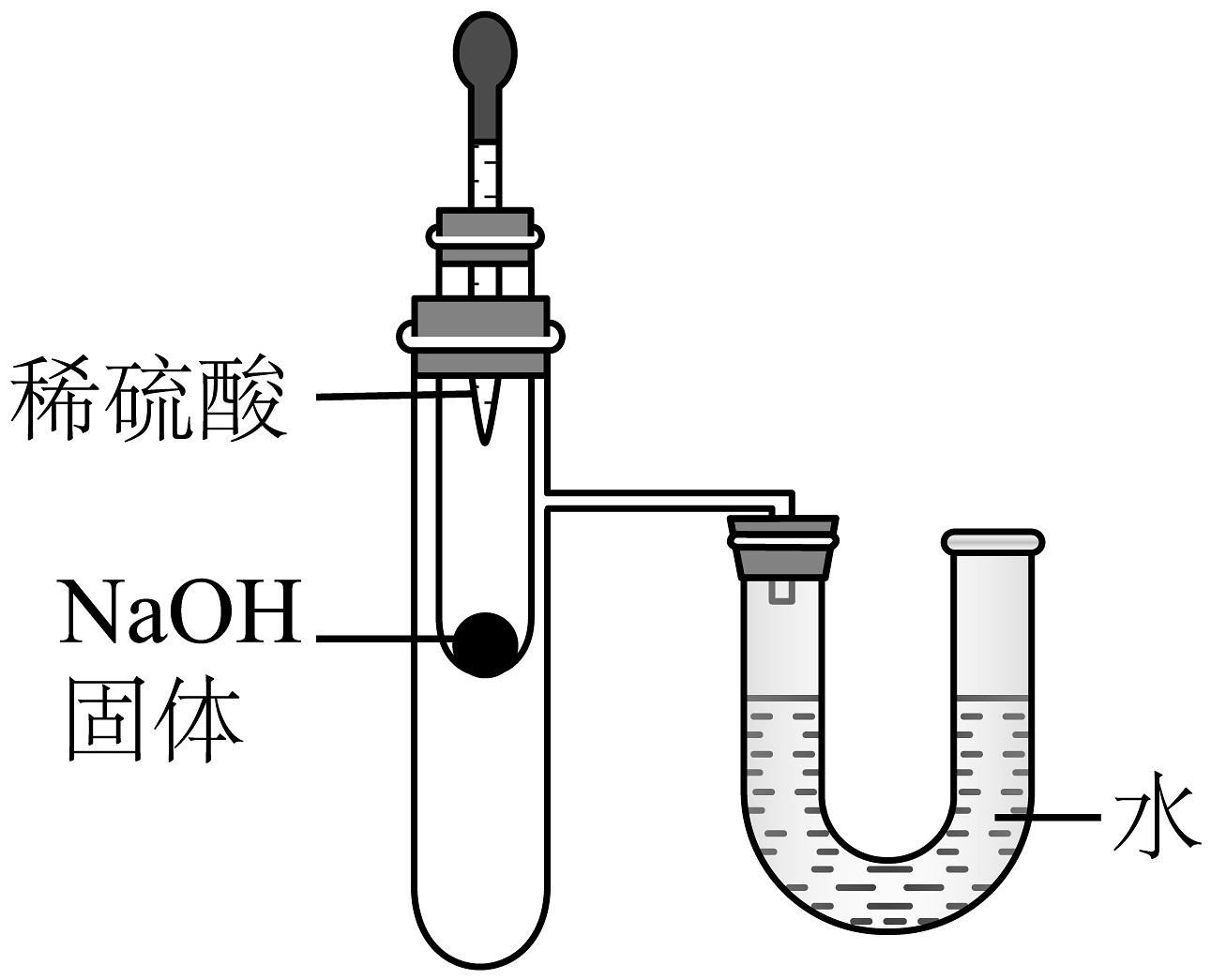 探究酸碱中和反应放热
C、
探究酸碱中和反应放热
C、 探究甲烷中含氢元素
D、
探究甲烷中含氢元素
D、 探究铁生锈的条件
8. 和的溶解度曲线如图所示。下列说法正确的是
探究铁生锈的条件
8. 和的溶解度曲线如图所示。下列说法正确的是 A、溶质的质量分数大小比较: B、将饱和溶液从升温到无晶体析出 C、饱和溶液中溶质质量分数为37.5% D、混有少量的溶液,将其蒸发浓缩后降温结晶可提纯晶体9. 下列实验操作能达到实验目的的是
A、溶质的质量分数大小比较: B、将饱和溶液从升温到无晶体析出 C、饱和溶液中溶质质量分数为37.5% D、混有少量的溶液,将其蒸发浓缩后降温结晶可提纯晶体9. 下列实验操作能达到实验目的的是选项
实验目的
实验操作
A
除去KCl中混有的固体
滴加过量溶液,过滤
B
鉴别CO和
分别通过灼热氧化铜
C
检验敞口放置的NaOH变质程度
加入适量溶液,过滤,向滤液加酚酞溶液,观察现象
D
除去中的少量HCl
通过盛有NaOH溶液的洗气瓶
A、A B、B C、C D、D10. 用三颈烧瓶收集一瓶 , 然后将三颈烧瓶与盛有盐酸、NaOH溶液的注射器和压强传感器密封连接(如图1)。检验气密性后,在时快速注入一种溶液,时快速注入第二种溶液,测得瓶内压强随时间变化曲线如图2,下列说法中正确的是 A、时注入的溶液是盐酸 B、期间发生反应: C、后压强增大的原因是NaOH溶液与盐酸发生反应 D、期间压强不变且大于0可证明收集的气体不纯
A、时注入的溶液是盐酸 B、期间发生反应: C、后压强增大的原因是NaOH溶液与盐酸发生反应 D、期间压强不变且大于0可证明收集的气体不纯二、【科普阅读】
-
11. 加快能源转型升级,发展新质生产力。氢气是最理想的清洁能源,依据不同制取方式,可分为“绿氢”“灰氢”“蓝氢”“紫氢”和“金氢”等,如图带你认识“多彩”的氢。
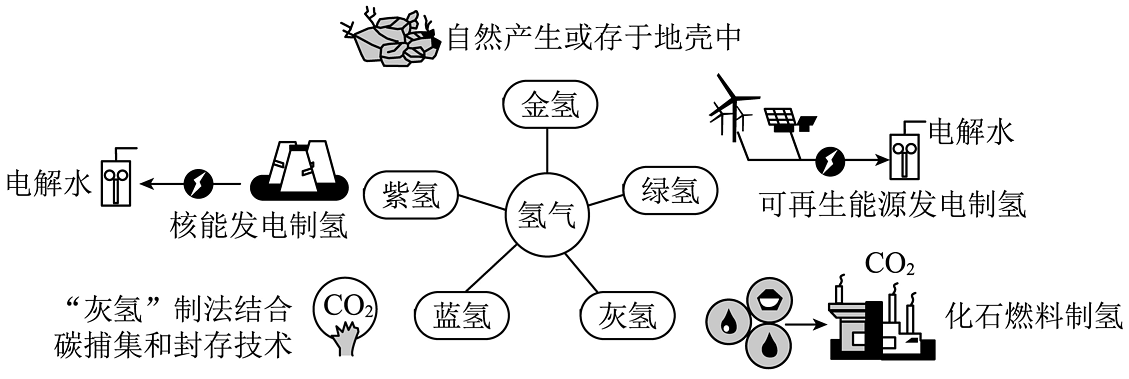
储氢是实现氢能广泛应用的重要环节,分为物理储氢和化学储氢,前者包括高压气态、低温液态、吸附等储存方式,后者将氢气转化为其他化合物进行储存。“液氨储氢”的原理是氢气与氮气在一定条件下生成氨气,进行储存。
(1)、下列选项,属于“绿氢”是_______(填字母)。A、煤燃烧发电制氢 B、风能发电制氢 C、核能发电制氢(2)、灰氢的制备过程发生的是(选填“物理”或“化学”)变化。(3)、“液氨储氢”的化学方程式。(4)、在电解水反应中,下面三个图出现的先后顺序是(填写字母)。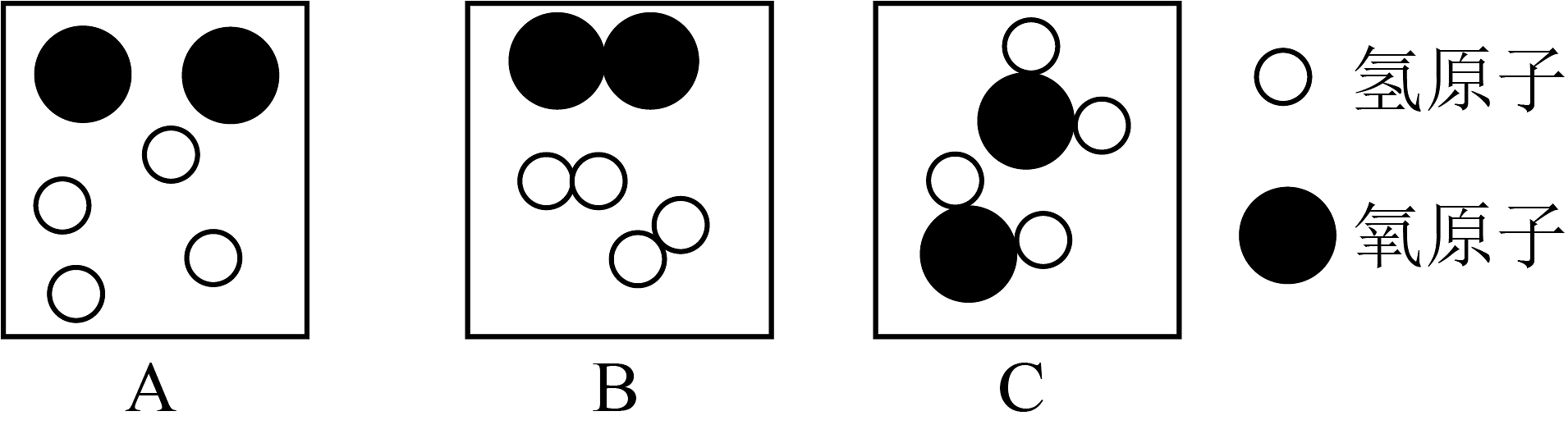 (5)、氢气燃烧发出色火焰,相比化石能源,氢能的优点有。12.
(5)、氢气燃烧发出色火焰,相比化石能源,氢能的优点有。12.松花蛋是我国特有的一种传统美食。化学兴趣小组同学进行了“松花蛋制作”的项目研究,请结合任务回答问题。
【任务一】初识松花蛋,查阅营养成分
(1)松花蛋,又称皮蛋,制作原料为鸡蛋,鸡蛋中富含的营养素为________,除此之外,还含有油脂、维生素及无机盐等多种营养素,具有较高的营养价值。【任务二】品尝松花蛋,感受松花蛋的酸碱性。
(2)同学们品尝松花蛋时,发现松花蛋略有涩味,推测松花蛋中含有碱性物质,生活中食用时可加入________(选填“料酒、食醋或酱油”)来减少涩味。【任务三】浸松花蛋粉,寻找涩味缘由
(3)取适量松花蛋粉(用于制作松花蛋泥的原料),加入足量水,搅拌、过滤。向滤液中加入________溶液(填写指示剂名称),溶液变红证明滤液中含有碱性物质。【提出问题】滤液中的碱性物质是什么?
【查阅资料】松花蛋粉中主要含有生石灰、食盐、纯碱等。
【分析推理】
(4)松花蛋粉加水调和时发生如下反应:①;
②________
【提出猜想】
(5)猜想1:NaOH;猜想2:NaOH和;猜想3:NaOH和________(填化学式);(6)设计实验验证猜想实验方案
实验现象
实验结论
操作一:取少量滤液于试管中,向其中加入过量的稀盐酸
无明显实验现象
猜想________不成立
操作二:________
________
猜想2成立
【讨论交流】
(7)根据复分解反应发生的条件,操作1中除可用稀盐酸外,还可选用_______也能达到同样实验目的。A. 酸碱指示剂 B. 氯化钾溶液 C. 氢氧化钙溶液 D. 氯化钡溶液 13.我国新能源汽车产业不仅推动了汽车技术的进步;也带动了相关产业链的发展。
Ⅰ.外观结构
化学材料在“新能源汽车”的推广中发挥着重要作用。
(1)车漆:汽车漆面保护膜采用TPU材料,能有效防止剐蹭、飞溅颗粒对车漆造成永久伤害。车身喷漆的防锈原理是。
(2)轮胎:汽车轮胎含有合成橡胶、炭黑和钢丝等材料,其中属于有机合成材料的是。
Ⅱ.动力转化
(3)电池为新能源汽车提供动力。依据图1甲,目前国内新能源汽车的电池多采用锂电池的主要原因是:(写一点)。

(4)磷酸亚铁锂电池常被用作动力源,请将制备原理补充完整:(填写化学式)。
Ⅲ.废料处理
废磷酸亚铁锂材料(主要成分为)的回收再利用工艺如图2。

(5)为高效回收锂,“酸浸”需提高锂元素浸出率,抑制磷元素、铁元素浸出率。如题图2甲,最佳反应温度为。
(6)沉锂:往浸出液(主要溶质为)中加饱和溶液,生成沉淀和另一种盐,化学方程式为。
(7)锂原子失去电子形成(填写微粒符号),锂、钠、钾等金属很容易失去电子,所以常被用作电池材料。研究表明,半径越大的金属离子越容易在电池正负极之间移动,充电速度越快。如图2乙,可得出结论:电池容量相同的这三种电池,充满电时间最短的是电池。
14. 《天工开物》中有“煤饼烧石成灰”的记载,“烧石成灰”是指高温煅烧石灰石(主要成分为)生成CaO和气体X。兴趣小组以石灰石为原料制备轻质碳酸钙的工艺如图所示。石灰石中含少量: , 不参加反应,也不溶于水。 (1)、煅烧石灰石时,通常要将石灰石粉碎,这样做的目是。(2)、操作Ⅰ的名称为。气体X通入操作Ⅰ得到的滤液中,发生的反应(用化学方程式表示)。(3)、为测定该石灰石中碳酸钙的含量(碳酸钙占石灰石的质量百分数),兴趣小组取12.5g该石灰石样品,高温灼烧充分反应后,剩余固体质量为8.1g(杂质不发生反应)。请计算:该石灰石中碳酸钙的质量分数是多少?(写出计算过程)(4)、写出气体X在生活中的用途(写一条)
(1)、煅烧石灰石时,通常要将石灰石粉碎,这样做的目是。(2)、操作Ⅰ的名称为。气体X通入操作Ⅰ得到的滤液中,发生的反应(用化学方程式表示)。(3)、为测定该石灰石中碳酸钙的含量(碳酸钙占石灰石的质量百分数),兴趣小组取12.5g该石灰石样品,高温灼烧充分反应后,剩余固体质量为8.1g(杂质不发生反应)。请计算:该石灰石中碳酸钙的质量分数是多少?(写出计算过程)(4)、写出气体X在生活中的用途(写一条)