浙江省温州市育英国际实验学校2019-2020学年八年级上学期科学开学考试B班检测试卷
试卷更新日期:2019-09-16 类型:开学考试
一、选择题(每小题2分,共40分)
-
1. 下列四个图形属于符号的是( )


A、原子结构
B、节水标志
C、甲烷分子结构
D、足球烯结构
A、A B、B C、C D、D2. 如图是水分子分解过程示意图,据图可以得知( )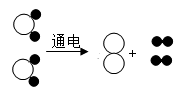 A、水是由氢气和氧气组成 B、水在一定条件下可以分解为氢气和氧气 C、水分子中含有氢分子和氧原子 D、水分子中氢原子和氧原子可以再分3. 近年,我国科学家首次拍摄到水分子团簇图像,模型如图。下列说法正确的是( )
A、水是由氢气和氧气组成 B、水在一定条件下可以分解为氢气和氧气 C、水分子中含有氢分子和氧原子 D、水分子中氢原子和氧原子可以再分3. 近年,我国科学家首次拍摄到水分子团簇图像,模型如图。下列说法正确的是( ) A、氢、氧两种元素只能组成水 B、团簇中的水分子不再运动 C、水蒸气冷凝成水,分子间空隙减小 D、水分子聚合在一起后化学性质发生了改变4. 国产大型客机C919部分机身采用了新型的铝锂合金,这种材料具有较高的强度和适宜的延展性。铝锂合金中的铝(Al)元素与锂(Li)元素的本质区别是( )A、元素符号不同 B、原子质量不同 C、原子的质子数不同 D、原子的电子数不同5. 关于原子及原子结构发现史的说法不正确的是( )A、汤姆森、卢瑟福两位科学家都是在实验的基础上,通过推理和想象建构原子模型 B、汤姆森发现了电子,证实原子是可分的 C、原子的最外层电子数发生变化时,元素的种类也发生了变化 D、原子在化学变化中的表现主要取决于原子的最外层电子6. 地壳中含量最多的金属元素、非金属元素和空气中含量最多的元素组成的化合物的化学式是( )A、Al(NO3)3 B、CaCO3 C、Al2(SO4)3 D、Fe(NO3)37. 与铵根离子(NH )具有相同的质子数和电子数的微粒是( )
A、氢、氧两种元素只能组成水 B、团簇中的水分子不再运动 C、水蒸气冷凝成水,分子间空隙减小 D、水分子聚合在一起后化学性质发生了改变4. 国产大型客机C919部分机身采用了新型的铝锂合金,这种材料具有较高的强度和适宜的延展性。铝锂合金中的铝(Al)元素与锂(Li)元素的本质区别是( )A、元素符号不同 B、原子质量不同 C、原子的质子数不同 D、原子的电子数不同5. 关于原子及原子结构发现史的说法不正确的是( )A、汤姆森、卢瑟福两位科学家都是在实验的基础上,通过推理和想象建构原子模型 B、汤姆森发现了电子,证实原子是可分的 C、原子的最外层电子数发生变化时,元素的种类也发生了变化 D、原子在化学变化中的表现主要取决于原子的最外层电子6. 地壳中含量最多的金属元素、非金属元素和空气中含量最多的元素组成的化合物的化学式是( )A、Al(NO3)3 B、CaCO3 C、Al2(SO4)3 D、Fe(NO3)37. 与铵根离子(NH )具有相同的质子数和电子数的微粒是( )
A、Na+ B、OH- C、H2O D、LiF8. 已知微观粒子π+介子、π-介子都是由一个夸克(夸克u或夸克d)和一个反夸克(反夸克u或反夸克 )组成的,它们的带电量如下表所示,表中e表示一种电量单位,称为元电荷。π+
π-
u
d
带电量
+e
-e
+ e
- e
- e
+ e
下列说法正确的是( )
A、π+由u和 组成 B、π+由d和u组成 C、π-由u和 组成 D、π-由d和u组成9. 胭脂红是一种安全的食品添加剂,其化学式是C20H11N2O10S3Na3 . 下列关于胭脂红的说法正确的是( )A、该物质是由五种元素组成的 B、1个胭脂红分子中含有49个原子 C、该化合物中硫元素的质量分数最大 D、该化合物的相对分子质量为604g10. 著名科学家居里夫人首先发现某些原子具有放射性,即原子能自动放射出一些粒子。若一种元素的原子经过放射变成了另一种元素的原子,则此原子放射出的粒子中一定有 ( )A、电子 B、中子 C、质子 D、原子核11. 下列概念中,前者从属于后者的是( )A、化合物 纯净物 B、单质 化合物 C、化合物 单质 D、化合物 混合物12. 科学上用符号“ZAX”表示原子的组成,其中X代表元素符号,Z表示原子核内的质子数,A表示原子核内质子数与中子数之和。已知abXn+和cdYm-的核外电子数相等。则下列关系正确的是( )
A、b-a=d-c B、a+n=c-m C、a-n=c+m D、b-n=d+m13. 对于Fe、Fe2+、Fe3+三种粒子的判断,正确的是( )①核电荷数相同 ②核外电子数相等 ③质量几乎相等 ④所含的质子数相等
A、①③④ B、②③ C、①②④ D、③④14. 喜树中含有一种被称为喜树碱的生物碱,这种碱的相对分子质量在300~400之间,实验分析得知其元素组成为:C占69.0%、O占18.4%,且O含量为H的4倍,其余为N,则一个喜树碱分子中含有的原子总数为( )A、42 B、43 C、44 D、4515. 如图为某化学反应的微观示意图,图中“●”表示硫原子,“○”表示氧原子.下列说法中错误的是( )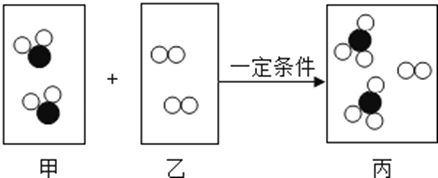 A、甲是SO2 B、该反应属于化合反应 C、反应前后,分子、原子种类均不变 D、反应中,甲、乙、丙三种物质的分子个数比为2:1:216. 思维导图有助于建构知识,如图是小金建立的有关物质宏观组成和微观构成的思维导图,其中“▲”应填入的是( )
A、甲是SO2 B、该反应属于化合反应 C、反应前后,分子、原子种类均不变 D、反应中,甲、乙、丙三种物质的分子个数比为2:1:216. 思维导图有助于建构知识,如图是小金建立的有关物质宏观组成和微观构成的思维导图,其中“▲”应填入的是( ) A、原子 B、中子 C、电子 D、质子17. 2019年联合国把今年定为“元素周期表年”。俄国科学家门捷列夫对元素周期表的编制做出巨大贡献,人们将101号元素命名为“钔”来纪念他。钔原子的核电荷数为101,相对原子质量为258,则钔原子的质子数为( )A、101 B、157 C、258 D、35918. 高氯酸钾(化学式为KClO4)是烟花中常用的氧化剂,可增加烟花的亮度。高氯酸钾中氯元素的化合价为( )A、-7 B、-1 C、+5 D、+719. 对于m个SO3分子和n个SO2分子,下列相应的结论正确的是( )A、氧原子的个数比为3m:2n B、氧元素的质量比为m:n C、硫原子的个数比为6m:5n D、硫元素的质量比为3m:2n20. 作为相对原子质量标准的碳—12 可以写成 12C。1 个 12C 的原子的质量为 akg,1 个 12CO2 分子的质量为 bkg,若以 12CO2 分子中的 1 个氧原子质量的 1/16 作为相对原子质量的标准,则 12CO2 的相对分子质量是( )A、 B、 C、 D、
A、原子 B、中子 C、电子 D、质子17. 2019年联合国把今年定为“元素周期表年”。俄国科学家门捷列夫对元素周期表的编制做出巨大贡献,人们将101号元素命名为“钔”来纪念他。钔原子的核电荷数为101,相对原子质量为258,则钔原子的质子数为( )A、101 B、157 C、258 D、35918. 高氯酸钾(化学式为KClO4)是烟花中常用的氧化剂,可增加烟花的亮度。高氯酸钾中氯元素的化合价为( )A、-7 B、-1 C、+5 D、+719. 对于m个SO3分子和n个SO2分子,下列相应的结论正确的是( )A、氧原子的个数比为3m:2n B、氧元素的质量比为m:n C、硫原子的个数比为6m:5n D、硫元素的质量比为3m:2n20. 作为相对原子质量标准的碳—12 可以写成 12C。1 个 12C 的原子的质量为 akg,1 个 12CO2 分子的质量为 bkg,若以 12CO2 分子中的 1 个氧原子质量的 1/16 作为相对原子质量的标准,则 12CO2 的相对分子质量是( )A、 B、 C、 D、二、填空题(6小题,21题每空1分,其它小题每空2分,共32分)
-
21. 用符号或化学式表示:(1)、n个硫原子;(2)、4个硝酸根离子;(3)、氦气;(4)、氯化钙中钙元素的化合价为+2 价。22. 下列物质中:①空气②酱油③食醋④汞⑤水⑥矿泉水⑦氧气⑧氢气⑨二氧化碳⑩铁。纯净物的是 , 混合物的是。23. 原子、分子、离子都是构成物质的微观离子。在氮气、水、汞、氯化钠、铁,这五种物质中,由原子构成的物质是 , 由分子构成的物质是。24. 元素周期表是学习科学的重要工具。下表是元素周期表的一部分,请回答下列问题。
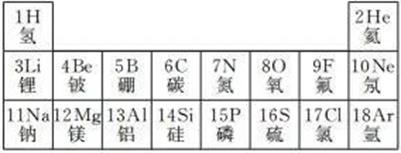 (1)、不同种元素之间最本质的区别是 不同。A、相对原子质量 B、质子数 C、中子数(2)、第3号元素属于(选填“金属”或“非金属")元素。(3)、第12号元素和第17号元素组成化合物的化学式是。25. 下表是某位同学收集的一些微粒的资料,请根据表格数据回答下列问题。
(1)、不同种元素之间最本质的区别是 不同。A、相对原子质量 B、质子数 C、中子数(2)、第3号元素属于(选填“金属”或“非金属")元素。(3)、第12号元素和第17号元素组成化合物的化学式是。25. 下表是某位同学收集的一些微粒的资料,请根据表格数据回答下列问题。粒子名称
质子数
中子数
电子数
带电性
A
14
14
14
不带电
B
26
30
24
带 2 个单位正电荷
C
14
14
16
D
14
16
14
不带电
(1)、上述粒子中属于原子的是。(2)、表格中互为同位素的粒子是。(3)、比较 C 与 D 两种粒子,其中质量较大的是。26.(1)、某三价金属与氧元素形成的化合物中氧元素质量分数为30%,则该金属的相对原子质量为。(2)、A、B两元素相对原子质量之比为2∶1,仅由这两种元素组成的化合物里,A、B两元素质量比为2∶3,则该化合物的化学式为;若其中B为-n价,则此化合物中A元素的化合价为。(3)、元素R可与氧形成多种化合物,其中RO中含氧53.33%,那么相对分子质量为76,含氧量为63.16%的R与氧元素形成的化合物的化学式是。三、探究题(2小题,每空2分,共14分)
-
27. 由碳、氢元素组成的物质种类繁多,烷烃就是其中一类重要的物质,表中列出了烷烃的一些信息.
名称
甲烷
乙烷
丙烷
丁烷
戊烷
十一烷
十六烷
化学式
CH4
C2H6
C3H8
?
C5H12
C11H24
C16H34
沸点(℃)
-164
-88.6
-42.1
-0.5
36.1
194.5
287.5
相对密度
0.466
0.572
0.585
0.579
0.626
0.741
0.774
分析上表中的信息,回答下列问题:
(1)、烷烃的命名与分子中原子个数有关.(2)、总结一条烷烃物理性质的递变规律28. 电子带负电,原子不带电,说明原子内存在着带正电荷的部分,它们是均匀分布还是集中分布的呢?1910 年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。实验做法如图: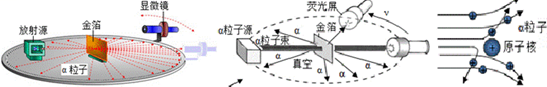
绝大多数α粒子穿过金箔后仍沿原来的方向前进,但是有少数 α 粒子却发生了较大的偏转,并且有极少数α粒子的偏转超过 90°,有的甚至几乎达到 180°,像是被金箔弹了回来。
【猜想与假设】α粒子遇到电子后,就像飞行的子弹碰到灰尘一样运动方向不会发生明显的改变,而结果却出乎意料,除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的。
【解释与结论】
(1)、大多数α粒子不改变原来的运动方向,原因是;(2)、若原子质量、正电荷在原子内均匀分布,则极少数 α 粒子就(填“会”或“不会”)发生大角度散射。卢瑟福所说的“除非原子的大部分质量集中到了一个很小的结构上”中的“很小的结构”指的是;(3)、科学家对原子结构的探究经历了三个过程,通过α 粒子散射实验,你认为原子结构为以下的 。A、 B、
B、 C、
C、
四、解答题(2小题,29小题6分,30小题8分,共14分)
-
29. 如图分别是物质发生变化的微观示意图。
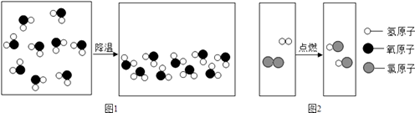
请回答:
(1)、图1表示的变化,从微观角度看改变的是。(2)、图2表示的变化,所表示的宏观事实是。(3)、图2表示的变化,从微观角度看,在变化前后,一定不变的是。30. “珍爱生命,拒绝毒品”是每个公民的责任,但是在某些娱乐场所,还有人服用俗称“摇头丸”的毒品。该毒品能使人手舞足蹈,呈癫狂状态,严重危害人的身心健康和社会稳定,有一种“摇头丸”的化学式为C12HxO2N,相对分子质量为209。试回答下列问题:(1)、该物质的一个分子中含氢原子个,碳元素与氧元素的质量比为。(2)、该物质中氮元素的质量分数是多少(结果保留到0.1%)(3)、418g“摇头丸”中含多少克氮元素。(结果保留到整数)