四川省南充市2017-2018学年中考化学三模考试试卷
试卷更新日期:2018-06-01 类型:中考模拟
一、单选题
-
1. 生活中下列物质的用途主要利用其化学性质的是( )A、大理石用作建筑材料 B、干冰用于人工降雨 C、铁粉用作月饼的保鲜剂 D、稀有气体用于制作霓虹灯2. 下列做法不符合“改善环境质量,推动绿色发展”理念的是( )
A、鼓励使用共享单车 B、鼓励使用一次性餐具 C、鼓励自带布袋购物 D、鼓励乘坐公共交通工具3. 下列对化学基本观念的认识错误的是( )A、能量观:所有燃烧都是放热反应、 B、守恒观:所有的化学变化都遵守质量守恒定律 C、分类观:凡是含碳元素的化合物都是有机物 D、结构观:元素的化学性质是由原子的最外层电子数决定的4. 自制汽水的原料有糖、小苏打、柠檬酸(C6H8O7),下列关于柠檬酸的说法中正确的是( )
A、柠檬酸中氧元素的质量分数最大 B、柠檬酸的相对分子质量是192g C、柠檬酸分子是由碳元素、氧元素、氢元素组成的 D、柠檬酸分子是由6个碳原子、8个氢原子和7个氧原子构成的5. 自来水消毒的微观过程可用下图表示,下列说法正确的是( ) (
(  表示氧原子,
表示氧原子,  表示氢原子,
表示氢原子,  表示氯原子)A、化学变化中分子不会再分 B、A,C,D都是氧化物 C、该反应属于置换反应 D、参加反应的两种分子个数比是1:16. 根据下列实验方案进行实验,其中存在错误的是( )A、
表示氯原子)A、化学变化中分子不会再分 B、A,C,D都是氧化物 C、该反应属于置换反应 D、参加反应的两种分子个数比是1:16. 根据下列实验方案进行实验,其中存在错误的是( )A、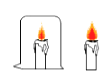 探究燃烧需要氧气
B、
探究燃烧需要氧气
B、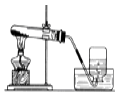 高锰酸钾制取氧气
C、
高锰酸钾制取氧气
C、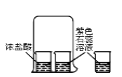 证明为力在不断运动
D、
证明为力在不断运动
D、 测定空气中洋气的含量
7. 甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )
测定空气中洋气的含量
7. 甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示,下列说法正确的是( ) A、升高温度,可使甲的饱和溶液变为不饱和溶液 B、50℃时,可以配制溶质质量分数是20%的乙溶液 C、50℃时分别在100 g水中加入20 g甲、乙充分搅拌,再同时降温至20℃,甲、乙溶液均变为饱和溶液 D、20℃时乙溶液的溶质质量分数一定大于甲8. 化学知识来源于生活又服务于生活。下列有关化学知识在生活生产中的运用,错误的是( )A、用熟石灰中和酸性土壤 B、室内起火马上打开所有的门窗通风 C、煮沸、蒸馏的方法都能将硬水软化 D、洗洁精除去餐具上的油污是“乳化作用”9. 下列实验操作能达到实验目的的是( )
A、升高温度,可使甲的饱和溶液变为不饱和溶液 B、50℃时,可以配制溶质质量分数是20%的乙溶液 C、50℃时分别在100 g水中加入20 g甲、乙充分搅拌,再同时降温至20℃,甲、乙溶液均变为饱和溶液 D、20℃时乙溶液的溶质质量分数一定大于甲8. 化学知识来源于生活又服务于生活。下列有关化学知识在生活生产中的运用,错误的是( )A、用熟石灰中和酸性土壤 B、室内起火马上打开所有的门窗通风 C、煮沸、蒸馏的方法都能将硬水软化 D、洗洁精除去餐具上的油污是“乳化作用”9. 下列实验操作能达到实验目的的是( )选项
实验目的
实验操作
A
区别空气、氧气和氮气
分别伸入带火星的木条
B
提纯含少量KNO3的NaCl
配成高温时的热饱和溶液、降温结晶、过滤
C
鉴别CuO粉末和碳粉
分别加稀硫酸观察溶液颜色是否变化
D
除去KCl溶液中少量CuCl2
滴加NaOH溶液,至不再生成沉淀,过滤
A、A B、B C、C D、D10. 下列图象能正确反映其对应的实验操作的是( )A、 加热一定量的高锰酸钾固体
B、
加热一定量的高锰酸钾固体
B、 向一定量的MnO2中加入H2O2溶液
C、
向一定量的MnO2中加入H2O2溶液
C、 向一定质量的饱和石灰水中加入生石灰
D、
向一定质量的饱和石灰水中加入生石灰
D、 向一定质量的AgNO3和Cu(NO3)2的混合溶液中不断加入铁粉
向一定质量的AgNO3和Cu(NO3)2的混合溶液中不断加入铁粉
二、综合题
-
11. 自动充气气球因使用方便,无需其它充气器材而逐渐得以推广。某化学兴趣小组对自动充气气球进行了如下探究。

【查阅资料】①自动充气气球的结构如图所示,气球的充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气。
②氯化银是一种白色沉淀且不溶于稀硝酸。
(1)、探究液体包的成分:取液体包中的少量溶液分别放于两只于试管中,在其中一只试管中加入锌粒产生气泡,另一只试管中滴加硝酸银溶液,产生白色沉淀,继续滴加稀硝酸沉淀不溶,则小组同学证明液体包中装的是 , 写出该液体与锌粒反应的化学方程式。
(2)、探究白色粉末成分:【猜想与假设】甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠。
【设计并进行实验】实验一:完成下表
操作步骤
现象
结论
甲同学的猜想错误
(3)、实验二:按下图的实验装置,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的烧瓶中注入等体积、足量的稀盐酸,并测量生成二氧化碳的体积,记录如下表:
实验编号
锥形瓶内物质
最终得到CO2
体积/mL
名称
质量/g
①
碳酸氢钠
0.8
V1
②
碳酸钠
0.8
V2
③
白色粉末
a
V1
实验装置中植物油的作用是;表中a= ;V1V2(填“>”、“<”或“=”)。
(4)、【分析并得出结论】分析上表中数据得出结论:白色粉末的成分是 , 依据是。三、填空题
-
12. 厕所中有刺激性气味的氨气(NH3)是小便中的尿素分解产生的。
(1)、标出氨气中氮元素的化合价;(2)、工业上在高温和催化剂的条件下,可用氨气制得氢气,其反应类型与水电解制氢气相同,生成物也都为单质。该反应的化学方程式为。13. 这个季节草莓是最受大众喜爱的水果。星期天小红和妈妈去采摘草莓,发现生活中有很多知识与化学有关。请回答:(1)、草莓大棚所用的塑料薄膜属于_________________(填序号,下同)。A、天然材料 B、金属材料 C、有机合成材料(2)、用发酵后的豆浆或豆渣做肥料,种出的草莓又大又甜。发酵后的豆浆或豆渣含有C、H、K和P等元素。浇发酵后的豆浆或豆渣相当于施加了____________。
A、氮肥 B、磷肥 C、钾肥 D、复合肥14. 国际上提倡向中国人学习用铁锅炒菜。工业上常用赤铁矿(主要成分氧化铁)和一氧化碳冶炼生铁,该反应的化学方程式为。用铁锅炒菜时,油锅中的油不慎起火,只需一个简单的操作,火就熄灭了,该操作是 , 其灭火的原理是。
15. “五一”长假,小明和化学兴趣小组的同学去实验室做实验,请你根据下图所示的实验过程,回答问题: (1)、烧杯①加入石灰水后发生反应的化学方程式为。(2)、烧杯②中滴加稀盐酸至过量会看到沉淀消失有气泡冒出,产生气泡的化学方程式为 , 最终烧杯③中的溶质是(写化学式)。(3)、烧杯③的废液直接倒入下水道会造成水质污染。请你帮助小明选择下列物质中的一种加入烧杯③的废液中,完全反应后再倒掉废液就不再对水质存在污染。你选择的是_____(填字母序号)。A、石蕊溶液 B、过量的氢氧化钠溶液 C、适量的氢氧化铜 D、过量的大理石16. 阅读下面科普短文
(1)、烧杯①加入石灰水后发生反应的化学方程式为。(2)、烧杯②中滴加稀盐酸至过量会看到沉淀消失有气泡冒出,产生气泡的化学方程式为 , 最终烧杯③中的溶质是(写化学式)。(3)、烧杯③的废液直接倒入下水道会造成水质污染。请你帮助小明选择下列物质中的一种加入烧杯③的废液中,完全反应后再倒掉废液就不再对水质存在污染。你选择的是_____(填字母序号)。A、石蕊溶液 B、过量的氢氧化钠溶液 C、适量的氢氧化铜 D、过量的大理石16. 阅读下面科普短文松花蛋又称皮蛋、变蛋、灰包蛋等,因剥开蛋壳后胶冻状的蛋清中常有松针状的结晶或花纹而得名,是一种我国传统风味食品。
松花蛋是用料泥包裹鸭蛋、鸡蛋等加工而成。料泥是由生石灰、纯碱、食盐、草木灰(主要成分K2CO3)等原料与水按一定比例混合均匀制得,原料中还可加入少量硫酸锌改变皮蛋的品质。料泥制作过程中,通过一系列反应,产生的强碱(NaOH、KOH)经蛋壳渗入到蛋清和蛋黄中,与其中的蛋白质作用,致使蛋白质分解、凝固并放出少量硫化氢气体和氨气。同时渗入的碱还会与蛋白质分解出的氨基酸进一步发生中和反应,生成的盐的晶体沉积在凝胶态的蛋清中,便出现了朵朵“松花”。而硫化氢气体则与蛋清和蛋黄中的矿物质作用生成各种硫化物,使蛋清和蛋黄的颜色发生改变,蛋清呈特殊的荼褐色、蛋黄则呈墨绿色。很多人在平时生活中都非常喜欢凉拌松花蛋,由于松花蛋有一股碱涩味,在吃松花蛋的时候可以加入少量的姜醋汁。但专家提醒松花蛋少吃无妨,却不能过多食用,其一,松花蛋腌制过程中蛋白质分解、变质,导致营养价值遭到了一定的破坏;其二,市售松花蛋还可能含铅(国家规定松花蛋中铅含量需小于0.5mg/kg),微量铅很容易被儿童吸收,导致铅中毒;其三,剥开皮的松花蛋1至2小时内一定要吃完,若长时间暴露在空气中,非常容易感染沙门氏杆菌,沙门氏杆菌会快速繁殖,此时食用松花蛋很容易引起中毒现象。
依据文章内容,回答下列问题:
(1)、食用松花蛋时加入_________调料可以除去松花蛋中碱涩味。A、油辣子 B、食盐 C、酱油 D、醋(2)、料泥制作过程中会生成了强碱NaOH和KOH,KOH中的钾元素来自于原料中。(3)、原料中的少量硫酸锌可为人体补充了锌这种元素(选填“常量”、“微量”)。(4)、制作松花蛋的鸡蛋、鸭蛋富含的营养素有_____________(填字母序号,下同)。A、蛋白质 B、脂肪 C、维生素(5)、下列关于松花蛋的说法正确的是_______________。A、松花蛋中蛋清和蛋黄颜色的形成与氨气有关 B、松花蛋中“松花”的形成与料泥产生的强碱有关 C、市售松花蛋可能含有少量的铅,儿童不宜食用 D、剥开皮的松花蛋隔夜放置后依然可以放心食用四、计算题
-
17. 某同学把干燥、纯净的氯酸钾和二氧化锰的混合物31.5g装入大试管中,加热制取氧气,并在不同时刻测定试管内剩余固体物质的质量(如下表):
反应时间/min
1.0
1.5
2.0
2.5
3.0
剩余固体质量/g
28.9
26.3
23.7
21.9
21.9
分析表中数据,完成下列问题:
(1)、完全反应后,生成氧气的质量为g;(2)、把剩余固体加入足量的水溶解过滤得到滤液55g(二氧化锰难溶于水),计算滤液中溶质的质量分数是多少?(精确到0.1%)
-