上海市杨浦区2017-2018学年中考化学二模考试试卷
试卷更新日期:2018-06-01 类型:中考模拟
一、单选题
-
1. 下列变化属于化学变化的是( )A、煤炭燃烧 B、冰雪消融 C、汽油挥发 D、矿石粉碎2. 属于纯净物的是( )A、雨水 B、啤酒 C、液氧 D、河水3. 在化学式 KClO3中,Cl元素的化合价是( )A、﹣1 B、+1 C、+3 D、+54. 属于有机物的是( )A、CH4 B、CO C、CO2 D、K2CO35. 下列不属于化石燃料的是( )A、氢气 B、煤 C、石油 D、天然气6. 自来水厂净化水通常不采用的方法是( )A、蒸馏 B、沉淀 C、过滤 D、消毒7. 醋的主要成分是醋酸,其化学式为CH3COOH,有关叙述正确的是( )A、用醋可以除去热水瓶、水壶中的水垢 B、醋酸是一种氧化物 C、醋酸由碳、氢、氧三种原子构成 D、醋酸的摩尔质量为608. 有关物质的俗名、学名与化学式均表示同一物质的是( )A、干冰 水 H2O B、纯碱 碳酸钠 Na2CO3 C、石灰水 氢氧化钙 Ca(OH)2 D、胆矾 硫酸铜 CuSO4∙5H2O9. 分类是学习化学的一种重要方法.以下分类正确的是( )A、常见的酸溶液:H2O HCl H2SO4 B、常见的黑色固体:CuO MnO2Fe3O4 C、常见的有还原性的物质:C CO O2 D、常见的氧化物:MgO KMnO4 H2O10. 有关物质用途的说法错误的是( )A、氯化钠用于配制生理盐水 B、干冰用于人工降雨 C、氢氧化铝用于治疗胃酸过多 D、氢氧化钠用作食品干燥剂11. 关于金刚石、石墨和C60的说法正确的是( )A、都是黑色固体 B、都具有导电性 C、都是由原子直接构成的 D、燃烧都生成二氧化碳12. 有关说法正确的是( )A、分子可分,原子不可再分 B、空气是由空气分子构成的 C、温度越高,分子运动速率越快 D、温度升高,分子体积增大13. 可燃冰主要含甲烷水合物,用作燃料时反应的微观示意图如图,下列说法正确的是( )
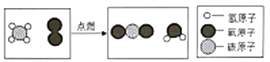 A、可燃冰中只有甲烷 B、反应前后分子总数不变 C、反应的化学方程式为CH4 + O2 CO2 + H2O D、反应前后的物质均由原子构成14. 实验操作正确且能达到实验目的是( )A、
A、可燃冰中只有甲烷 B、反应前后分子总数不变 C、反应的化学方程式为CH4 + O2 CO2 + H2O D、反应前后的物质均由原子构成14. 实验操作正确且能达到实验目的是( )A、 探究NaOH固体溶于水的能量变化
B、
探究NaOH固体溶于水的能量变化
B、 排水法收集氧气
C、
排水法收集氧气
C、 检查气密性
D、
检查气密性
D、 铁在氧气中燃烧
15. 溶解度曲线是溶解度表示方法之一。曲线上任意一点表示的是( )
铁在氧气中燃烧
15. 溶解度曲线是溶解度表示方法之一。曲线上任意一点表示的是( )
A、溶液达到饱和时溶解的溶质的质量 B、一定温度和一定质量的溶剂里溶解的溶质的质量 C、该温度时,100 g 溶剂里溶解的溶质的质量 D、该温度时,溶液处于饱和状态16. 在硫酸铜溶液中加入一定量的锌粉和铁粉,充分反应后过滤,向滤渣中加入少量稀硫酸,有气泡产生。对滤渣的叙述正确的是( )①一定有锌 ②一定有铁 ③一定有铜 ④可能有锌 ⑤可能有铁 ⑥可能有铜
A、①③⑤ B、③④⑤ C、②③④ D、①②⑥17. 对比实验是常用的实验方法,相关实验结论正确的是( )

A.CO2 能使紫色石蕊变红
B.二氧化锰是催化剂


C.金属 M 生锈需要 O
D.同种溶质在不同溶剂中的溶解性不同
A、A B、B C、C D、D18. 有关实验方案设计正确的是( )选项
实验目的
实验方案
A
检验某物质中是否含有碳酸根
加稀盐酸,观察是否有气泡冒出
B
除去KCl固体中混有的少量MnO2
加水溶解,过滤,洗涤,干燥
C
鉴别H2、CH4、CO三种气体
分别点燃,观察火焰颜色
D
鉴别稀盐酸、NaOH、NaCl三种溶液
分别滴入酚酞溶液,再相互混合,观察溶液颜色变化
A、A B、B C、C D、D19. 下列各组溶液,不外加试剂就能鉴别出来的是( )
A、NaOH、Ba(NO3)2、NaCl、MgSO4 B、NaOH、FeCl3、HCl、HNO3 C、Na2CO3、NaCl、Na2SO4、Ba(OH)2 D、Na2CO3、HCl、BaCl2、NaCl20. 向盛有一定量氧化铁粉末的烧杯中不断加入稀盐酸,烧杯中相关量的变化与图像相符的是( )
A、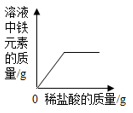 B、
B、 C、
C、 D、
D、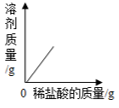 21. 向一定质量FeCl2和CuCl2的混合溶液中加入锌粉,反应过程中,混合物中溶液的质量与加入锌的质量关系如图所示,该反应过程中混合物中的溶液和固体的有关说法正确的是( )
21. 向一定质量FeCl2和CuCl2的混合溶液中加入锌粉,反应过程中,混合物中溶液的质量与加入锌的质量关系如图所示,该反应过程中混合物中的溶液和固体的有关说法正确的是( ) A、a点时,溶液中只含有两种溶质 B、c点时,向固体中滴加稀盐酸,无气泡产生 C、d点时,溶液中的溶质为ZnCl2 D、e点时,固体中只含两种物质22. 关于银的性质描述中,属于化学性质的是( )A、银是银白色的 B、银不易与氧气反应 C、银具有优良的导电性 D、银具有良好的延展性23. 人体内一些液体的近似pH如下,其中酸性最强的是( )A、血浆(7.35﹣7.45) B、胃液(0.9﹣1.5) C、唾液(6.6﹣7.1) D、尿液(4.7﹣8.4)24. 某同学对化学知识的归纳正确的是( )A、pH>7的溶液一定是碱的溶液 B、同种元素组成的物质一定是单质 C、生成盐和水的反应一定是复分解反应 D、能分解生成氧气的物质一定含有氧元素
A、a点时,溶液中只含有两种溶质 B、c点时,向固体中滴加稀盐酸,无气泡产生 C、d点时,溶液中的溶质为ZnCl2 D、e点时,固体中只含两种物质22. 关于银的性质描述中,属于化学性质的是( )A、银是银白色的 B、银不易与氧气反应 C、银具有优良的导电性 D、银具有良好的延展性23. 人体内一些液体的近似pH如下,其中酸性最强的是( )A、血浆(7.35﹣7.45) B、胃液(0.9﹣1.5) C、唾液(6.6﹣7.1) D、尿液(4.7﹣8.4)24. 某同学对化学知识的归纳正确的是( )A、pH>7的溶液一定是碱的溶液 B、同种元素组成的物质一定是单质 C、生成盐和水的反应一定是复分解反应 D、能分解生成氧气的物质一定含有氧元素二、填空题
-
25. 25、生活中处处有化学。
(1)、体温计中的液体金属化学式为。(2)、玻璃的主要成分是SiO2 , SiO2读作。(3)、生石灰常用作食品干燥剂,其干燥原理是(用化学方程式表示)。(4)、医用消毒酒精中酒精的化学式为C2H5OH,碳、氢元素原子个数比为。0.1mol酒精的质量为g ,含有个氢原子。
三、简答题
-
26. 结合如图所示实验回答问题:
 (1)、实验1电解水实验中,元素从态变化态。(2)、实验2净水器利用活性炭的性质是。(3)、实验3将燃着的蜡烛放入冰水中,观察到蜡烛火焰逐渐熄灭,原因。
(1)、实验1电解水实验中,元素从态变化态。(2)、实验2净水器利用活性炭的性质是。(3)、实验3将燃着的蜡烛放入冰水中,观察到蜡烛火焰逐渐熄灭,原因。四、选择填充题
-
27. 溶液在生产、生活中起着十分重要的作用。(1)、可作为溶质的是_______。A、只有固体 B、只有液体 C、只有气体 D、气体、液体、固体都可以(2)、物质加入足量水中,能形成无色透明溶液的是_______。A、汽油 B、面粉 C、纯碱 D、硫酸铜(3)、物质加入水中形成溶液过程中,温度会升高的是_______。A、烧碱 B、氯化钠 C、氧化钙 D、碳酸钙(4)、下表是NaCl和KNO3在不同温度时的溶解度,回答问题。
温度/℃
10
20
30
40
50
60
溶解度g/100g水
NaCl
35.8
36.0
36.3
36.6
37.0
37.3
KNO3
20.9
31.6
45.8
63.9
85.5
110.0
①两种物质中,溶解度受温度影响变化较大的是。
②NaCl和KNO3溶解度相等的温度范围是。
③KNO3晶体中含有少量NaCl,提纯KNO3晶体的方法是。
④60℃时,按图示操作:

A中溶液是(填“饱和”或“不饱和”)溶液,C中溶液的总质量是g。
⑤50℃时,将两种物质的饱和溶液各100g,分别加热蒸发10g水后,再恢复到50℃,剩余溶液的质量:NaCl溶液(填“大于”“等于”或“小于”)KNO3溶液。
五、流程题
-
28. 粗盐除去泥砂后含有氯化镁、硫酸钠、氯化钙等杂质,某同学对粗盐进一步提纯的实验操作过程如图所示:
 (1)、实验中称取5.0g粗盐,为了使粗盐充分溶解(该温度下氯化钠的溶解度为36g/100g水)量取水所用量筒的规格为__________。A、10mL B、20mL C、50mL D、100mL(2)、步骤②所加试剂X的化学式为。(3)、步骤④中加入过量碳酸钠的目的是。(4)、步骤⑤过滤实验,制作过滤器的正确顺序为。
(1)、实验中称取5.0g粗盐,为了使粗盐充分溶解(该温度下氯化钠的溶解度为36g/100g水)量取水所用量筒的规格为__________。A、10mL B、20mL C、50mL D、100mL(2)、步骤②所加试剂X的化学式为。(3)、步骤④中加入过量碳酸钠的目的是。(4)、步骤⑤过滤实验,制作过滤器的正确顺序为。
过滤后所得滤渣的化学式为。
(5)、步骤⑦蒸发实验除去(填化学式)得到精盐。29. 某干燥剂含有CaO、NaOH和CaCl2中的两种物质,为探究其成分,设计如图所示实验。依据实验流程回答相关问题。 (1)、溶液a一定显性。(2)、白色固体b一定是(填化学式)。写出可能生成白色固体的化学方程式(任写一种)。(3)、加入过量的稀HNO3的目的是。(4)、现象c:①若无白色沉淀,干燥剂成分为。
(1)、溶液a一定显性。(2)、白色固体b一定是(填化学式)。写出可能生成白色固体的化学方程式(任写一种)。(3)、加入过量的稀HNO3的目的是。(4)、现象c:①若无白色沉淀,干燥剂成分为。②若有白色沉淀,写出产生此现象的化学方程式。干燥剂成分为。
(5)、稀HNO3溶液能否用稀HCl溶液替代(填“能”或“不能”)。六、实验题
-
30. 实验一:电子天平AB的表面皿中分别盛有浓HCl、浓H2SO4 , 放置一段时间。(1)、A中的示数变小,原因是。(2)、与图C所示变化相一致的是(选填“A”或“B”)
 (3)、实验二:做对比实验,得出相应结论。
(3)、实验二:做对比实验,得出相应结论。I和II试管中都产生气泡,且I中比II中剧烈。此现象说明物质反应的快慢与有关。
III试管中可能的现象是。
请用化学方程式解释其原因、。
(4)、如图所示,比较金属的活动性大小。实验现象:试管IV比试管V中产生气泡剧烈。得出结论:金属活动性X>Y。我不赞同此结论,理由是。完成本实验需要控制的变量是。 31. 图1装置左管带孔的燃烧匙内盛有足量的锌粒,右管盛有稀硫酸。
31. 图1装置左管带孔的燃烧匙内盛有足量的锌粒,右管盛有稀硫酸。 (1)、关闭K3 , 打开K1和K2 , 除了右管液面下降,还会出现的现象是。
(1)、关闭K3 , 打开K1和K2 , 除了右管液面下降,还会出现的现象是。写出产生该现象的化学方程式。
(2)、在K1的导管口处用橡皮管连接图2的(填“a”或“b”)端收集气体。(3)、按图3进行实验,用橡皮管与K1相连接并点燃尖嘴管,可观察到的现象是;(4)、为了使反应停止,正确的操作是 , 该装置的优点是。(5)、用下列部分仪器,组装一套与上面装置有相同优点的装置,用编号表示组装的装置。
七、科学探究题
-
32. 某兴趣小组同学称取10g氧化铜和碳粉,通过下列实验对其中炭粉含量进行探究。实验前进行知识准备:2Cu + O2
 2CuO
2CuO (1)、关闭弹簧夹,打开分液漏斗活塞。写出A中的化学反应方程式。(2)、点燃酒精灯,将尖嘴管对着火焰,以提高温度,其原因是。玻璃管中发生的反应为 木炭还原氧化铜:C+ 2CuO → 2Cu + CO2↑,该反应条件是。(3)、反应一段时间,装置B中一定会观察到。装置D中澄清石灰水不变浑浊,说明。(4)、再打开弹簧夹,继续加热装置B,装置C中观察到的现象是。
(1)、关闭弹簧夹,打开分液漏斗活塞。写出A中的化学反应方程式。(2)、点燃酒精灯,将尖嘴管对着火焰,以提高温度,其原因是。玻璃管中发生的反应为 木炭还原氧化铜:C+ 2CuO → 2Cu + CO2↑,该反应条件是。(3)、反应一段时间,装置B中一定会观察到。装置D中澄清石灰水不变浑浊,说明。(4)、再打开弹簧夹,继续加热装置B,装置C中观察到的现象是。直至固体颜色不再变化后停止加热,称量装置C,质量比反应前增重4.4g,增重质量就是质量。通过计算可知装置B中含碳元素质量为g。本实验还可以通过称量 , 也能计算出原混合物中碳的质量分数。
33. 如图所示,在6支试管中分别滴加2滴紫色石蕊溶液。(资料:KCl溶液、CaCl2溶液均显中性) (1)、作为对照试验的是试管(选填①~⑥编号)。(2)、试管②、⑤溶液变为红色,其原因是溶液中溶质都含有元素。(3)、试管⑥中溶液变为蓝色,说明碳酸钾溶液显(选填“酸性”、“中性”或“碱性”)。碳酸钾属于(填物质类别),可做肥使用,取该溶液灼烧,透过蓝色钴玻璃火焰呈色。(4)、将试管⑤倒入试管④中,写出该反应的化学方程式。
(1)、作为对照试验的是试管(选填①~⑥编号)。(2)、试管②、⑤溶液变为红色,其原因是溶液中溶质都含有元素。(3)、试管⑥中溶液变为蓝色,说明碳酸钾溶液显(选填“酸性”、“中性”或“碱性”)。碳酸钾属于(填物质类别),可做肥使用,取该溶液灼烧,透过蓝色钴玻璃火焰呈色。(4)、将试管⑤倒入试管④中,写出该反应的化学方程式。充分反应后溶液呈现。
A.红色
B.紫色
C.蓝色
(5)、实验后将试管①②⑥中的废液倒入大烧杯中,最终得到红色溶液,则大烧杯的废液中除了石蕊外,一定还含有。八、计算题
-
34. 向盛有一定质量稀盐酸的烧杯中逐渐加入石灰石,产生气体质量与石灰石质量的关系如图所示。恰好完全反应后称的烧杯中剩余物质的质量为108.1g,根据关系图分析并计算:
 (1)、稀盐酸完全反应时,产生CO2气体的物质的量为。(2)、该稀盐酸溶质的质量分数为。(写出计算过程)。
(1)、稀盐酸完全反应时,产生CO2气体的物质的量为。(2)、该稀盐酸溶质的质量分数为。(写出计算过程)。
-
-
-