2018年全国版中考化学冲刺卷(一)
试卷更新日期:2018-05-30 类型:中考模拟
一、单选题
-
1. ①水的沸腾②胆矾研碎③铁丝燃烧④食物腐败等四个变化”中,属于化学变化的是( )A、①② B、①③ C、②③ D、③④2. 对下列常见物质分类,正确的是( )
①食盐水 ②金属铝 ③生石灰 ④烧碱 ⑤盐酸 ⑥纯碱 ⑦水 ⑧石墨.
A、属于纯净物的是②④⑤⑥⑦⑧ B、属于单质的是②⑧ C、属于碱的是④⑥ D、属于氧化物的是③④⑥⑦3. 某同学对所学部分化学知识归纳如下,完全正确的一组是( )A.化学与资源
B.化学与材料
①铁护栏表面刷上油漆,防止生锈
②爱护水资源只能通过节约用水实现
①用钛合金制作航天飞机的外壳,利用其密度大,耐腐蚀等性质
②装食品用的聚乙烯塑料袋具有热塑性
C.化学与环境
D.化学与生活
①减少空气污染的措施:风力发电、多用高含硫煤做燃料等
②防治“白色污染”的措施:回收废弃塑料、使用新型降解塑料等
①青少年食欲不振,生长迟缓,发育不良应多食海产品、瘦肉等含锌的食物
②二氧化碳灭火器灭火时有降温和隔绝空气的作用
A、A B、B C、C D、D4. 下列图示实验操作中,不正确的是( )A、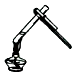 给试管里液体加热
B、
给试管里液体加热
B、 向试管中倾倒液体
C、
向试管中倾倒液体
C、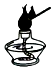 点燃酒精灯
D、
点燃酒精灯
D、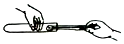 向试管中加入块状固体
5. 下列化学用语书写正确的是( )A、两个氢分子:2H B、2个硫酸根离子:2SO4﹣2 C、水中氧元素的化合价为﹣2 价: D、两个氮原子:N26. 婴幼儿患佝偻病,体内缺少的元素是( )A、铁 B、碘 C、氟 D、钙7. 下列有关溶液的说法中,错误的是( )A、外界条件不改变,溶质不会从溶液中分离出来 B、物质的溶解过程通常会伴随着能量的变化 C、溶液中的溶质以分子或离子的形式均匀分散在溶剂中保持静止不动,所以溶液具有均一性和稳定性 D、改变条件,能够使饱和溶液与不饱和溶液相互转化8. 如图是四种粒子的结构示意图,下列说法正确的是( )
向试管中加入块状固体
5. 下列化学用语书写正确的是( )A、两个氢分子:2H B、2个硫酸根离子:2SO4﹣2 C、水中氧元素的化合价为﹣2 价: D、两个氮原子:N26. 婴幼儿患佝偻病,体内缺少的元素是( )A、铁 B、碘 C、氟 D、钙7. 下列有关溶液的说法中,错误的是( )A、外界条件不改变,溶质不会从溶液中分离出来 B、物质的溶解过程通常会伴随着能量的变化 C、溶液中的溶质以分子或离子的形式均匀分散在溶剂中保持静止不动,所以溶液具有均一性和稳定性 D、改变条件,能够使饱和溶液与不饱和溶液相互转化8. 如图是四种粒子的结构示意图,下列说法正确的是( ) A、②③属于同种元素 B、②④的化学性质相同 C、②的符号为Al+3 D、①③形成的化合物是MgF29. 类比推理在化学学习和科学研究中有重要意义.下列类比推理正确的是( )A、NaOH和KOH都是强碱,两者都能与硫酸铜溶液反应生成蓝色沉淀 B、N2和O2都是非金属单质,两者的化学性质都非常活泼 C、盐酸和硫酸都是强酸,两者都易挥发 D、CaO和Fe2O3都是金属氧化物,两者都能与水反应生成碱10. 下列物质的用途,正确的是( )A、食盐可作发酵粉 B、石灰石可作建筑材料 C、碳酸氢钠可制玻璃 D、氢氧化钠可改良酸性土壤11. 下列对实验现象的描述中,正确的是( )A、向稀盐酸中滴加紫色石蕊试液,溶液显蓝色 B、将红热的细铁丝放在氧气中,剧烈燃烧,火星四射,生成白色固体 C、将羊毛线放在酒精灯火焰上灼烧,闻到烧焦羽毛的特殊气味 D、向氯化铁溶液中滴加氢氧化钠溶液,生成蓝色沉淀12. 每年的 4月15日是我国“全民国家安全教育日”. 下列做法错误的是( )A、高层楼房着火时,不能乘坐电梯逃离 B、在加油站张贴严禁烟火的标志 C、进入久未开启的地窖,要做灯火实验 D、家用电器着火时,立即用水扑灭13. 以下是某化学反应的微观示意图,有关该反应的说法正确的是( )
A、②③属于同种元素 B、②④的化学性质相同 C、②的符号为Al+3 D、①③形成的化合物是MgF29. 类比推理在化学学习和科学研究中有重要意义.下列类比推理正确的是( )A、NaOH和KOH都是强碱,两者都能与硫酸铜溶液反应生成蓝色沉淀 B、N2和O2都是非金属单质,两者的化学性质都非常活泼 C、盐酸和硫酸都是强酸,两者都易挥发 D、CaO和Fe2O3都是金属氧化物,两者都能与水反应生成碱10. 下列物质的用途,正确的是( )A、食盐可作发酵粉 B、石灰石可作建筑材料 C、碳酸氢钠可制玻璃 D、氢氧化钠可改良酸性土壤11. 下列对实验现象的描述中,正确的是( )A、向稀盐酸中滴加紫色石蕊试液,溶液显蓝色 B、将红热的细铁丝放在氧气中,剧烈燃烧,火星四射,生成白色固体 C、将羊毛线放在酒精灯火焰上灼烧,闻到烧焦羽毛的特殊气味 D、向氯化铁溶液中滴加氢氧化钠溶液,生成蓝色沉淀12. 每年的 4月15日是我国“全民国家安全教育日”. 下列做法错误的是( )A、高层楼房着火时,不能乘坐电梯逃离 B、在加油站张贴严禁烟火的标志 C、进入久未开启的地窖,要做灯火实验 D、家用电器着火时,立即用水扑灭13. 以下是某化学反应的微观示意图,有关该反应的说法正确的是( ) A、该反应中丙与丁的分子个数比为4:1 B、该反应属于化合反应 C、该反应前后原子的数目发生改变 D、该反应没有单质生成14. 阿司匹林的主要成分是乙酰水杨酸(化学式C9H8O4),是治疗心血管疾病的重要药物之一.下列关于乙酰水杨酸的说法错误的是( )A、一个乙酰水杨酸分子中原子总个数为21 B、乙酰水杨酸的相对分子质量为180 C、乙酰水杨酸属于有机物 D、乙酰水杨酸中氢元素与氧元素的质量比为2:115. 下列物质能在pH=1的无色溶液中大量共存的是( )A、KMnO4、CuCl2、Fe2(SO4)3、NaNO3 B、H2SO4、HCl、AgNO3、Na2SO4 C、NaNO3、NaCl、KNO3、(NH4)2SO4 D、K2SO4、NaCl、K2CO3、NaOH16. 除去下列各物质中的少量杂质,所选用的试剂、方法能达到目的是( )
A、该反应中丙与丁的分子个数比为4:1 B、该反应属于化合反应 C、该反应前后原子的数目发生改变 D、该反应没有单质生成14. 阿司匹林的主要成分是乙酰水杨酸(化学式C9H8O4),是治疗心血管疾病的重要药物之一.下列关于乙酰水杨酸的说法错误的是( )A、一个乙酰水杨酸分子中原子总个数为21 B、乙酰水杨酸的相对分子质量为180 C、乙酰水杨酸属于有机物 D、乙酰水杨酸中氢元素与氧元素的质量比为2:115. 下列物质能在pH=1的无色溶液中大量共存的是( )A、KMnO4、CuCl2、Fe2(SO4)3、NaNO3 B、H2SO4、HCl、AgNO3、Na2SO4 C、NaNO3、NaCl、KNO3、(NH4)2SO4 D、K2SO4、NaCl、K2CO3、NaOH16. 除去下列各物质中的少量杂质,所选用的试剂、方法能达到目的是( )选项
物质
杂质(少量)
试剂
操作方法
A
N2
O2
碳粉
将混合气体通过灼热的碳粉
B
NaOH溶液
Na2CO3溶液
氢氧化钙溶液
加入适量氢氧化钙溶液,过滤
C
氯化钠固体
泥沙
水
加水溶解,蒸发结晶
D
KCl溶液
K2SO4溶液
Ba(NO3)2 溶液
加入适量Ba(NO3)2溶液,过滤
A、A B、B C、C D、D17. 下图为甲、乙两种固体物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )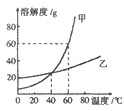 A、20℃时,甲物质的溶解度比乙物质的溶解度大 B、甲物质中混有少量乙物质,采用恒温蒸发溶剂的方法提纯甲物质 C、40℃时,甲、乙两种物质的饱和溶液中溶质质量相等 D、60℃时,甲物质的溶解度是60g,所以将80g甲物质放入100g 水中,所得溶液中溶质质量与溶剂质量之比是:60g:100g=3:518. 已知:Cu2O+H2SO4═Cu+CuSO4+H2O。16.0g CuO与CO反应得到Cu、Cu2O混合物13.6g,将此混合物溶于足量的100.0g稀H2SO4得9.6gCu.下列说法正确的是( )A、生成2.4g CO2 B、混合物中含9.6g铜元素 C、混合物中Cu与Cu2O的质量之比为8:9 D、反应后溶液中CuSO4的质量分数约为7.0%
A、20℃时,甲物质的溶解度比乙物质的溶解度大 B、甲物质中混有少量乙物质,采用恒温蒸发溶剂的方法提纯甲物质 C、40℃时,甲、乙两种物质的饱和溶液中溶质质量相等 D、60℃时,甲物质的溶解度是60g,所以将80g甲物质放入100g 水中,所得溶液中溶质质量与溶剂质量之比是:60g:100g=3:518. 已知:Cu2O+H2SO4═Cu+CuSO4+H2O。16.0g CuO与CO反应得到Cu、Cu2O混合物13.6g,将此混合物溶于足量的100.0g稀H2SO4得9.6gCu.下列说法正确的是( )A、生成2.4g CO2 B、混合物中含9.6g铜元素 C、混合物中Cu与Cu2O的质量之比为8:9 D、反应后溶液中CuSO4的质量分数约为7.0%二、填空题
-
19. 用化学用语填空:
(1)两个氢原子;
(2)氢氧根离子;
(3)氧化铝中铝元素的化合价 .20. 化学与我们的生活密切相关.(1)某地区学生营养午餐摄入标准值(每人每天)如表所示.
能量
3890kJ
蛋白质
48g
脂肪
30g
钙
480mg
锌
6mg
铁
4mg
维生素
24mg
①糖类和表中的蛋白质、能够为人体提供能量.
②下列食物中富含淀粉的是 .(填序号)
a.土豆 b.牛奶 c.豆油
③缺(填元素名称)可能导致骨骼疏松、畸形,易得佝偻病.
④人体不可缺少的营养物质有蛋白质、糖类、脂肪、矿物质、水和 .
(2)材料对我们生活的影响越来越大.
①下列属于无机材料的是 ,属于复合材料的是 .(填序号)
a.镁铝合金 b.聚乙烯 c.钢筋混凝土 d.有机玻璃
②下列方法不能防止钢铁腐蚀的是 .(填序号)
a.表面涂油 b.食盐水浸泡 c.表面镀铬.
21.右图是常见固体物质的溶解度曲线,根据图示回答:
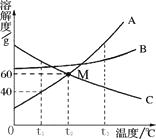
(1)曲线上M点表示 ,t3℃时,A、B、C三种物质的溶解度由大到小的顺序为 。
(2)t1℃时,将10g A物质放入100g水中,充分溶解后所得的溶液是 (填“饱和”或“不饱和”)溶液。欲使t2℃时C物质的饱和溶液变为不饱和溶液,可采取的方法是 (任填一种方法)。
(3)现有30℃的不饱和KNO3溶液,与该溶液有关的量有:
①水的质量 ②溶液中KNO3的质量 ③KNO3的质量分数 ④30℃时KNO3的溶解度 ⑤溶液的质量
Ⅰ.在该不饱和溶液中加硝酸钾至饱和,不变的量有 (填序号,下同)。
Ⅱ.将该不饱和溶液恒温蒸发至饱和,不变的量有。22. A~G是初中化学常见的物质,B和D能参与光合作用,F可用于改良酸性土壤. 它们之间的关系如图所示(“﹣”表示相连两物质之间能发生反应,“→”表示由某一物成转化为另一物质,部分反应物、生成物及反应条件已略去),每个虚线圈中各反应的基本反应类型相同.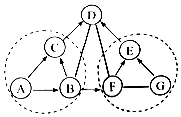 (1)、写出物质的化学式:A , G .(2)、反应F→E的基本反应类型是 .(3)、反应D﹣F的化学方程式是 .(4)、反应G→E的现象是 .23. 根据题意回答。
(1)、写出物质的化学式:A , G .(2)、反应F→E的基本反应类型是 .(3)、反应D﹣F的化学方程式是 .(4)、反应G→E的现象是 .23. 根据题意回答。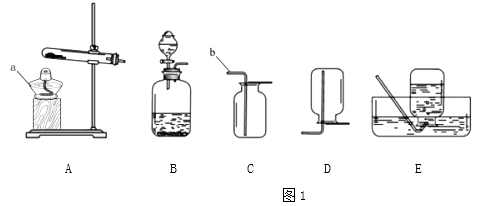
①写出仪器名称:a , b;
②实验室用氯酸钾和二氧化锰的混合物制取氧气,可选择的一组装置是(填编号)写出反应的化学方程式;
③下图是检查装置气密性的过程。最终在F处观察到的现象是(选填“甲~丁”);
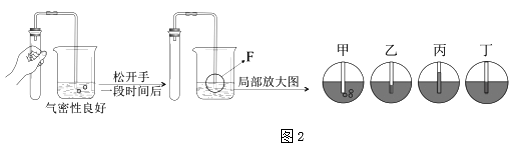
④ 资料表明:高铁酸钾(K2FeO4)固体也能用于制取氧气,原理如下:
方案一:4K2FeO4 2Fe2O3+4K2O+3O2↑
方案二:4K2FeO4+10H2O→4Fe(OH)3↓+8KOH+3O2↑
Ⅰ.关于以上方案说法错误的是
a.方案一是分解反应
b.方案二更节能简便
c.方案一、二均可在图1的装置B中进行实验
d.制取等质量的氧气,两种方案所需高铁酸钾的质量相等
Ⅱ.若用方案一(4K2FeO4 2Fe2O3+4K2O+3O2↑)制取0.3mol氧气,需要高铁酸钾的物质的量为 mol(根据化学方程式列式计算)。
24. 实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图),为确认其中的溶质,同学们进行了如下的探究活动.请你参与到其中去,回答有关问题.
【进行猜想】猜想Ⅰ:该溶液的溶质是NaCl;
猜想Ⅱ:该溶液的溶质是NaOH;
猜想Ⅲ:该溶液的溶质是Na2CO3;
猜想 IV:该溶液的溶质是NaHCO3 .
【查阅资料】常温下物质的相关信息如表:
物质
NaCl
NaOH
Na2CO3
NaHCO3
常温下的溶解度/g
36
109
21.5
9.6
常温下稀溶液的pH
7
13
11
9
(1)、从物质的相关信息可知,该溶液的溶质不是NaHCO3 , 因为常温下NaHCO3溶液溶质的质量分数最大是(精确到01.%).【进行实验】测定溶液的pH大于7,该溶液的溶质不是(填化学式).
(2)、同学们又进行了如下实验,实验过程如图: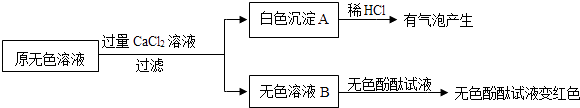
产生白色沉淀的化学方程式是 .
实验可以判断原无色溶液中含有的溶质有 .
【获得结论】
该瓶原来装的无色溶液的溶质是NaOH,并且 (填“没有”、“部分”或“全部”)变质.
【拓展】
提纯该无色溶液的步骤是:先向无色溶液中加入适量的 , 然后过滤.反应化学方程式是 .
三、计算题
-
25. 为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水,杂质中不含钙元素)。
有关实验数据如下表所示:
 (1)、反应中生成二氧化碳的质量为多少克?(2)、求该石灰石中碳酸钙的质量分数。
(1)、反应中生成二氧化碳的质量为多少克?(2)、求该石灰石中碳酸钙的质量分数。