山东省德州市宁津县2017-2018学年中考化学二模考试试卷
试卷更新日期:2018-05-25 类型:中考模拟
一、单选题
-
1. 下列描述物质的变化中,不属于化学变化的是( )A、
 B、
B、 C、
C、 D、
D、 2. 下列对于实验操作和实验现象描述错误的是( )A、红色的铜丝在酒精灯火焰上加热,变成黑色 B、盛有铁丝的试管中加入稀盐酸,溶液由无色变成浅绿色 C、CO在空气中点燃,发出蓝色火焰,放出热量 D、将细铁丝放入氧气中,火星四射,生成一种黑色固体3. 下列实验操作中,错误的是( )A、
2. 下列对于实验操作和实验现象描述错误的是( )A、红色的铜丝在酒精灯火焰上加热,变成黑色 B、盛有铁丝的试管中加入稀盐酸,溶液由无色变成浅绿色 C、CO在空气中点燃,发出蓝色火焰,放出热量 D、将细铁丝放入氧气中,火星四射,生成一种黑色固体3. 下列实验操作中,错误的是( )A、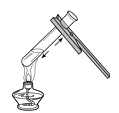 加热液体
B、
加热液体
B、 稀释浓硫酸
C、
稀释浓硫酸
C、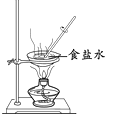 蒸发食盐水
D、
蒸发食盐水
D、 检查装置气密性
4. 下列现象或事实,用分子的相关知识加以解释,其中错误的是( )A、热胀冷缩 , 说明分子大小随温度改变而改变 B、酒香不怕巷子深,说明分子不断地运动 C、25L的石油气可以装入 0.024L的钢瓶中,说明分子之间有间隔 D、水通电后生成氢气和氧气 , 说明在化学变化中分子可以再分5. 徐闻盛产菠萝,每100克菠萝含钾126毫克,钠1.2毫克,锌0.08毫克,这里的钾、钠、锌是指( )A、单质 B、原子 C、元素 D、离子6. 硝化甘油(C3H5N3O9)可用于治疗心绞痛,因为它在人体内被缓慢氧化生成A气体,反应的化学方程式为:4C3H5N3O9+5O2=12A+12CO2+10H2O,则A的化学式是( )A、N2O B、NO C、NO2 D、N27. 荔枝是廉江市特产之一,肉肥汁多,清香鲜美,甜酸宜人,含有丰富的维生素C(化学式为C6H8O6),可强化免疫系统,促进伤口愈合和对铁质的吸收;它所富含的肌醇[化学式为(CHOH)6]及氨基酸,可抑制抑郁症,补充脑力所消耗的营养。下列有关说法正确的是 ( )A、肌醇由四种元素组成 B、维生素C相对分子质量为176g C、维生素C是由6个碳原子、8个氢原子和6个氧原子构成 D、维生素C完全燃烧生成二氧化碳和水8. 今年4月同学们参加了南通市实验技能考查,切身体会到规范操作的重要性。下列实验操作符合规范要求的是( )A、“配制一定溶质质量分数的溶液”实验中,多余的药品应放回原瓶 B、“粗盐的提纯”实验中,过滤时将悬浊液直接倒入漏斗里 C、“高锰酸钾制取氧气”实验中,收集好气体后应先将导管移出水槽再停止加热 D、“探究酸和碱的性质”实验中,测定溶液pH时应先将试纸湿润9. 化学知识与我们的生活密切相关。以下说法错误的是( )A、厨房煤气泄漏时,应立即打开排气扇 B、蚊子叮咬时会释放出蚁酸而导致皮肤肿痛,可涂上小苏打溶液 C、用稀盐酸可鉴别真黄金和“假黄金(铜锌合金)” D、羊毛衣服和腈纶衣服可用燃烧的方法区别10. 逻辑推理是化学学习常用的思维方法。下列推理正确的是( )A、酸性溶液的pH都小于7,所以酸溶液pH一定小于7 B、有机物都含碳元素,所以含碳元素的化合物都是有机物 C、水是纯净物,所以海水也是纯净物 D、中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应11. 将a、b、c三种金属分别投入稀盐酸中,只有b溶解并产生气泡;把a和c分别放入硫酸铜溶液中,在a表面有铜析出,c没有变化。则a、b、c的金属活动性顺序是( )A、c>b>a B、b>a>c C、a>c>b D、b>c>a12. 向一定量的锌粉中滴加稀盐酸至过量,下图表示反应过程中某种物质的质量m随加入盐酸质量的变化关系,则m不可能表示( )
检查装置气密性
4. 下列现象或事实,用分子的相关知识加以解释,其中错误的是( )A、热胀冷缩 , 说明分子大小随温度改变而改变 B、酒香不怕巷子深,说明分子不断地运动 C、25L的石油气可以装入 0.024L的钢瓶中,说明分子之间有间隔 D、水通电后生成氢气和氧气 , 说明在化学变化中分子可以再分5. 徐闻盛产菠萝,每100克菠萝含钾126毫克,钠1.2毫克,锌0.08毫克,这里的钾、钠、锌是指( )A、单质 B、原子 C、元素 D、离子6. 硝化甘油(C3H5N3O9)可用于治疗心绞痛,因为它在人体内被缓慢氧化生成A气体,反应的化学方程式为:4C3H5N3O9+5O2=12A+12CO2+10H2O,则A的化学式是( )A、N2O B、NO C、NO2 D、N27. 荔枝是廉江市特产之一,肉肥汁多,清香鲜美,甜酸宜人,含有丰富的维生素C(化学式为C6H8O6),可强化免疫系统,促进伤口愈合和对铁质的吸收;它所富含的肌醇[化学式为(CHOH)6]及氨基酸,可抑制抑郁症,补充脑力所消耗的营养。下列有关说法正确的是 ( )A、肌醇由四种元素组成 B、维生素C相对分子质量为176g C、维生素C是由6个碳原子、8个氢原子和6个氧原子构成 D、维生素C完全燃烧生成二氧化碳和水8. 今年4月同学们参加了南通市实验技能考查,切身体会到规范操作的重要性。下列实验操作符合规范要求的是( )A、“配制一定溶质质量分数的溶液”实验中,多余的药品应放回原瓶 B、“粗盐的提纯”实验中,过滤时将悬浊液直接倒入漏斗里 C、“高锰酸钾制取氧气”实验中,收集好气体后应先将导管移出水槽再停止加热 D、“探究酸和碱的性质”实验中,测定溶液pH时应先将试纸湿润9. 化学知识与我们的生活密切相关。以下说法错误的是( )A、厨房煤气泄漏时,应立即打开排气扇 B、蚊子叮咬时会释放出蚁酸而导致皮肤肿痛,可涂上小苏打溶液 C、用稀盐酸可鉴别真黄金和“假黄金(铜锌合金)” D、羊毛衣服和腈纶衣服可用燃烧的方法区别10. 逻辑推理是化学学习常用的思维方法。下列推理正确的是( )A、酸性溶液的pH都小于7,所以酸溶液pH一定小于7 B、有机物都含碳元素,所以含碳元素的化合物都是有机物 C、水是纯净物,所以海水也是纯净物 D、中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应11. 将a、b、c三种金属分别投入稀盐酸中,只有b溶解并产生气泡;把a和c分别放入硫酸铜溶液中,在a表面有铜析出,c没有变化。则a、b、c的金属活动性顺序是( )A、c>b>a B、b>a>c C、a>c>b D、b>c>a12. 向一定量的锌粉中滴加稀盐酸至过量,下图表示反应过程中某种物质的质量m随加入盐酸质量的变化关系,则m不可能表示( ) A、溶液总质量 B、消耗锌粉的质量 C、生成ZnCl2的质量 D、生成H2的质量13. 下图是某个化学反应的微观模拟示意图,其中不同的球代表不同元素的原子。从图中获得的有关信息正确的是( )
A、溶液总质量 B、消耗锌粉的质量 C、生成ZnCl2的质量 D、生成H2的质量13. 下图是某个化学反应的微观模拟示意图,其中不同的球代表不同元素的原子。从图中获得的有关信息正确的是( ) A、该反应属于置换反应 B、参加反应的两种分子个数比为1∶1 C、1个X分子中含有3个原子 D、1个X分子中含有3种不同的原子14. 以下表示的是碳及其化合物的相互转化关系:( )
A、该反应属于置换反应 B、参加反应的两种分子个数比为1∶1 C、1个X分子中含有3个原子 D、1个X分子中含有3种不同的原子14. 以下表示的是碳及其化合物的相互转化关系:( )其中涉及的基本反应类型依次为( )
A、化合、置换、分解、复分解 B、置换、复分解、化合、分解 C、置换、化合、分解、复分解 D、置换、化合、复分解、分解15. 下图为A、B、C三种物质的溶解度曲线,请据图判断下列叙述中正确的是( ) A、t1℃时,B物质的溶解度为40 B、t1℃时,三种物质的溶解度由大到小的顺序为:A﹥B﹥C C、要使A从其热饱和溶液中析出,最好采用冷却溶液法 D、要将C的不饱和溶液转化为饱和溶液可以采取降温的方法16. 下列4个图像能符合题意反映对应变化关系是( )
A、t1℃时,B物质的溶解度为40 B、t1℃时,三种物质的溶解度由大到小的顺序为:A﹥B﹥C C、要使A从其热饱和溶液中析出,最好采用冷却溶液法 D、要将C的不饱和溶液转化为饱和溶液可以采取降温的方法16. 下列4个图像能符合题意反映对应变化关系是( )A
B
C
D




向一定量铁粉中滴加稀盐酸液
用酒精灯加热一定量KMnO4固体
向一定量澄清石灰水中加入Na2CO3溶液
向盛有MnO2的烧杯中加入H2O2溶液
A、A B、B C、C D、D二、填空题
-
17. 生活中处处有化学,请根据你所学的化学知识填空:(1)、小明的妈妈为小明准备了一份午餐:大米饭、红烧鲤鱼、溜豆腐、鸡蛋汤.请根据学过的知识回答下列问题.
①从营养均衡的角度考虑,他还应该增加的食物是(写一种即可).
②在中午做汤时加入加铁酱油,其中的“铁”是指(填“原子”、“分子”、“元素”或“物质”).
③饭后用洗洁精去餐具上的油污,是因为洗洁精具有功能.
(2)、从C、H、O、S、Na五种元素中,选择适当元素组成符合下列要求的化学用语。①发酵粉的主要成分之一是 。
②“西气东输”的气体主要成分是。
③能形成酸雨的主要气体是。
④一个中和反应的化学方程式:。
18. 2017年5月18日,我国首次海域“可燃冰”试采成功。中共中央、国务院发出贺电,中国人民又一次攀登上了世界科技的新高峰。“可燃冰”是天然气水合物,外观像冰一样,遇火即可燃烧。(1)、开采海域“可燃冰”,要用金刚石做成的钻头钻凿海底坚硬的岩层,这是利用了金刚石的物理性质。(2)、燃烧必须满足一定的条件才能发生,“可燃冰”为燃烧提供了。(3)、开采海域“可燃冰”的钻井平台“蓝鲸一号”使用了大量的金属材料。下列措施中哪一项不能有效防止金属锈蚀? (填序号)a.在金属表面涂油或剧漆
b.制成耐腐蚀的合金
c.打磨掉铝制品表面的氧化膜
(4)、天然气也是重要的化工原料。甲烷(CH4)与二氧化碳在一定条件下反应生成两种可燃性气体(其中一种是单质),请写出该反应的化学方程式。19. 如图1是小明在20℃时进行的系列实验示意图,①-⑤表示实验所得溶液;图2是NaCl、KNO3的溶解度曲线. (1)、20℃时,KNO3的溶解度(S)=;⑤是 (填“饱和”或“不饱和”)溶液.(2)、50℃时,饱和NaCl溶液中溶质的质量分数(w1)与饱和KNO3溶液中溶质的质量分数(w2)的大小关系是:w1w2(填“>”“=”或“<”).(3)、小明发现:升温至50℃,②→③的过程中有少量水蒸发,下列叙述正确的是(填序号)
(1)、20℃时,KNO3的溶解度(S)=;⑤是 (填“饱和”或“不饱和”)溶液.(2)、50℃时,饱和NaCl溶液中溶质的质量分数(w1)与饱和KNO3溶液中溶质的质量分数(w2)的大小关系是:w1w2(填“>”“=”或“<”).(3)、小明发现:升温至50℃,②→③的过程中有少量水蒸发,下列叙述正确的是(填序号)a.①、②均为不饱和溶液
b.②→③的过程中溶质质量分数变大
c.④→⑤的过程中析出KNO3晶体53.9g
(4)、除去KNO3固体中混有的少量NaCl的实验操作为:加适量水溶解→加热得到热饱和溶液→→过滤→洗涤→干燥→KNO3 .20. 为了探究化学反应前后物质的总质量是否发生改变, 甲同学和乙同学分别设计了下面两个实验, 请根据图示回答问题: (1)、甲同学设计的实验如图 A 所示,反应前,托盘天平的指针指向刻度盘的中间;两种物质反应后, 托盘天平的指针(选填“向左”、“向右”或“不”)偏转, 原因是。(2)、乙同学设计的实验如图B所示,通过实验得出结论:化学反应前后物质的总质量。(3)、两位同学通过交流反思得到启示: 在探究化学反应前后物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在装置中进行。(4)、从微观角度分析, 在化学反应前后一定不变的是(选填序号)。
(1)、甲同学设计的实验如图 A 所示,反应前,托盘天平的指针指向刻度盘的中间;两种物质反应后, 托盘天平的指针(选填“向左”、“向右”或“不”)偏转, 原因是。(2)、乙同学设计的实验如图B所示,通过实验得出结论:化学反应前后物质的总质量。(3)、两位同学通过交流反思得到启示: 在探究化学反应前后物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在装置中进行。(4)、从微观角度分析, 在化学反应前后一定不变的是(选填序号)。①原子种类 ②分子种类 ③原子数目 ④分子质量 ⑤分子数目 ⑥原子质量
21. 可用带柄V形玻璃管完成以下实验: (1)、如图1所示,往A处注入H2O2溶液,在B处下方加热使硫粉燃烧,产生的气体通入C处后排放的目的是。写出A处和C处反应的化学方程式: , 。
(1)、如图1所示,往A处注入H2O2溶液,在B处下方加热使硫粉燃烧,产生的气体通入C处后排放的目的是。写出A处和C处反应的化学方程式: , 。图1中用V型管代替集气瓶的优点是。
(2)、如图2所示,A处盛浓氨水,B处放滴有无色酚酞试液的长滤纸条,可观察到的现象是。若另取一相同V形玻璃管(含相同的实验用品),在A处稍加热,在更短的时间内可观察到上述现象,请从微观角度解释:。三、实验题
-
22. 酸碱盐是有广泛用途的重要化合物,某活动小组的同学围绕这几类化合物进行了一系探究活动.(1)、同学们打开浓盐酸、浓硫酸的瓶盖,立即就能把它们区别开来,这是为什么?。(2)、某地化学实验操作考试中。小刚同学选择了稀盐酸、氢氧化钠溶液、酚酞溶液三种试剂,按如图所示进行酸碱中和反应的实验。请回答:

①试剂I是 ,试剂Ⅱ是。
②本实验中,常常选用酚酞溶液而不选用石蕊溶液做指示剂的原因是。
③欲验证上述实验中稀盐酸和氢氧化钠溶液是否恰好完全反应,不能选择的试剂是
A.石蕊溶液
B.铜片
C.碳酸氢钠粉末
四、科学探究题
-
23. 实验中学的化学兴趣小组同学在探究碱的化学性质时,做了如下实验:
小亮、舟舟和月月分别向澄清石灰水中通入CO2气体,滴加氯化镁溶液和稀盐酸
(1)、小亮实验观察的实验现象是 , 发生反应的化学方程式是。(2)、舟舟实验发生反应的化学方程式为 。(3)、【提出问题】月月实验中没有观察到明显现象,那么盐酸与氢氧化钙是否发生了化学反应?
【进行实验】小亮取月月实验后的废液少量,向其中滴加几滴无色酚酞溶液,观察到无色酚酞溶液变红色,于是小亮得出盐酸与氢氧化钙没有发生反应。
你是否同意小亮得出的结论,并说明理由:。
(4)、舟舟另取月月实验后的废液少量,向其中加入MgCl2溶液,若观察到 现象,于是得出盐酸与氢氧化钙发生了反应。(5)、【归纳总结】通过上述实验我们能够总结出:在判断反应发生时,除了看是否有新物质生成外,还可通过判断来证明发生了化学反应。五、综合题
-
24. 实验室中要配制70g20%的NaCl溶液(图中为部分仪器),请回答下列问题:
 (1)、图中缺少一种必须用到的玻璃仪器是(2)、量取水时,仰视刻度,会使配制溶液的溶质质量分数 (填“偏大”或“偏小”)(3)、将配制好的70g20%NaCl溶液,稀释成10%的溶液,需要加水克
(1)、图中缺少一种必须用到的玻璃仪器是(2)、量取水时,仰视刻度,会使配制溶液的溶质质量分数 (填“偏大”或“偏小”)(3)、将配制好的70g20%NaCl溶液,稀释成10%的溶液,需要加水克六、计算题
-
25. 实验室有一瓶标签残缺的硫酸铜溶液,为了测定此溶液的溶质质量分数,某同学取出50g该溶液.向其中逐滴加入溶质质量分数为10%的氢氧化钠溶液,加入NaOH溶液的质量与生成沉淀的质量之间的关系如图所示,请计算该硫酸铜溶液的溶质质量分数。(反应的化学方程式是:2NaOH+CuSO4=Na2SO4+Cu(OH)2↓)

-
-
-