2018年广东省深圳市中考化学冲刺试卷(二)
试卷更新日期:2018-05-23 类型:中考模拟
一、选择题
-
1. 下列化学用语关于数字“3”的意义,说法正确的是( )
①3Hg②Fe3+③SO3④3H2O.
A、表示分子个数的是③ B、表示离子所带电荷数的是② C、表示原子个数的是④ D、表示一个分子中含有某种原子个数的是①2. 化学对人类生活和社会发展做出了巨大贡献.下列对某一主题知识归纳都正确的一组是( )A.生活常识
B.物质鉴别
洗涤剂洗油污﹣﹣乳化作用
人体缺锌元素﹣﹣甲状腺肿大
食盐与亚硝酸钠﹣﹣品尝
羊毛绒与棉线﹣﹣灼烧
C.安全常识
D.环境保护
油锅不慎着火﹣﹣可以盖上锅盖灭火
火灾烟很大时﹣﹣用湿毛巾捂住口鼻
减少白色污染﹣﹣少使用塑料制品
减少酸雨污染﹣﹣不使用化石燃料
A、A B、B C、C D、D3. 下列实验基本操作中正确的是( )A、加热液体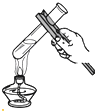 B、称量氢氧化钠固体
B、称量氢氧化钠固体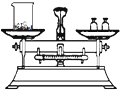 C、蒸发食盐水
C、蒸发食盐水  D、盐酸和NaOH验证中和反应
D、盐酸和NaOH验证中和反应 4. 豆腐是人们喜爱的食物,营养丰富,能为人体提供所需的多种氨基酸,其中含量最多的是亮氨酸(C6H13NO2 ),关于亮氨酸的说法正确的是( )A、亮氨酸是氧化物 B、亮氨酸中碳、氢、氮、氧四种元素的质量比为72:13:14:32 C、一个亮氨酸分子由21个原子构成 D、亮氨酸中碳元素的质量分数为27.5%5. 甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )
4. 豆腐是人们喜爱的食物,营养丰富,能为人体提供所需的多种氨基酸,其中含量最多的是亮氨酸(C6H13NO2 ),关于亮氨酸的说法正确的是( )A、亮氨酸是氧化物 B、亮氨酸中碳、氢、氮、氧四种元素的质量比为72:13:14:32 C、一个亮氨酸分子由21个原子构成 D、亮氨酸中碳元素的质量分数为27.5%5. 甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )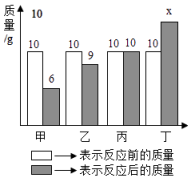 A、x的值是15 B、丙可能是该反应的催化剂 C、该反应是分解反应 D、反应中甲和乙的质量比为4:16.
A、x的值是15 B、丙可能是该反应的催化剂 C、该反应是分解反应 D、反应中甲和乙的质量比为4:16.如图是硝酸钾的溶解度曲线,下列说法错误的是( )
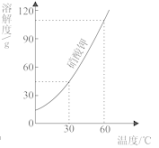 A、硝酸钾的溶解度随温度的升高而增大 B、降低温度可以使接近饱和的硝酸钾溶液变饱和 C、60℃时120g硝酸钾与100g水充分混合可以形成饱和溶液 D、60℃时硝酸钾溶液的溶质质量分数一定大于30℃时硝酸钾溶液的溶质质量分数7. 如图是宇宙飞船发动机内氢气和氧气燃烧生成水的微观过程,结合上述反应,下列说法正确的是( )
A、硝酸钾的溶解度随温度的升高而增大 B、降低温度可以使接近饱和的硝酸钾溶液变饱和 C、60℃时120g硝酸钾与100g水充分混合可以形成饱和溶液 D、60℃时硝酸钾溶液的溶质质量分数一定大于30℃时硝酸钾溶液的溶质质量分数7. 如图是宇宙飞船发动机内氢气和氧气燃烧生成水的微观过程,结合上述反应,下列说法正确的是( )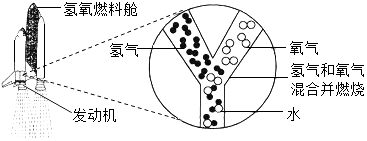 A、保持水化学性质的粒子是氢原子和氧原子 B、通过上述反应可知,氧气具有可燃性 C、该反应属于化合反应 D、该反应前后,原子种类发生了改变8. 25℃时,向20.0mL质量分数为30%的盐酸中滴加氢氧化钠溶液,溶液的pH与所加氢氧化钠溶液的体积如图所示,下列有关叙述正确的是( )
A、保持水化学性质的粒子是氢原子和氧原子 B、通过上述反应可知,氧气具有可燃性 C、该反应属于化合反应 D、该反应前后,原子种类发生了改变8. 25℃时,向20.0mL质量分数为30%的盐酸中滴加氢氧化钠溶液,溶液的pH与所加氢氧化钠溶液的体积如图所示,下列有关叙述正确的是( ) A、b、d点对应溶液的pH:b>d B、所用氢氧化钠溶液的质量分数一定为30% C、向b点对应的溶液中滴加石蕊溶液,溶液呈无色 D、d点对应的溶液中溶质是NaCl和NaOH9. 为达到实验目的,下列实验方案或结论不正确的是( )
A、b、d点对应溶液的pH:b>d B、所用氢氧化钠溶液的质量分数一定为30% C、向b点对应的溶液中滴加石蕊溶液,溶液呈无色 D、d点对应的溶液中溶质是NaCl和NaOH9. 为达到实验目的,下列实验方案或结论不正确的是( )选项
实验目的
实验方案或结论
A
除去铜粉中含有的少量铁粉
将混合固体加入到足量稀盐酸中,充分反应后过滤、洗涤、干燥
B
鉴别①CuSO4溶液②稀H2SO4③NaCl溶液④NaOH溶液
不用其它任何试剂就能鉴别,且鉴别的顺序为①④②③或①④③②
C
除去CO2中的少量HCl气体
先通过NaOH溶液,再通过浓硫酸
D
CaCl2固体中除去CaCO3杂质
加水溶解、过滤、增发结晶
A、A B、B C、C D、D10. 向一定质量AgNO3和Cu(NO3)2的混合溶液中加入锌粉,溶液质量与加入锌粉的质量关系如图所示.下列说法中,错误的是( )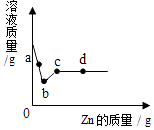 A、a点溶液对应的固体中只有一种物质 B、若取b~C段固体,滴加稀盐酸,无气泡产生 C、b点溶液呈蓝色 D、d点溶液对应的固体中只有两种物质
A、a点溶液对应的固体中只有一种物质 B、若取b~C段固体,滴加稀盐酸,无气泡产生 C、b点溶液呈蓝色 D、d点溶液对应的固体中只有两种物质二、非选择题
-
11.
甲、乙、A、B、C、D是初中化学常见物质,其中A、B、C、D是由H、C、O、Ca、Na元素中的两种或三种组成.
(1)甲是胃酸的主要成分,与活泼金属反应生成一种在标准状况下密度最小的气体,该气体化学式为
(2)乙是一种红色的氧化物,能溶于稀盐酸,得到黄色溶液,则乙的化学式为
(3)A俗称为纯碱;B、C、D三种物质中含同种金属元素,并存在下列转化关系B→C→D.A与C反应的化学方程式为
(4)实验小组同学将A、B、C、D中的一种或几种物质混合在一起得到一包白色固体粉末,为确定其组成,进行了如下图所示的实验.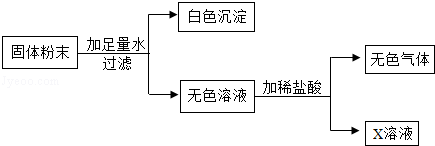
请回答:
①若X溶液只含一种溶质,根据实验可以确定X溶液中的溶质是;
②下列对固体粉末成分的判断中,不正确的是(填字母序号).
A.一定有碳酸钠
B.一定有碳酸钙
C.可能是氧化钙、氢氧化钙、碳酸钙的混合物
D.该固体粉末的组成最多有三种情况.12. 浴室喷头长时间使用会有白色固体附着,俗称水垢。这是因为硬水中含有较多的可溶性的碳酸氢钙【Ca(HCO3)2】,还含有可溶性的碳酸氢镁【Mg(HCO3)2】。查阅资料,加热时会产生难溶性的固体。其中碳酸氢钙【Ca(HCO3)2】受热易分解,生成难溶性的化合物、气体等物质。某小组想探究碳酸氢钙受热分解后产物的成分。(1)、【提出猜想】猜想1.难溶性化合物可能是CaCO3;猜想2.气体可能是H2、CO、CO2 。【方案设计】请你设计实验,帮助该组同学确定难溶物的成分。
实验步骤
实验现象
结论
难溶物是CaCO3
(2)、【实验探究】该组同学设计如图实验,继续探究气体的成分。
操作1.加热A装置,一段时间后,B装置中的澄清石灰水变浑浊。
操作2.在a处用燃着的木条检验,无明显现象。
【实验结论】结论1.碳酸氢钙分解产生的气体是;
结论2.碳酸氢钙受热分解的化学方程式为。
(3)、【反思评价】有同学提出:硬水中可溶性的碳酸氢镁【Mg(HCO3)2】受热也会产生不溶性的固体,那水垢的成分中还有什么物质?根据上述探究,该组同学设计如下图装置进一步实验。(已知碱石灰主要成分为CaO和NaOH)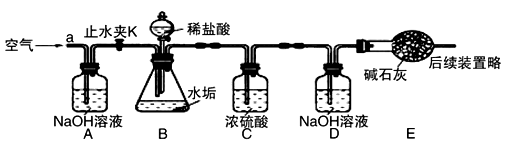
【实验测定】 步骤如下:
①按图组装仪器,先 , 再将50g水垢样品放入锥形瓶中。
②打开止水夹K,从导管a处缓缓鼓入一定量的空气。
③逐滴加入足量稀盐酸,待锥形瓶中出现气泡不再产生现象时,停止滴加稀盐酸。
④打开止水夹K,从导管a处缓缓鼓入一定量的空气;
⑤称量D瓶内物质增加的质量,直至D瓶内物质质量不变;
⑥测量滴加稀盐酸体积与D瓶内物质增加质量的关系如下图曲线所示。
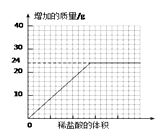 (4)、【讨论交流】
(4)、【讨论交流】①A装置中的NaOH溶液的作用是 , 若没有A装置,D装置中的质量将(填“偏大”、“不变”或“偏小”)。
②C装置中浓硫酸的作用是 , E装置的作用是。
③分析曲线图,通过计算可知:水垢中一定含有(化学式) , 理由是。
④查阅资料:水垢的主要成分有CaCO3、MgCO3和Mg(OH)2三种成分,三种物质加热后均能生成两种氧化物。小组同学提出探究水垢中氢氧化镁的质量分数:另取质量为50g的水垢试样,放入试管中加热至质量不再减少为止,测得二氧化碳24 g,残留固体25.1g。结合以上数据,确定水垢样品中氢氧化镁的质量分数为。(结果保留小数点后一位)
13. 用“侯氏联合制碱法”制得的纯碱中常含有少量的氯化钠.为测定某纯碱样品中碳酸钠的质量分数,小明称取该纯碱样品12g,完全溶解于100g水中,再滴加一定溶质质量分数的氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示: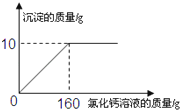
求:
①该纯碱样品中碳酸钠的质量分数(计算结果精确到0.1%);
②反应后所得溶液中溶质的质量分数.