广东省汕头市龙湖区2017-2018学年九年级化学中考模拟试卷
试卷更新日期:2018-05-18 类型:中考模拟
一、单选题
-
1. 中华民族的发明创造为人类文明进步做出了巨大贡献。下列没有涉及化学变化的是( )A、侯氏制碱
 B、蚕丝纺织
B、蚕丝纺织  C、火药应用
C、火药应用  D、粮食酿酒
D、粮食酿酒  2. 空气中含量最多的气体是( )A、O2 B、N2 C、He D、CO23. 下列做法符合“美丽汕头,清洁城乡”活动主题的是( )A、生活垃圾分类处理 B、在田野直接焚烧秸杆 C、工业废水直接排放下水道 D、在空旷地方焚烧废旧塑料袋4. 如图文化衫:你的“魅力”偷走我的“心”。该反应能发生是由于镁单质( )
2. 空气中含量最多的气体是( )A、O2 B、N2 C、He D、CO23. 下列做法符合“美丽汕头,清洁城乡”活动主题的是( )A、生活垃圾分类处理 B、在田野直接焚烧秸杆 C、工业废水直接排放下水道 D、在空旷地方焚烧废旧塑料袋4. 如图文化衫:你的“魅力”偷走我的“心”。该反应能发生是由于镁单质( ) A、金属光泽美丽 B、导电性优良 C、金属活动性强 D、延展性好5. 不需要补充其它仪器,就能改正如图实验中错误操作的是( )A、
A、金属光泽美丽 B、导电性优良 C、金属活动性强 D、延展性好5. 不需要补充其它仪器,就能改正如图实验中错误操作的是( )A、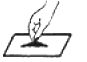 取用固体药品
B、
取用固体药品
B、 浓硫酸稀释
C、
浓硫酸稀释
C、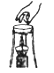 移走蒸发皿
D、
移走蒸发皿
D、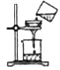 过滤
6. 下列有关化学用语表示错误的是( )A、2个铝离子:2Al3+ B、钠原子的结构示意图:
过滤
6. 下列有关化学用语表示错误的是( )A、2个铝离子:2Al3+ B、钠原子的结构示意图: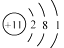 C、氧分子:O
D、氧化镁中镁元素显+2价:
C、氧分子:O
D、氧化镁中镁元素显+2价: 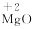 7. 甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是( )
7. 甲、乙两种物质的溶解度曲线如图所示。下列说法正确的是( )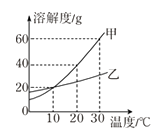 A、依据溶解度曲线可判断,甲的溶解度比乙大 B、10℃时,甲、乙饱和溶液溶质的质量相同 C、20℃时,把30g甲放入50g水中形成的溶液中溶质质量分数为37.5% D、将20℃时的甲、乙饱和溶液升温至30℃,甲、乙溶液中溶质的质量分数均不变8. 欲将粗盐提纯并用所得精盐配制一定溶质质量分数的氯化钠溶液,说法正确的是( )A、过滤时,用玻璃棒搅拌加快过滤速度 B、蒸发时,待蒸发皿中晶体全部析出后停止加热 C、配制溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等 D、配制溶液需要经过计算、称量、溶解、装瓶存放等步骤9. 科学贵在创新,以下是对部分化学实验的改进,其中不能达到目的的是 ( )
A、依据溶解度曲线可判断,甲的溶解度比乙大 B、10℃时,甲、乙饱和溶液溶质的质量相同 C、20℃时,把30g甲放入50g水中形成的溶液中溶质质量分数为37.5% D、将20℃时的甲、乙饱和溶液升温至30℃,甲、乙溶液中溶质的质量分数均不变8. 欲将粗盐提纯并用所得精盐配制一定溶质质量分数的氯化钠溶液,说法正确的是( )A、过滤时,用玻璃棒搅拌加快过滤速度 B、蒸发时,待蒸发皿中晶体全部析出后停止加热 C、配制溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等 D、配制溶液需要经过计算、称量、溶解、装瓶存放等步骤9. 科学贵在创新,以下是对部分化学实验的改进,其中不能达到目的的是 ( )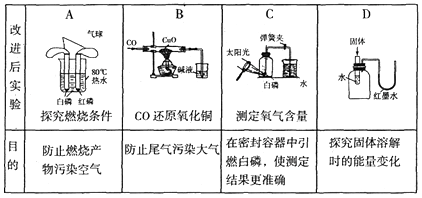 A、A B、B C、C D、D10. 清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如图(图中的微粒恰好完全反应)。下列说法正确的是( )
A、A B、B C、C D、D10. 清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如图(图中的微粒恰好完全反应)。下列说法正确的是( )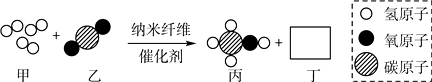 A、丁的化学式为H2O,该反应为置换反应 B、参加反应的甲与乙的质量比为3∶1 C、甲是单质,乙、丙、丁均为氧化物 D、该反应体现了无机物可以转化为有机物11. 下列四组溶液,只提供无色酚酞试液,不能鉴别的是:( )A、NaOH Ca(OH)2 HCl Na2CO3 B、HCl H2SO4 Na2CO3 KNO3 C、Na2CO3 Na2SO4 H2SO4 NaOH D、Na2SO4 Ba(OH)2 H2SO4 HCl12. 除去下列各物质中的少量杂质,所选用的试剂、方法均正确的是( )
A、丁的化学式为H2O,该反应为置换反应 B、参加反应的甲与乙的质量比为3∶1 C、甲是单质,乙、丙、丁均为氧化物 D、该反应体现了无机物可以转化为有机物11. 下列四组溶液,只提供无色酚酞试液,不能鉴别的是:( )A、NaOH Ca(OH)2 HCl Na2CO3 B、HCl H2SO4 Na2CO3 KNO3 C、Na2CO3 Na2SO4 H2SO4 NaOH D、Na2SO4 Ba(OH)2 H2SO4 HCl12. 除去下列各物质中的少量杂质,所选用的试剂、方法均正确的是( )物 质
杂质(少量)
加入试剂及用量
除杂操作方法
A
KCl溶液
CaCl2
适量的Na2CO3溶液
过滤、除去滤渣
B
NaCl
Na2CO3
过量的盐酸
加热蒸发
C
Cu(NO3)2
AgNO3
足量铜粉
过滤将滤渣烘干
D
N2
O2
足量的碳粉
加热
A、A B、B C、C D、D13. 甲、乙、丙三种物质的转化关系如右图所示(“→”表示反应一步实现,部分物质和反应条件已略去)。下列选项不能实现图示转化的是( )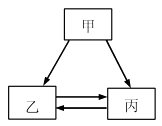
选项
甲
乙
丙
A
H2SO4
H2
H2O
B
C
CO
CO2
C
Ca(OH)2
CaCl2
CaCO3
D
NaOH
NaCl
NaNO3
A、A B、B C、C D、D二、填空题
-
14. 小明利用12种元素制作了一张如图所示的“元素钟面”。
 (1)、钟面上的这些元素之间最根本的区别是不同。(2)、小明根据钟面上提供的元素,写出了下列三种物质的化学式:O2、H2O和NaNO3 , 其中属于氧化物的是。(3)、此刻钟面上的时针、分针和秒针分别指向三种不同元素,请写出由这三种元素组成的化合物。(用化学式表示)15. 能源、材料、环保、食品等问题越来越引起人们的重视。请从化学的视角分析下列有关问题并填写空格:(1)、化石燃料包括煤、石油和。(2)、铝合金可用于制造飞机的外壳,铝合金属于(填“合成材料”“金属材料”或“复合材料”)。(3)、塑料在为我们的生活创造便利的同时,也对环境造成不利影响。人们把塑料给环境带来的危害称为“”。(4)、为了合理膳食,营养均衡,生活中把榨好的蔬菜汁放到面粉中,做成口味独特、营养丰富的蔬菜馒头,这种馒头提供的主要营养物质是和。(5)、化肥对提高农作物产量具有重要作用。尿素[CO(NH2)2]属于(填“氮肥”“钾肥”或“磷肥”)。16. 学校化学实验室新购买的药品有白磷、汞、乙醇、硝酸、氢氧化钠等(1)、从物质分类的角度看:属于金属单质的是(写化学式);(2)、从物质存放的角度看:①白磷保存在盛有的广口瓶中;
(1)、钟面上的这些元素之间最根本的区别是不同。(2)、小明根据钟面上提供的元素,写出了下列三种物质的化学式:O2、H2O和NaNO3 , 其中属于氧化物的是。(3)、此刻钟面上的时针、分针和秒针分别指向三种不同元素,请写出由这三种元素组成的化合物。(用化学式表示)15. 能源、材料、环保、食品等问题越来越引起人们的重视。请从化学的视角分析下列有关问题并填写空格:(1)、化石燃料包括煤、石油和。(2)、铝合金可用于制造飞机的外壳,铝合金属于(填“合成材料”“金属材料”或“复合材料”)。(3)、塑料在为我们的生活创造便利的同时,也对环境造成不利影响。人们把塑料给环境带来的危害称为“”。(4)、为了合理膳食,营养均衡,生活中把榨好的蔬菜汁放到面粉中,做成口味独特、营养丰富的蔬菜馒头,这种馒头提供的主要营养物质是和。(5)、化肥对提高农作物产量具有重要作用。尿素[CO(NH2)2]属于(填“氮肥”“钾肥”或“磷肥”)。16. 学校化学实验室新购买的药品有白磷、汞、乙醇、硝酸、氢氧化钠等(1)、从物质分类的角度看:属于金属单质的是(写化学式);(2)、从物质存放的角度看:①白磷保存在盛有的广口瓶中;②硝酸保存在棕色细口瓶中,原因是见光易分解.硝酸见光分解的化学方程式: 4HNO3 4X+O2↑+2H2O,其中X的化学式为;
③氢氧化钠要密封保存,因为敞口瓶放置易潮解和变质。用化学方程式表示变质的原因
17. 神舟十一号与天宫二号的成功对接增强了国人的民族自信,推动了相关领域的研究。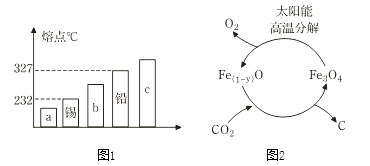 (1)、合金材料的研发
(1)、合金材料的研发①合金的很多性能与组成它们的纯金属不同,图1能表示锡铅合金的是(填序号“a”“b”或“c”).
②镁合金被誉为“21世纪绿色金属结构材料”.Mg17Al12是一种特殊的镁合金,通常选择真空熔炼而非空气中熔炼的原因是(任写一个化学方程式)。
(2)、合成材料的改良①碱式碳酸铝镁[MgaAlb[OH]c(CO3)d· H2O]是一种新型塑料阻燃剂,其中a、b、c、d的代数关系式:2a+3b= .
(3)、CO2的绿色利用①目前空间站处理CO2的一种方法是在催化剂作用下,利用H2使CO2转化为甲烷并得到生活用水.该反应的化学方程式为 .
②以“铁氧化物”为催化剂,利用太阳能将CO2热解为碳和氧气,这一转化过程(如图2)中化合价升高的非金属元素是 .
18. 某种矿石由氧化镁、氧化铁、氧化铜和二氧化硅组成,用它制备氢氧化镁的流程示意图如图所示(已知:二氧化硅不溶于水也不与稀盐酸反应)。
请回答下列问题:
(1)、溶液A中共含有种阳离子;写出矿石中的任意一种金属氧化物与稀盐酸反应的化学方程式:(只写一个)。(2)、在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子逐步转化为沉淀。该实验条件下,使金属阳离子沉淀的相关pH数据见下表。为保证产品纯度、减少产品损失,并便于操作,所得溶液B的pH的取值范围为。氢氧化物
Fe(OH)3
Cu(OH)2
Mg(OH)2
开始沉淀的pH
1.5
4.2
8.6
完全沉淀的pH
3.2
6.7
11.1
(3)、写出溶液B中加入熟石灰发生的化学反应方程式:。19. 下图为某药品的说明书的一部分: (1)、该药品可治疗疾病;(2)、硫酸亚铁的相对分子质量是;(3)、硫酸亚铁中Fe、S、O元素的质量比为;(4)、一位3岁的儿童若按说明书的用量,一天从药中获得mg铁元素。(计算结果精确到0.1mg)。
(1)、该药品可治疗疾病;(2)、硫酸亚铁的相对分子质量是;(3)、硫酸亚铁中Fe、S、O元素的质量比为;(4)、一位3岁的儿童若按说明书的用量,一天从药中获得mg铁元素。(计算结果精确到0.1mg)。三、简答题
-
20. 炎热的夏季是“登革热(dengue fever)”的高发期,防止蚊虫滋生、预防蚊虫叮咬成为预防“登革热”的重要手段。蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤。蚁酸化学名称叫甲酸,化学式为HCOOH。
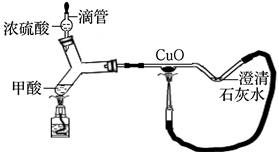 (1)、向盛有蚁酸溶液的试管中滴加 , 观察到溶液中有气泡产生,说明蚁酸溶液显酸性。(2)、如图为某同学制作的微型实验装置,已知蚁酸(甲酸)在浓硫酸及加热的条件下会分解,图中(填现象)说明甲酸分解生成了CO;此装置的优点有:(写一个)(3)、被蚊虫叮咬后,在叮咬处涂抹一些物质可减轻痛痒。下列物质中,你会选择的物质是____A、氢氧化钠溶液 B、食醋 C、苏打水 D、食盐水
(1)、向盛有蚁酸溶液的试管中滴加 , 观察到溶液中有气泡产生,说明蚁酸溶液显酸性。(2)、如图为某同学制作的微型实验装置,已知蚁酸(甲酸)在浓硫酸及加热的条件下会分解,图中(填现象)说明甲酸分解生成了CO;此装置的优点有:(写一个)(3)、被蚊虫叮咬后,在叮咬处涂抹一些物质可减轻痛痒。下列物质中,你会选择的物质是____A、氢氧化钠溶液 B、食醋 C、苏打水 D、食盐水四、综合题
-
21. 下图是一座化学城堡,可以抵御外敌入侵。现有A、B、C、D、E 5种物质作为城堡的守护“卫士”,它们分别由氢、碳、氧、钠、钙中的两种或三种元素组成。五种物质间建立起如图所示的关系才能组成守护的防线,其中物质A和B是常用的灭火剂。
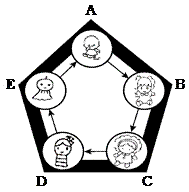 (1)、物质A的化学式为 .(2)、写出反应C→D的化学方程式 .(3)、现有下列物质作为“外敌”分别对城堡发起进攻,若该物质只要与两位相邻的守护“卫士”都能发生反应就能攻破防线,那么能攻入城堡的物质是 .
(1)、物质A的化学式为 .(2)、写出反应C→D的化学方程式 .(3)、现有下列物质作为“外敌”分别对城堡发起进攻,若该物质只要与两位相邻的守护“卫士”都能发生反应就能攻破防线,那么能攻入城堡的物质是 .①铁 ②稀盐酸 ③氧化铁 ④稀硫酸
(4)、室温下,将稀盐酸慢慢滴入装有D溶液的烧杯中,利用温度传感器测出烧杯中溶液的温度,溶液温度随加入盐酸的质量而变化的曲线如下图所示。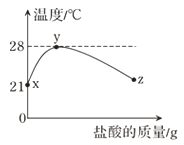
请解释xy段温度变化的原因。
22. 小明取酸性锌锰干电池进行探究,他发现电池内部结构如图1所示。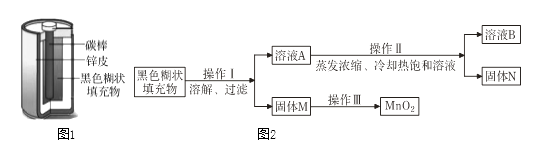
【查阅资料】①锌皮为金属锌(含有少量的铁)
②黑色糊状填充物由炭黑、MnO2、ZnCl2和NH4Cl等组成
③有关数据见下表
温度/℃
0
20
40
60
80
100
溶解度/g
NH4Cl
29.3
37.2
45.8
55.3
65.6
77.3
ZnCl2
343
395
452
488
541
614
(1)、【实验探究一】小明取适量黑色糊状填充物,按图2所示实验流程进行探究。溶液A中溶质主要有(填化学式),操作Ⅱ中采用冷却热饱和溶液的方法实现两者分离的依据是。
(2)、欲从固体M 中得到较纯的MnO2 , 操作Ⅲ可采用的简便方法是。(3)、【实验探究二】小明取电池外壳锌皮,用砂纸打磨干净,剪成小块,进行实验。取一块锌皮放入盛有适量稀盐酸的烧杯中,有ZnCl2生成。
① 实验中可观察到的现象是;
② 下列各组物质混合后,也能生成ZnCl2的有(填字母序号)。
A.ZnO与稀盐酸
B.ZnSO4溶液与BaCl2溶液
C.ZnCO3与NaCl溶液
D.Zn(NO3)2溶液与NH4Cl溶液
(4)、另取一块锌皮放入盛有一定量CuSO4溶液的烧杯中,充分反应后得到溶液E和固体F。当溶液E中只含一种溶质时,该溶质是(填化学式);当固体F中只含一种物质时,溶液E中最少含有种溶质。③若将6.5g锌皮与足量稀硫酸完全反应,则生成氢气的质量0.2g(选填“<”、“>”或“=”)。
五、实验题
-
23. 如图为实验室常用的实验装置.回答问题:
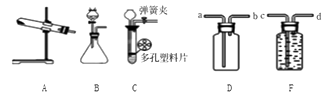 (1)、写出用KClO3与MnO2的制取O2的化学方程式:;若用A装置作为发生装置,还缺少(填仪器名称);若要收集较纯净的氧气,则应将气体从(选填“a”“b”“c”或“d”)通入。(2)、实验室用锌粒与稀硫酸反应制取氢气,发生装置如C图所示。打开止水夹,若发现稀硫酸未能与有孔塑料板上锌粒接触,但此时已无稀硫酸可加,则下列溶液中,最适宜从长颈漏斗中添加的是_________(填字母)。A、氢氧化钠溶液 B、碳酸钠溶液 C、硫酸钠溶液 D、澄清石灰水(3)、小明同学设计了如下图所示的实验装置,既可用于制取CO2 , 又可用于探究CO2的性质。
(1)、写出用KClO3与MnO2的制取O2的化学方程式:;若用A装置作为发生装置,还缺少(填仪器名称);若要收集较纯净的氧气,则应将气体从(选填“a”“b”“c”或“d”)通入。(2)、实验室用锌粒与稀硫酸反应制取氢气,发生装置如C图所示。打开止水夹,若发现稀硫酸未能与有孔塑料板上锌粒接触,但此时已无稀硫酸可加,则下列溶液中,最适宜从长颈漏斗中添加的是_________(填字母)。A、氢氧化钠溶液 B、碳酸钠溶液 C、硫酸钠溶液 D、澄清石灰水(3)、小明同学设计了如下图所示的实验装置,既可用于制取CO2 , 又可用于探究CO2的性质。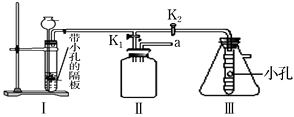
说明:①装置Ⅰ中盛放的药品是石灰石和稀盐酸。②装置Ⅲ中在小试管外壁贴有4片试纸:其中两端的两片用紫色石蕊溶液润湿,中间两片用紫色石蕊溶液浸过并晒干。
a.实验时,打开K1关闭K2可用来制取CO2。装置Ⅰ中发生的化学反应的基本反应类型为 ,装置Ⅰ的优点是;若用排空气法收集CO2 , 请将图Ⅱ补充完整;若在Ⅱ中放入 , 还可用于检验CO2。
B.实验时,关闭K1打开K2可用于探究CO2的性质。实验时Ⅲ中出现的现象是。
六、计算题
-
24. 实验室用10克8%的氢氧化钠溶液和稀硫酸进行中和反应实验,实验过程中溶液的pH变化如图所示:
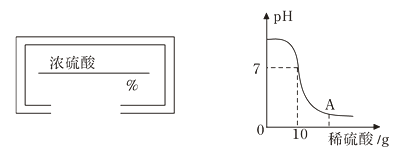 (1)、A点溶液的溶质。(填化学式)(2)、计算所用的该稀硫酸的质量分数?(3)、如果配制100克该稀硫酸所用图中浓硫酸的质量为10克,则图中盛浓硫酸试剂瓶上的标签(已破损)的溶质质量分数应填上%。(4)、图中的浓硫酸多次使用后,发现浓度变小了,原因是。
(1)、A点溶液的溶质。(填化学式)(2)、计算所用的该稀硫酸的质量分数?(3)、如果配制100克该稀硫酸所用图中浓硫酸的质量为10克,则图中盛浓硫酸试剂瓶上的标签(已破损)的溶质质量分数应填上%。(4)、图中的浓硫酸多次使用后,发现浓度变小了,原因是。
-
-