江苏省南京市鼓楼区2017-2018学年中考化学一模考试试卷
试卷更新日期:2018-05-11 类型:中考模拟
一、单选题
-
1. 下列变化属于物理变化的是( )A、
 品红在水中扩散
B、
品红在水中扩散
B、 蜡烛燃烧
C、
蜡烛燃烧
C、 铁生锈
D、
铁生锈
D、 电解水
2. 下列化肥中,属于钾肥的是( )A、尿素 B、氯化钾 C、硝酸铵 D、磷酸二氢铵3. “绿箱子环保计划——废弃手机及配件回收联合行动”已在全国40个重点城市开展了多 年。下列有关废弃手机中的金属材料回收利用的说法错误的是( )
电解水
2. 下列化肥中,属于钾肥的是( )A、尿素 B、氯化钾 C、硝酸铵 D、磷酸二氢铵3. “绿箱子环保计划——废弃手机及配件回收联合行动”已在全国40个重点城市开展了多 年。下列有关废弃手机中的金属材料回收利用的说法错误的是( )
A、可以节约金属资源 B、可以节约冶炼相关金属所消耗的能源 C、可以减少对环境的污染 D、回收废弃手机中的金属材料没有任何价值4. 下列物质由离子构成的是( )
A、铁 B、硫酸铜 C、氨气 D、金刚石5. 下列粒子结构示意图中,表示阳离子的是( )A、 B、
B、 C、
C、 D、
D、 6. 在元素周期表中锡元素的某些信息如图所示,下列有关锡的说法正确的是( )
6. 在元素周期表中锡元素的某些信息如图所示,下列有关锡的说法正确的是( )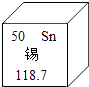 A、原子序数为50 B、属于非金属元素 C、相对原子质量是118.7g D、原子核内中子数为507. 下图实验操作中,正确的是( )A、
A、原子序数为50 B、属于非金属元素 C、相对原子质量是118.7g D、原子核内中子数为507. 下图实验操作中,正确的是( )A、 稀释浓硫酸
B、
稀释浓硫酸
B、 加热液体
C、
加热液体
C、 称量固体质量
D、
称量固体质量
D、 测溶液的 pH
8. 下列有关材料的说法错误的是( )A、蚕丝属于合成纤维 B、保鲜膜属于塑料 C、不锈钢属于金属材料 D、玻璃钢属于复合材料9. 下图表示治理汽车尾气所涉及反应的微观过程。下列说法错误的是( )
测溶液的 pH
8. 下列有关材料的说法错误的是( )A、蚕丝属于合成纤维 B、保鲜膜属于塑料 C、不锈钢属于金属材料 D、玻璃钢属于复合材料9. 下图表示治理汽车尾气所涉及反应的微观过程。下列说法错误的是( ) A、图中所示单质的化学式为N2 B、图中所示有三种氧化物的分子 C、生成单质与化合物的质量比为7:11 D、反应后分子个数变少了10. 葡萄糖属于糖类,其化学式为 C6H12O6。下列有关葡萄糖的说法中错误的是( )
A、图中所示单质的化学式为N2 B、图中所示有三种氧化物的分子 C、生成单质与化合物的质量比为7:11 D、反应后分子个数变少了10. 葡萄糖属于糖类,其化学式为 C6H12O6。下列有关葡萄糖的说法中错误的是( )
A、葡萄糖为有机化合物 B、一个葡萄糖分子中含有 24 个原子 C、葡萄糖的相对分子质量为 180 D、18%的葡萄糖溶液中氧元素的质量分数为 9.6%11. 下列各组离子在水中一定能大量共存,并形成无色溶液的是( )A、Na+、H+、NO3 ﹣、OH﹣ B、H+、K+、Cl﹣、HCO3- C、H+、NH4+ 、NO3﹣、SO42﹣ D、Na+、K+、MnO4﹣、NO3﹣12. 下列实验不能成功的是( )
A、用肥皂水区分软水和硬水 B、用食醋区分食盐和小苏打 C、淬火后的缝衣钢针不能弯曲 D、加熟石灰粉末研磨,区分氯化铵和硫酸铵13. 除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是( )A、NaCl 溶液(MgCl2)——加入过量的 NaOH 溶液,过滤 B、MnO2(KCl)——加水充分溶解,过滤,蒸发结晶 C、CO2(HCl)——通入 NaOH 溶液,干燥 D、Cu(NO3)2 溶液(AgNO3)——加入过量的铜粉,过滤14. 下列四个图像不能正确反映其对应实验操作的是( )
A、 等质量碳酸钙分别与等体积等质量分数的稀盐酸(足量)反应
B、
等质量碳酸钙分别与等体积等质量分数的稀盐酸(足量)反应
B、 20℃时,向一定量不饱和的硝酸钾溶液中加入过量的硝酸钾晶体
C、
20℃时,向一定量不饱和的硝酸钾溶液中加入过量的硝酸钾晶体
C、 向一定量的氢氧化钠溶液中逐滴加入 pH=2 的稀盐酸至过量
D、
向一定量的氢氧化钠溶液中逐滴加入 pH=2 的稀盐酸至过量
D、 向盐酸和氯化钙的混合溶液中滴加碳酸钠溶液
15. 某无色气体可能含有 CO2、CO、H2 中的一种或几种,依次进行以下实验(假设每步反 应均完全进行);①通过赤热的炭层后,恢复到原状态,气体体积增大;②通过灼热的 CuO 时,固体变成红色;③通过白色 CuSO4 粉末时无明显现象(提示:白色 CuSO4 粉末遇水变 蓝)④通入澄清石灰水中,石灰水变浑浊。下列判断正确的是( )
向盐酸和氯化钙的混合溶液中滴加碳酸钠溶液
15. 某无色气体可能含有 CO2、CO、H2 中的一种或几种,依次进行以下实验(假设每步反 应均完全进行);①通过赤热的炭层后,恢复到原状态,气体体积增大;②通过灼热的 CuO 时,固体变成红色;③通过白色 CuSO4 粉末时无明显现象(提示:白色 CuSO4 粉末遇水变 蓝)④通入澄清石灰水中,石灰水变浑浊。下列判断正确的是( )
A、原混合气体中一定含有 CO2 和 CO,一定没有 H2 B、原混合气体中一定没有 CO2 和 H2 , 一定含有 CO C、原混合气体中一定含有 CO2,可能含有 CO,一定没有 H2 D、原混合气体中无法确定是否含有 CO2二、综合题
-
16. 请结合下图回答问题:
 (1)、标出仪器 a 的名称。(2)、实验室通常利用上图中装.置.的.组.合.制取二氧化碳(选填字母),该反应的化学方程式为。(3)、选用 E 装置收集氧气的原因是。(4)、工业上煅烧石灰石可制得生石灰和二氧化碳。如果要制取 5.6t 氧化钙,理论上需要含 碳酸钙 80%的石灰石的质量是多少?17. 水和溶液在生产、生活中起着十分重要的作用。请回 答下列问题:(1)、对于静置沉淀、吸附沉淀、过滤、蒸馏等净化水的操作中,单一操作相对净化程度较高的是。(2)、根据如图 A、B、C 三种固体的溶解度曲线回答:
(1)、标出仪器 a 的名称。(2)、实验室通常利用上图中装.置.的.组.合.制取二氧化碳(选填字母),该反应的化学方程式为。(3)、选用 E 装置收集氧气的原因是。(4)、工业上煅烧石灰石可制得生石灰和二氧化碳。如果要制取 5.6t 氧化钙,理论上需要含 碳酸钙 80%的石灰石的质量是多少?17. 水和溶液在生产、生活中起着十分重要的作用。请回 答下列问题:(1)、对于静置沉淀、吸附沉淀、过滤、蒸馏等净化水的操作中,单一操作相对净化程度较高的是。(2)、根据如图 A、B、C 三种固体的溶解度曲线回答:
①50℃时,等质量的 A、C 的饱和溶液中溶剂的质量大小关系为: AC(填“>”、“=”或“<”)。
②将三种物质饱和溶液的温度分别从 50℃降到 20℃时,溶液中溶质的质量分数最大的 是
(3)、若要配制 98g 质量分数为 10%的稀硫酸,需要质量分数为 98%的浓硫酸(密度为1.84g/cm3)mL(计算结果保留一位小数)。在实验室用浓硫酸配制稀硫酸的主要步 骤有:计算、量取、、冷却至室温装瓶并贴上标签。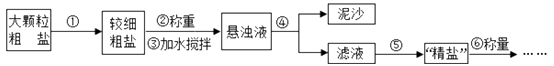
(4)、粗盐提纯的步骤如下:a.操作⑤中用到的仪器有铁架台、玻璃棒、酒精灯、坩埚钳、 , 其中玻璃棒的作用 是。
b. 实验结束后称量获得的精盐,并计算精盐的产率,发现产率偏低,其可能的原因是。
A、食盐没有全部溶解即过滤
B、蒸发时食盐飞溅剧烈
C、蒸发后,所得精盐很潮湿
D、器皿上沾有的精盐没全部转移到称量纸上
18. 阅读下面科普短文。一段时间以来,网传隔夜菜、肉类腌制品不能吃,是因为含亚硝酸盐。对于亚硝酸盐大 家有众多疑问。
疑问一:亚硝酸盐是什么东西? 亚硝酸盐是一类无机化合物的总称,主要指亚硝酸钠(NaNO2),它是白色或淡黄色粉末,有咸味,易溶于水。它是一种常见的食品添加剂,广泛用于各种火腿、酱卤肉等熟肉类食品加工,作为防腐剂和护色剂。国家对食品中含有的亚硝酸盐的最大含量限定为:蔬菜4mg/kg,肉类 3mg/kg。
疑问二:亚硝酸盐的“毒”从何来?
亚硝酸盐本身并无致癌效应,它被吸入血液 1~5 分钟后,就已经分解。亚硝酸盐在胃中酸性环境下,易与氨基酸的分解产物发生反应,产生致癌物。当摄入维生素 C 时可以阻止 致癌物产生。
疑问三:隔夜菜中的亚硝酸盐含量会超标吗? 实验人员准备了清炒菠菜、清炒芹菜和小白菜炒肉,三种菜各自被分成 6 份,常温和冷藏条件下各保存一半。实验人员分别取 1 小时后、6 小时后、20 小时后的剩菜,经过捣碎、提取、离心、过滤,取出汤汁。通过比色法逐一测得样品中亚硝酸盐含量,如下图所示。

实验结果表明,三种菜在放置 20 小时后,无论常温还是冷藏,亚硝酸盐含量虽均有增 加,但都远未超过国家标准。
疑问四:摄入多少亚硝酸盐会对人体产生危害?
人体对亚硝酸盐的一次性安全摄入量为每千克体重 0.2 mg。我们日常吃的大米、蔬菜、 肉品里面几乎都含有亚硝酸盐。有数据显示,人体摄入的亚硝酸盐 80%来自蔬菜。如果你 体重 50 kg,即使一次性吃 2.5 kg 蔬菜也是安全的。因此,将亚硝酸盐摄入量控制在安全范 围内不会对人体造成危害。
依据文章内容,回答下列问题。
(1)、亚硝酸钠中氮元素的化合价为。(2)、人体对亚硝酸盐的一次性安全摄入量为。(3)、下列有关说法正确的是_____。A、“吃隔夜菜会致癌”是没有科学依据的 B、常温储存及冷藏储存条件下,亚硝酸盐含量均呈增加趋势 C、适量吃富含维生素的新鲜蔬菜水果,有利于抑制致癌物的产生 D、从实验数据中发现蔬菜类的隔夜菜亚硝酸 盐含量要高于含肉类的隔夜菜(4)、亚硝酸钠是实验室常用的试剂,实验室 一般用亚硝酸钠溶液与氯化铵溶液反应来制 取 N2。N2 的化学性质十分稳定,但在一定条件下能与 H2 部.分.化.合.生成 NH3。如图为制取少量 NH3 的装置(获取 H2 的装置已略去):
①C 装置的硬质试管中发生反应的化学方程 式为。
②反应时 N2 和 H2 的质量比如果按此比例进行反应,反应时,D 中导管口有气泡逸出,说明逸出气泡的原因(已知 NH3极易溶于水):。
③B 中浓硫酸的作用是。
④用实验方法证明确实有 NH3 生成。
三、流程题
-
19. 我国著名的化学家侯德榜发明的“侯氏制碱法”,是向饱和食盐水中通入过量氨气,再通入过量的二氧化碳,即可析出 NaHCO3 固体,将其加热得到纯碱。其原理流程如下 图所示:
 (1)、操作Ⅲ的名称是。(2)、氨气极易溶于水,向饱和食盐水通入氨气可得到饱和食盐水和氨水的混合盐水(称为 氨盐水)。氨盐水比食盐水更容易吸收二氧化碳,其原因是;
(1)、操作Ⅲ的名称是。(2)、氨气极易溶于水,向饱和食盐水通入氨气可得到饱和食盐水和氨水的混合盐水(称为 氨盐水)。氨盐水比食盐水更容易吸收二氧化碳,其原因是;
(3)、写出制取碳酸氢钠的化学方程式。四、推断题
-
20. 下图中 A、B、C、D、E、F 是初中常见物质,其 中 A、B、C、D、E 是五种不同类别的物质,D 是氧化物, 且 D 中两种元素的质量比为 3:8。图中“—”表示两端物质间能 发生化学反应,“→”表示物质间存在转化关系;反应条件、 部分反应物和生成物已略去。
 (1)、D 物质是(填写化学式)。(2)、写出 B 与 C 反应的化学方程式:。(3)、写出 F→E 的化学反应方程式:。
(1)、D 物质是(填写化学式)。(2)、写出 B 与 C 反应的化学方程式:。(3)、写出 F→E 的化学反应方程式:。五、科学探究题
-
21. 我国钢铁年产量居世界第一,为国民经济的发展奠定了坚实的基础。(1)、工业上以空气、铁矿石、石灰石和为原料来冶炼生铁。铁矿石冶炼成铁是一个复杂的过程,某炼铁厂用赤铁矿来炼铁,其炼铁的主要原理是(用化学方程式表示)。
已知某铁锈的成分为 Fe2O3•xH2O 和 FeCO3 , 某兴趣小组的同学在老师指导下测定其组成。
(2)、【提出问题】根据铁生锈得成分推测,参加反应的除了空气中的氧气和水蒸气之外,还有 参加了反应。
(3)、如何确定此铁锈的组成?【查阅资料】
①Fe2O3•xH2O 失去结晶水温度为 110℃,FeCO3 在 282℃ 分解为 FeO 和 CO2 , Fe2O3 在 300℃时不分解。
②本实验条件下,二氧化碳气体的密度为 1.80g/L,装置内空气中的水蒸气和二氧化碳对相 关数据测定的影响可忽略不计。
【设计方案】兴趣小组的同学设计了如下图所示的实验装置(夹持仪器省略)进行实验。(B、D 装置中药品均足量)

【实验步骤】
①连接仪器,并检查装置气密性。
②取一定量此铁锈样品,准确称得其质量为 5.44g。
③按上图所示装入药品,测量并记录相关数据 I。
④连接 A、B、C 装置,关闭装置 A 中活塞,C 装置读数后,控制 A 装置在 300℃ 进行实验。当观察到 C 装置中有现象时,停止加热,待装置冷却后,再次测量并记 录相关数据 II。
(4)、【相关数据】Ⅰ
Ⅱ
A 装置的质量/g
55.44
53.92
B 装置的质量/g
102.00
103.08
C 装置读数/mL
0
244.4
【问题讨论】
Ⅰ.量气管中水面上油的作用是。 分析计算测量的数据,FeCO3 的质量为g,x 为。
Ⅱ.下列数据组合能确定样品组成的是(填序号)。
①A、B 装置反应前后测得的数据 ②A、C 装置反应前后测得的数据
③B、C 装置反应前后测得的数据
(5)、【拓展探究】小华同学将上述实验中的 C 装置换成 D 装置来测定二氧化碳气体的质量,并根据测定的数 据确定样品的组成。小华同学通过多次反复实验发现,在此实验中,用 C 装置测定二氧化 碳气体的体积与用 D 装置测定二氧化碳气体的质量相比较,当误差数值都为 0.1 时,前者对 实验结果影响小。试通过计算说明原因。
-
-