北京市石景山区2017-2018学年中考化学一模考试试卷
试卷更新日期:2018-05-11 类型:中考模拟
一、单选题
-
1. 下列制作蛋糕的原料中,富含蛋白质的是( )A、面粉 B、鸡蛋 C、白糖 D、橄榄油2. 下列气体中,能供给动植物呼吸的是( )
A、H2 B、O2 C、N2 D、CO23. 下列元素中,人体摄入量过低会引起贫血的是( )A、Fe B、Zn C、Na D、Ca4. 下列符号中,表示2个氢分子的是( )A、H2 B、2H C、2H2 D、2H2O5. 铁锅能烹饪食品,说明铁具有良好的( )
A、导电性 B、延展性 C、导热性 D、抗腐蚀性6. 水晶的主要成分是二氧化硅(SiO2),SiO2中硅元素的化合价为( )A、﹣4 B、﹣2 C、﹢2 D、﹢47. 下列实验操作中,正确的是( )A、 滴加液体
B、
滴加液体
B、 过滤
C、
过滤
C、 取用粉末药品
D、
取用粉末药品
D、 点燃酒精灯
8. 下列不属于二氧化碳用途的是( )A、用作燃料 B、制碳酸饮料 C、用于灭火 D、植物的光合作用9. 下列金属中,不能从CuSO4溶液中置换出Cu的是( )A、Fe B、Zn C、Mg D、Ag10. 下列物质露置于空气中,一段时间后,质量减小的是( )
点燃酒精灯
8. 下列不属于二氧化碳用途的是( )A、用作燃料 B、制碳酸饮料 C、用于灭火 D、植物的光合作用9. 下列金属中,不能从CuSO4溶液中置换出Cu的是( )A、Fe B、Zn C、Mg D、Ag10. 下列物质露置于空气中,一段时间后,质量减小的是( )
A、浓盐酸 B、浓硫酸 C、氢氧化钠 D、碳酸钙11. 甲和乙在点燃条件下生成丙和丁,结合微观示意图分析,下列结论错误的是( ) A、1个甲分子由5个原子构成 B、生成丙和丁的分子个数比为1:2 C、该化学反应前后,原子种类保持不变 D、丁物质中氢和氧元素质量比为2:112. 下图是a、b两种固体物质的溶解度曲线。下列说法中错误的是( )
A、1个甲分子由5个原子构成 B、生成丙和丁的分子个数比为1:2 C、该化学反应前后,原子种类保持不变 D、丁物质中氢和氧元素质量比为2:112. 下图是a、b两种固体物质的溶解度曲线。下列说法中错误的是( ) A、a物质的溶解度随温度的升高而增大 B、t2℃时b物质的溶解度比a物质的溶解度大 C、M点表示在t1℃时a、b两种物质的溶解度相等 D、升高温度可以将a、b的饱和溶液转化为不饱和溶液
A、a物质的溶解度随温度的升高而增大 B、t2℃时b物质的溶解度比a物质的溶解度大 C、M点表示在t1℃时a、b两种物质的溶解度相等 D、升高温度可以将a、b的饱和溶液转化为不饱和溶液二、填空题
-
13. 采用熔盐蓄热储能的光热发电站,其工作原理如下图所示。
 (1)、该发电站利用的新能源是。(2)、熔盐蒸汽发生器中,冷水被加热产生蒸汽,推动蒸汽涡轮机发电。该发生器中发生的是变化。(3)、贮罐中的熔盐为60%NaNO3、40%KNO3 , 该熔盐属于 (填“纯净物”或“混合物”);NaNO3的相对分子质量 (填“大于”或“小于”)KNO3的相对分子质量。14. “绿水青山就是金山银山”。某电镀厂处理含硫酸废水过程如下图所示。
(1)、该发电站利用的新能源是。(2)、熔盐蒸汽发生器中,冷水被加热产生蒸汽,推动蒸汽涡轮机发电。该发生器中发生的是变化。(3)、贮罐中的熔盐为60%NaNO3、40%KNO3 , 该熔盐属于 (填“纯净物”或“混合物”);NaNO3的相对分子质量 (填“大于”或“小于”)KNO3的相对分子质量。14. “绿水青山就是金山银山”。某电镀厂处理含硫酸废水过程如下图所示。 (1)、该过程中发生反应的化学方程式为。(2)、下列物质中,能用于检验废水中含有硫酸的是 (填序号)。A、铁粉 B、紫色石蕊溶液 C、pH试纸(3)、若处理含硫酸98 kg的废水,则至少加入熟石灰的质量为 kg。15. 请从A或B两题中任选1个作答,若两题均作答,按A计分。
(1)、该过程中发生反应的化学方程式为。(2)、下列物质中,能用于检验废水中含有硫酸的是 (填序号)。A、铁粉 B、紫色石蕊溶液 C、pH试纸(3)、若处理含硫酸98 kg的废水,则至少加入熟石灰的质量为 kg。15. 请从A或B两题中任选1个作答,若两题均作答,按A计分。A.下图为“**泡打粉”标签
【品名】**泡打粉
【保存】请置于阴凉干燥处
【配料】碳酸氢钠、碳酸钙、柠檬酸等
【使用方法】直接与面粉混合
B.下图为“胃酸完全抑制剂”标签
【药品名称】胃酸完全抑制剂
【主要成分】每片内含碳酸钙800mg氢氧化镁116mg
【用途】用于胃酸过多、消化不良等
【用法用量】口服一次1片每日2次
①碳酸氢钠俗称。
②加入泡打粉制作的蛋糕更松软,其原理可用化学方程式表示为:3NaHCO3+C6H8O7=C6H5O7Na3+3H2O+3X↑,则X的化学式为。
①氢氧化镁和胃酸发生的反应为:Mg(OH)2+2HCl= MgCl2+2H2O,该反应的基本类型是反应。
②碳酸钙与胃酸反应的化学方程式为。
三、简答题
-
16. 阅读下面科普短文。
最近关于水果打蜡的报道很多,引发了许多疑问。
问题1:水果能打蜡吗?
根据中国《食品添加剂使用卫生标准》,允许使用规定的、适量的食用蜡对鲜水果进行处理。食用蜡原料主要来自于动植物,如蜂蜡、棕榈蜡等,蜂蜡中的主要成分为十六烷酸(C16H32O2)与三十烷醇(C30H62O)形成的脂类。人体少量接触食用蜡不会产生危害,偶尔食用也可排出体外。
问题2:为什么给水果打蜡?
给水果打蜡最主要的目的是为了保鲜。下图是农科院王日葵等人对夏橙的研究结果。

问题3:如何分辨水果是否打了工业蜡?
用工业蜡加工水果,其中的重金属成分对人体会造成伤害。下面提供几种分辨方法。一是看,工业蜡多含有染色剂,使用湿纸巾擦拭水果表面,如有较重的颜色可能是工业蜡;二是闻,经工业蜡处理的水果会发出轻微的刺鼻味;三是刮,经工业蜡处理的水果用手指甲或水果刀一刮,会看到一层白色的蜡状物。
问题4:打蜡的水果如何清洗?
热水清洗:蜡遇热会熔化,把打蜡水果放到热水中,水中浮起一层蜡。
食盐洗:食盐的小颗粒能增强摩擦,也可以杀菌消毒。
另外,建议购买时令水果,少购买反季节及长途运输的水果,以减少买到打蜡水果的几率。
依据文章内容,回答下列问题。
(1)、给水果打蜡的主要目的是。(2)、研究人员对夏橙的研究,得出的结论是。(3)、根据热水清洗,可以得出蜡的物理性质有。(4)、C16H32O2与C30H62O两种物质具有的相同点是。四、流程题
-
17. 氯化钙应用广泛,以石灰石(杂质主要是Fe2O3、MgSO4)为原料生产氯化钙的流程如下。

已知:BaCl2 + MgSO4 = BaSO4↓+ MgCl2
Ca(OH)2 + MgCl2 = Mg(OH)2↓+ CaCl2
Ca(OH)2 + FeCl3 = Fe(OH)3↓+ CaCl2
(1)、氧化铁与盐酸反应的化学方程式为。(2)、滤液1中的溶质有HCl、FeCl3、MgSO4和。(3)、滤液2中加入Ca(OH)2是为了除去 (填序号,下同)。A、MgCl2 B、FeCl3 C、HCl(4)、滤液3呈碱性,为使溶液pH降低,可加入适量的 。A、NaCl B、NaOH C、盐酸五、实验题
-
18. 根据下图回答问题。请从A或B两题中任选1个作答,若两题均作答,按A计分。

A
B
⑴实验室制取CO2选取的发生装置是 (填序号)。
⑵用C装置收集CO2 , 检验收集满的方法是。
⑴实验室用高锰酸钾制取O2的化学方程式为。
⑵因为O2不易溶于水,可以用 (填序号)装置收集。
19. 根据下图所示研究氧气的性质。 (1)、木炭在氧气中燃烧的化学方程式为。(2)、图2实验中观察到细铁丝剧烈燃烧、放出热量、。(3)、图1和图2中液体的作用分别是。20. 根据下图所示研究二氧化碳的性质。
(1)、木炭在氧气中燃烧的化学方程式为。(2)、图2实验中观察到细铁丝剧烈燃烧、放出热量、。(3)、图1和图2中液体的作用分别是。20. 根据下图所示研究二氧化碳的性质。 (1)、若X为紫色石蕊溶液,观察到的现象是、澄清石灰水变浑浊。澄清石灰水中发生反应的化学方程式为。(2)、若X为氢氧化钠溶液,观察到澄清石灰水中无明显现象,其原因是。21. 利用下图装置测定空气中氧气含量。
(1)、若X为紫色石蕊溶液,观察到的现象是、澄清石灰水变浑浊。澄清石灰水中发生反应的化学方程式为。(2)、若X为氢氧化钠溶液,观察到澄清石灰水中无明显现象,其原因是。21. 利用下图装置测定空气中氧气含量。
已知:Y型管体积(已去除胶塞占的体积)为a mL,注射器中水的体积为b mL。
实验步骤:检查气密性;用酒精灯加热红磷至燃烧;反应结束并冷却后,读取注射器中水体积为c mL。
(1)、实验中红磷和水要足量,目的是。(2)、根据实验数据,求算空气中氧气体积分数的计算式为。六、科学探究题
-
22. 碘化钾(KI)保存不当会变质。实验小组进行以下实验探究KI变质的因素。
【提出问题】 KI变质的条件是什么?
【查阅资料】
① KI为白色粉末,暴露在空气中或久置会被氧化为碘(I2)而泛黄变质。
② 碘水中含较多KI时,滴加淀粉溶液显紫色或蓝紫色
【进行实验】分别取适量KI于燃烧匙中,再分别放入盛有不同物质的集气瓶中,塞紧胶塞,若干天后观察。
实验1
实验2
实验3
实验4



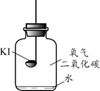
固体变潮、表面变微黄
固体无明显现象
固体变潮、无其他明显现象
固体变潮、表面变黄
继续实验:取实验1中少量微黄固体溶解,加入淀粉溶液,溶液变紫色。
取实验4中少量黄色固体溶解,加入淀粉溶液,溶液变紫色。
【解释与结论】
(1)、实验3的目的是。(2)、对比实验 , 可以得出KI变质一定与水有关。(3)、从上述实验可推知,KI变质的条件是。(4)、【提出问题2】CO2的作用是什么?【进行实验】分别取10 mL同浓度的KI溶液于3支试管中,再向试管2中通入CO2 , 向试管3中滴加几滴盐酸;分别测溶液的pH;几分钟后,观察溶液的颜色;再向试管中滴入淀粉溶液,观察溶液的颜色。实验现象记录如下:
试管序号
1
2
3
溶液pH
pH=8.5
pH=6.5
pH=4.5
溶液颜色
无色
浅黄色
黄色
滴加淀粉溶液后的颜色
无色
紫色
深紫色
较长时间后,观察到试管1中溶液变为紫色。
【解释与结论】
试管1实验的目的是。
(5)、CO2在KI变质过程中的作用是。(6)、【反思与评价】探究KI变质条件时,同学们排除了氮气和稀有气体的影响,其原因是。
-
-