广州市南沙区2017-2018学年中考化学一模考试试卷
试卷更新日期:2018-05-11 类型:中考模拟
一、单选题
-
1. 厨房里的下列操作中,发生了化学变化的是( )A、拉面条 B、磨豆浆 C、切黄瓜 D、酿米酒2. 下列物质属于盐类的是( )A、丙酸:C2H5COOH B、氨水:NH3·H2O C、氯化铵:NH4Cl D、熟石灰:Ca(OH)23. 在A+3B = 2C+2D的反应中,14gA完全反应生成44gC和18gD,若A的相对分子质量为28,则B的相对分子质量是( )A、16 B、32 C、64 D、964. 关于分子和原子两种微粒的叙述正确的是( )A、物质只能由分子构成 B、相同原子可能构成不同的分子 C、分子质量一定大于原子质量 D、化学变化中分子数目一定发生变化5. 下列有关水的说法中错误的是( )A、水(H2O)和过氧化氢(H2O2)分子中都含有氢气分子(H2) B、电解水实验中证明水是由氢、氧两种元素组成的 C、用肥皂水可以区分软水和硬水 D、常用吸附、沉淀、过滤和蒸馏等方法净化水6. 下图是某原子的结构示意图。下列关于该原子的说法错误的是( )
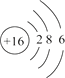 A、属于金属元素原子 B、最外层电子数为6 C、在化学反应中容易得到电子 D、原子核外有3个电子层7. 我国古代科技高度发达,对中国古代著作涉及化学的叙述,下列解读错误的是( )
A、属于金属元素原子 B、最外层电子数为6 C、在化学反应中容易得到电子 D、原子核外有3个电子层7. 我国古代科技高度发达,对中国古代著作涉及化学的叙述,下列解读错误的是( )
A、《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”中的“碱”是K2CO3 B、《黄白第十六》中“曾青涂铁,铁赤如铜”,其“曾青”是可溶性铜盐 C、《天工开物》中“凡石灰,经火焚炼为用”里的“石灰”指的是Ca(OH)2 D、《汉书》中“高奴县有洧水可燃”,这里的“洧水”指的可能是石油8. 婴儿“尿不湿”最关键的材料是聚丙烯酸钠,它是由丙烯酸(C3H4O2)与氢氧化钠经过一系列反应而制得。下列有关丙烯酸的说法中,正确的是( )A、它是有机高分子化合物 B、其中氧元素与氢元素的质量比为9:1 C、其中碳元素的质量分数为16.7% D、丙烯酸的相对分子质量为729. 下列实验操作正确的是( )A、滴加液体 B、取用固体
B、取用固体 C、测溶液pH
C、测溶液pH 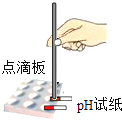 D、过滤
D、过滤 10. 高氯酸铵(NH4ClO4)可用作高能燃料,NH4ClO4中氯元素的化合价为( )A、-1 B、+7 C、-7 D、+111. 某同学在实验室测定了几种溶液的pH,其结果如下表:
10. 高氯酸铵(NH4ClO4)可用作高能燃料,NH4ClO4中氯元素的化合价为( )A、-1 B、+7 C、-7 D、+111. 某同学在实验室测定了几种溶液的pH,其结果如下表:溶液
盐酸
CuCl2溶液
Na2SO4溶液
水
Na2CO3溶液
NaOH溶液
pH
<7
<7
=7
=7
>7
>7
该同学由此得出结论正确的是( )
A、pH<7一定是酸的溶液 B、pH>7一定是碱的溶液 C、pH=7一定是盐溶液 D、盐溶液可能显酸性、碱性或中性12. 下列方法中,不能达到目的是( )选项
物质(括号内为杂质)
除去杂质的方法
A
NaOH溶液(Na2SO4)
加入适量的Ba(OH)2溶液、过滤
B
CaO(CaCO3)
加水溶解、过滤
C
CO(CO2)
通过足量氢氧化钠溶液,并干燥
D
CuSO4溶液(H2SO4)
加足量氧化铜粉末,过滤
A、A B、B C、C D、D13. 下列有关物质的性质和用途说法中,错误的是( )
A、石墨深灰色,质软,可制铅笔芯 B、金刚石非常坚硬,可作钻石戒指 C、碳具有还原性,可用于冶炼金属 D、浓硫酸有吸水性,可作某些气体的干燥剂14. 下列关于空气的说法正确的是( )A、空气中CO2是导致酸雨的主要原因 B、按质量计算,空气中氮气约占78% C、空气中PM2.5含量高说明空气质量好 D、空气中的氮气可用于食品防腐剂15. 下列说法正确的是( )
A、KNO3 20℃时的溶解度大于80℃时溶解度 B、氯化钠溶液能够导电是因为溶液中存在自由移动的阴、阳离子 C、加热KClO3时,用MnO2作催化剂,能提高氧气的产量 D、相同条件下,NaCl溶于水时溶液温度高于NaOH溶于水时溶液温度16. 下列物品所使用的材料,属于有机合成材料的是( )A、 涤纶背包
B、
涤纶背包
B、 纯棉帽子
C、
纯棉帽子
C、 陶瓷水杯
D、
陶瓷水杯
D、 铜质金鸡奖杯
17. 把等质量的X、Y、Z、M四种金属分别加入到同体积、同浓度的足量稀盐酸中.再把X加入到Z(NO3)2溶液中,M加入到YNO3溶液中.反应关系如图所示.据此判断四种金属的活动性顺序为( )
铜质金鸡奖杯
17. 把等质量的X、Y、Z、M四种金属分别加入到同体积、同浓度的足量稀盐酸中.再把X加入到Z(NO3)2溶液中,M加入到YNO3溶液中.反应关系如图所示.据此判断四种金属的活动性顺序为( ) A、Z>X>M>Y B、X>Z>M>Y C、X>Z>Y>M D、Y>M>Z>X18. 下列做法正确的是( )A、用燃烧的方法区分纯羊毛毛线和腈纶毛线 B、将自来水通过活性炭,得到无色透明的纯净水 C、稀释浓硫酸时,将水缓慢倒入浓硫酸中,并不断搅拌 D、不慎将烧碱溶液沾到皮肤上,应立即用大量的水冲洗,并涂上稀盐酸19. 为了使小麦叶色浓绿,增强抗倒伏能力,应施加的复合肥是( )A、尿素(CO(NH2)2) B、氯化钾 C、硝酸钾 D、磷酸二氢铵(NH4H2PO4)20. 下列关于Ba(OH)2性质描述中,不属于碱的通性的是( )A、能使紫色石蕊溶液变蓝色 B、能与二氧化碳反应生成碳酸钙沉淀和水 C、能与硫酸钠溶液反应生成硫酸钡沉淀和氢氧化钠 D、能与盐酸反应生成氯化钡和水
A、Z>X>M>Y B、X>Z>M>Y C、X>Z>Y>M D、Y>M>Z>X18. 下列做法正确的是( )A、用燃烧的方法区分纯羊毛毛线和腈纶毛线 B、将自来水通过活性炭,得到无色透明的纯净水 C、稀释浓硫酸时,将水缓慢倒入浓硫酸中,并不断搅拌 D、不慎将烧碱溶液沾到皮肤上,应立即用大量的水冲洗,并涂上稀盐酸19. 为了使小麦叶色浓绿,增强抗倒伏能力,应施加的复合肥是( )A、尿素(CO(NH2)2) B、氯化钾 C、硝酸钾 D、磷酸二氢铵(NH4H2PO4)20. 下列关于Ba(OH)2性质描述中,不属于碱的通性的是( )A、能使紫色石蕊溶液变蓝色 B、能与二氧化碳反应生成碳酸钙沉淀和水 C、能与硫酸钠溶液反应生成硫酸钡沉淀和氢氧化钠 D、能与盐酸反应生成氯化钡和水二、综合题
-
21. 人类的生活和生产都离不开金属材料。(1)、下列物质不属于合金的是 。(填序号)A、青铜 B、铝 C、钢 D、生铁(2)、每年因腐蚀而报废掉的金属材料数量惊人,铁生锈条件是铁与同时接触。(3)、工业炼铁可以把赤铁矿(主要成分为Fe2O3 )在高炉里和CO反应,该反应的化学方程式是;
① 氧化铁(Fe2O3)的相对分子质量是;
② 2000t含氧化铁80%的赤铁矿中理论上可炼得含铁95%生铁t。(保留一位小数)
22. 从微观视角认识和考察物质世界是学习化学的重要思维方法。(1)、下图是某反应的微观示意图:
B框中的物质属于 (填序号:①化合物 ②单质 ③纯净物 ④混合物)。此反应化学方程式为。
(2)、写出下图A所示的反应化学方程式 , 属于反应(填反应类型)。该反应前后,溶液减少的离子是。下图B中反应溶液变为无色时,此时溶液中大量存在的粒子是。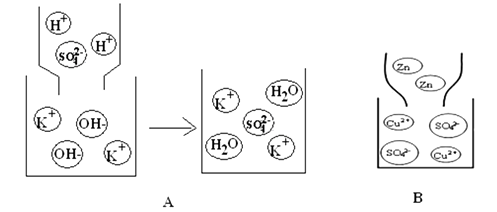 23. 下列是初中化学常见的实验或操作,回答下列问题:
23. 下列是初中化学常见的实验或操作,回答下列问题:A.
 量筒读数
量筒读数B.
 过滤
过滤C.
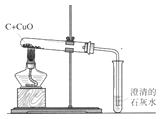 木炭还原氧化铜
木炭还原氧化铜 D.
 铁丝在氧气中燃烧(1)、A实验中读出液体的体积是mL。(2)、B实验中玻璃棒的作用是。(3)、C实验中看到的实验现象:。(4)、D实验把细铁丝盘成螺旋状目的是 , 集气瓶中放点水的目的是 , 铁丝燃烧的化学方程式是。24. Mg(OH)2是一种新型的阻燃剂,在温度达到380℃时吸收热量并分解产生水,同时生成的氧化镁附着于可燃物的表面阻止了进一步燃烧。
铁丝在氧气中燃烧(1)、A实验中读出液体的体积是mL。(2)、B实验中玻璃棒的作用是。(3)、C实验中看到的实验现象:。(4)、D实验把细铁丝盘成螺旋状目的是 , 集气瓶中放点水的目的是 , 铁丝燃烧的化学方程式是。24. Mg(OH)2是一种新型的阻燃剂,在温度达到380℃时吸收热量并分解产生水,同时生成的氧化镁附着于可燃物的表面阻止了进一步燃烧。
(1)、工业常用氯化镁溶液与烧碱溶液制取Mg(OH)2 , 化学方程式是。(2)、某同学用氨水在实验室模拟制取Mg(OH)2的过程:一定温度下,往含一定量氯化镁的溶液中加入适量氨水(氨水易挥发),再经过滤、洗涤得到Mg(OH)2晶体。为探究获得较高Mg(OH)2晶体转化率条件,该同学进行如下对比实验,数据如下:实验编号
氯化镁溶液溶质质量分数
反应温度/℃
Mg(OH)2转化率/%
a
10%
30
27.06
b
15%
30
56.77
c
15%
40
69.64
d
15%
60
54.30
e
20%
60
50.60
①实验b和c的目的是。
②由实验可知,能够得到最多Mg(OH)2的条件是溶质质量分数和温度℃。
③在氯化镁溶液溶质质量分数都是40%的情况下,60℃时Mg(OH)2的转化率比40℃时低的原因是。
(3)、根据燃烧的条件可知,Mg(OH)2能做阻燃剂的原因是 (填编号)。①清除可燃物 ②使温度降低到着火点以下 ③隔绝空气
25.(1)、我们已经学习了氢氧化钠的性质,知道这种固体要密封保存,原因有:①;②。兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验:
(2)、【对固体猜想】猜想I:全部是NaOH;猜想II:全部是Na2CO3;猜想III:是NaOH和Na2CO3混合物
【实验和推断】
为进一步确定成分,进行了以下探究:

填写以下实验报告:
实验操作
实验现象
实验结论
第一步:用试管取约2mL该无色溶液,滴入适量澄清石灰水。
现象a:溶液变浑浊。
化学方程式:① , 证明有碳酸钠。
第二步:静置,取上层清液于另一试管中,滴入无色酚酞溶液。
现象b:②
证明含有NaOH,猜想III成立,是NaOH和Na2CO3混合物
③分析:小组中有同学提出质疑,认为以上实验不能证明猜想III成立,理由是:
a、Na2CO3溶液呈碱性;
b、。
(3)、兴趣小组按下图实验测定部分变质的NaOH固体中Na2CO3的质量分数。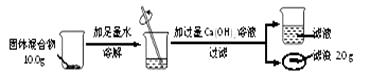
①根据题中信息 (填“能”或“不能”)计算Ca(OH)2溶液的质量分数。
②通过计算,固体混合物中Na2CO3的质量分数是。
三、填空题
-
26. 下图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点。据图回答:
 (1)、P点的含义是。(2)、t2℃时30ga物质加入到50g水中不断搅拌,形成的溶液质量是g。
(1)、P点的含义是。(2)、t2℃时30ga物质加入到50g水中不断搅拌,形成的溶液质量是g。
(3)、t2℃时a、b、c三种物质的溶解度按由小到大的顺序排列是(填写物质序号)。(4)、在t2℃时,将等质量的a、b、c三种物质的饱和溶液同时降温至t1℃时,析出晶体最多的是 , 所得溶液中溶质质量分数最小的是。四、实验题
-
27. 某课外活动小组为测定铜锌合金中铜的质量分数,设计了下列实验:
①称取ag样品放入烧杯,滴入足量稀盐酸。
②取一张质量为bg的滤纸,制作并安装好过滤器。
③待①中反应充分后,过滤。
④取沉淀连同滤纸放在干燥器中干燥后,称量,质量为cg。
回答下列问题:
(1)、称量样品时,应把样品放在托盘天平的盘里。(2)、过滤中发现滤液出现浑浊,应如何处理?。(3)、通过上述实验测得的铜的质量分数是 (用a、b、c表示)。(4)、老师指出,③、④之间缺少一个步骤,使实验结果偏大。该步骤操作是。28. 下图是实验室中常用的几种装置,回答下列问题: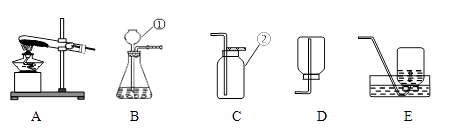 (1)、写出有编号仪器的名称:① , ②。(2)、利用上述B、C装置的组合可以制取一种可供呼吸的气体是 , 加入药品前应首先 , 制取该气体的化学方程式。为防止生成的气体从长颈漏斗逸出,添加的液体应。(3)、实验室用锌粒与稀硫酸反应制取并收集干燥的氢气,应选用的气体收集装置是 (填装置代号),该反应化学方程式为。
(1)、写出有编号仪器的名称:① , ②。(2)、利用上述B、C装置的组合可以制取一种可供呼吸的气体是 , 加入药品前应首先 , 制取该气体的化学方程式。为防止生成的气体从长颈漏斗逸出,添加的液体应。(3)、实验室用锌粒与稀硫酸反应制取并收集干燥的氢气,应选用的气体收集装置是 (填装置代号),该反应化学方程式为。五、科学探究题
-
29. 实验设计是化学实验的重要环节。请根据下列实验要求回答相关问题:
(1)、【活动与探究一】用对比实验方法探究二氧化碳的性质。实验一
实验二


①实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度由大到小顺序为 , B瓶内变浑浊的化学方程式为。
②实验二观察到C装置中发生的现象是、 , 结论是 (用化学方程式表示)。
(2)、【活动与探究二】定量测定空气中氧气的含量。实验三
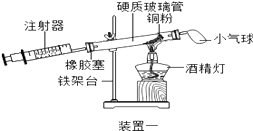
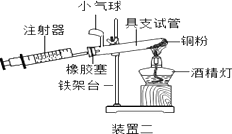
①实验三中,反应的原理为 (用化学方程式表示);
②装置一比装置二更合理,理由是。
根据下表提供的实验数据,完成下表:
硬质玻璃管中空气体积
反应前注射器中空气体积
反应后注射器中气体体积
实验测得空气中氧气体积分数
30mL
20mL
10mL
③
④定量实验操作中易产生误差,如果反应前气球中存在气体(其量小于注射器内的空气),而实验后冷却至室温,将气球内的气体全部挤出读数,导致实验测得结果(填“偏小”、“偏大”或“无影响”)。
-