粤教版2018年中考化学模拟试卷
试卷更新日期:2018-04-24 类型:中考模拟
一、单选题
-
1. 下列几种常见的物质中,属于纯净物的是( )A、食醋 B、碳酸氢铵 C、空气 D、自来水2. 下列变化属于化学变化的是( )A、火药爆炸 B、海水晒盐 C、黄瓜榨汁 D、干冰升华3. 下列关于混合物、酸、碱、盐、氧化物分类完全正确的是( )
混合物
酸
碱
盐
氧化物
A
冰水混合物
硫酸
氢氧化钠
硫酸钡
干冰
B
焦炉煤气
硝酸
氢氧化钙
碳酸氢钙
四氧化三铁
C
合金
盐酸
碱式碳酸铜
氯化银
一氧化碳
D
空气
醋酸
氢氧化钡
碳酸钙
氯酸钾
A、A B、B C、C D、D4. 下列化学用语正确的是( )
A、水银—Ag B、两个氢原子:2H C、镁离子:Mg+2 D、纯碱- NaOH5. 下列说法正确的是( )A、煤气泄漏,用明火查看 B、明矾净水,能杀菌消毒 C、油锅着火,可加水浇灭 D、金属回收,可节能防污6. 下列是某兴趣小组制取二氧化碳,收集并检验该气体的有关实验操作,其中错误的是( ) A、甲图中推动注射器时,长颈漏斗下端液面上升,说明气密性良好 B、乙图中长颈漏斗下端要伸入液面下,是为了防止气体逸出 C、丙图装置中植物油的作用是为了防止二氧化碳气体溶于水 D、丁图中为了检验二氧化碳气体,滴入的试剂为氢氧化钠溶液7. 下列实验不能达到预期目的的是A、用肥皂水区别硬水和软水 B、用碘水区别淀粉和蔗糖 C、用酚酞试液区别盐酸和食盐水 D、用点燃法区别聚乙烯和聚氯乙烯8. 下列排列顺序正确的是( )
A、甲图中推动注射器时,长颈漏斗下端液面上升,说明气密性良好 B、乙图中长颈漏斗下端要伸入液面下,是为了防止气体逸出 C、丙图装置中植物油的作用是为了防止二氧化碳气体溶于水 D、丁图中为了检验二氧化碳气体,滴入的试剂为氢氧化钠溶液7. 下列实验不能达到预期目的的是A、用肥皂水区别硬水和软水 B、用碘水区别淀粉和蔗糖 C、用酚酞试液区别盐酸和食盐水 D、用点燃法区别聚乙烯和聚氯乙烯8. 下列排列顺序正确的是( )
A、空气中物质的含量:
B、利用金属的年代:
B、利用金属的年代:
C、溶液的pH:
C、溶液的pH: D、铜元素的质量分数:
D、铜元素的质量分数:
9. 下列实验现象描述不正确的( )A、铁丝在氧气中燃烧,火星四射,生成黑色固体 B、铁丝插入盐酸中,有气泡产生,溶液呈黄色 C、红磷在空气中燃烧,产生大量白烟 D、盐酸滴入氢氧化钠溶液中,无明显现象10. 下列指定反应的化学方程式正确的是( )A、铝的自我保护:2Al+3O2═2Al2O3 B、用双氧水制氧气:H2O2 H2↑+O2↑ C、配制波尔多液:CaO+H2O+CuSO4=CaSO4+Cu(OH)2↓ D、小苏打治疗胃酸多:Na2CO3+2HCl═2NaCl+CO2↑+H2O11.
9. 下列实验现象描述不正确的( )A、铁丝在氧气中燃烧,火星四射,生成黑色固体 B、铁丝插入盐酸中,有气泡产生,溶液呈黄色 C、红磷在空气中燃烧,产生大量白烟 D、盐酸滴入氢氧化钠溶液中,无明显现象10. 下列指定反应的化学方程式正确的是( )A、铝的自我保护:2Al+3O2═2Al2O3 B、用双氧水制氧气:H2O2 H2↑+O2↑ C、配制波尔多液:CaO+H2O+CuSO4=CaSO4+Cu(OH)2↓ D、小苏打治疗胃酸多:Na2CO3+2HCl═2NaCl+CO2↑+H2O11.北京市的机动车保有量已超过476万辆,汽车尾气的排放对环境的污染日益严重。
利用四氧化三钴纳米棒作催化剂的催化净化装置,可将汽车尾气中的CO在低温下转化为CO2,过程如图所示。下列说法正确的是( ) A、该催化净化装置能将有毒尾气全部吸收 B、反应前后氧原子个数发生了变化 C、该过程不能说明CO具有可燃性 D、反应物和生成物均为氧化物12. 下列物质的用途与性质对应错误的是( )
A、该催化净化装置能将有毒尾气全部吸收 B、反应前后氧原子个数发生了变化 C、该过程不能说明CO具有可燃性 D、反应物和生成物均为氧化物12. 下列物质的用途与性质对应错误的是( )物质
用途
性质
A
二氧化碳
作气体肥料
二氧化碳既不燃烧也不支持燃烧
B
熟石灰
改良酸性土壤
熟石灰能与酸发生中和反应
C
氮气
用于食品防腐
氮气的化学性质较稳定
D
洗洁精
洗涤油污
洗洁精具有乳化作用
A、A B、B C、C D、D13. 下列物质间的转化,在一定条件不能一步实现的是( )
A、Fe2O3→FeCl2 B、CaO→Ca(OH)2 C、Na2CO3→CaCO3 D、Cu→Cu(NO3)214. 含杂质的Fe2O3固体样品20g,高温下用足量的CO完全还原(杂质不与CO反应),将生成的CO2气体用足量的澄清石灰水充分吸收后,产生30g白色沉淀.则下列说法正确的是( )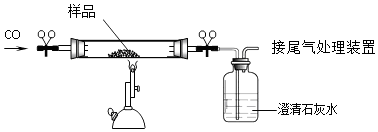 A、通入的CO质量为8.4g B、还原后的固体质量为11.2g C、样品中氧化铁的质量分数为80% D、样品中氧元素质量分数一定为24%15. 下列实验操作中(括号内为待检验物质或杂质)不能达到实验目的是( )
A、通入的CO质量为8.4g B、还原后的固体质量为11.2g C、样品中氧化铁的质量分数为80% D、样品中氧元素质量分数一定为24%15. 下列实验操作中(括号内为待检验物质或杂质)不能达到实验目的是( )选项
物质
目的
主要实验操作
甲
CO、CH4气体
鉴别
点燃,火焰上方罩干冷烧杯,观察现象
乙
Na2CO3(NaOH)溶液
检验
滴加酚酞试液,观察溶液颜色的变化
丙
HCl(H2SO4)固体
除杂
加入适量BaCl2溶液
丁
MnO2、KCl 固体
分离
溶解、过滤、洗涤、烘干、蒸发
A、甲 B、乙 C、丙 D、丁16. 实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线.下列有关该实验事实的说法正确的是( ) A、A点时的溶液不能使酚酞溶液变色 B、该实验是将氢氧化钠溶液滴入盐酸中 C、B点表示盐酸和氢氧化钠溶液恰好完全反应 D、C点时,溶液中溶质只有氯化氢17. 图1是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线,图2是30℃时,取其中两种固体各1g分别放进盛有10g水的两支试管中,充分振荡后的溶解情况,下列说法正确的是( )
A、A点时的溶液不能使酚酞溶液变色 B、该实验是将氢氧化钠溶液滴入盐酸中 C、B点表示盐酸和氢氧化钠溶液恰好完全反应 D、C点时,溶液中溶质只有氯化氢17. 图1是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线,图2是30℃时,取其中两种固体各1g分别放进盛有10g水的两支试管中,充分振荡后的溶解情况,下列说法正确的是( ) A、甲物质的溶解度比乙物质的溶解度大 B、加入试管1的固体是丙 C、向烧杯中加入NH4NO3固体后,试管2中一定有晶体析出 D、将30℃时甲、乙、丙三种物质的饱和溶液降温至20℃,所得溶液中溶质的质量分数的大小关系是乙>甲=丙18. 下列各组稀溶液中,不用其他任何实际就能鉴别出来的是( )A、Na2CO3、HCl、H2SO4、Na2SO4 B、Na2SO4、NaOH、CuSO4、NaCl C、HCl、AgNO3、HNO3、NaCl D、FeCl3、NaOH、HCl、NaCl
A、甲物质的溶解度比乙物质的溶解度大 B、加入试管1的固体是丙 C、向烧杯中加入NH4NO3固体后,试管2中一定有晶体析出 D、将30℃时甲、乙、丙三种物质的饱和溶液降温至20℃,所得溶液中溶质的质量分数的大小关系是乙>甲=丙18. 下列各组稀溶液中,不用其他任何实际就能鉴别出来的是( )A、Na2CO3、HCl、H2SO4、Na2SO4 B、Na2SO4、NaOH、CuSO4、NaCl C、HCl、AgNO3、HNO3、NaCl D、FeCl3、NaOH、HCl、NaCl二、多选题
-
19. 向一定质量的Ba(OH)2溶液中先后滴加CuSO4、H2SO4溶液,过程中加入溶液的质量与产生沉淀的质量关系如图所示.下列说法正确的是( )
 A、a点对应溶液pH>7 B、b点对应溶液中溶质有2种 C、m=3.31 D、取c点对应溶液,滴加NaOH溶液,立刻产生沉淀20. 下图为利用炉甘石(ZnCO3)、赤铜矿(Cu2O)和木炭粉制备黄铜(铜和锌的合金)的生产流程。下列说法正确的是( )
A、a点对应溶液pH>7 B、b点对应溶液中溶质有2种 C、m=3.31 D、取c点对应溶液,滴加NaOH溶液,立刻产生沉淀20. 下图为利用炉甘石(ZnCO3)、赤铜矿(Cu2O)和木炭粉制备黄铜(铜和锌的合金)的生产流程。下列说法正确的是( ) A、操作X的名称是溶解 B、加热过程中发生的反应一定不是化合反应 C、气体A 可能是混合物 D、向黄铜中加入稀盐酸,会产生气泡
A、操作X的名称是溶解 B、加热过程中发生的反应一定不是化合反应 C、气体A 可能是混合物 D、向黄铜中加入稀盐酸,会产生气泡三、填空题
-
21. 用化学符号表示:
(1)锌元素 ;
(2)2个亚铁离子 ;
(3)五氧化二磷 ;
(4)人体缺少 元素会骨质疏松.
22. 光亮的铁丝浸入到硫酸铜溶液中,化学方程式为此反应的类型属于反应.
23.请结合下列实验常用装置,回答有关问题:

(1)写出有关标号仪器的名称a .
(2)实验室制取CO2的方程式为 ,若要获得干燥的二氧化碳,还应选用D装置,并在该装置中盛放(填写试剂名称).如果用E装置收集该气体,则气体从 端进入(填“b”或“c”).
(3)实验室若用块状固体和液体无需加热制取气体,可将B装置改进为C装置(多孔隔板用来放块状固体),其改进后的优点是 .
24. 请从下列物质中选择适当的物质填空(填字母编号):A.熟石灰 B.一氧化碳 C.武德合金 D.硝酸铵 E.硫酸铜 F.肥皂水 G.氢氧化钠 H.纯碱
(1)、制电路保险丝的是;(2)、区分硬水与软水的是;(3)、改良酸性土壤的是;(4)、用于造纸的碱;(5)、配制波尔多液的盐;(6)、溶于水,溶液温度降低的是。25. APEC蓝告别北京后,2014年11月26、29日北京又连续出现严重的雾霾天气,给人们出行带来了严重的影响.此轮雾霾主要由于北京正值采暖季,燃煤排放强度明显高于其他时段,空气中大于PM2.5的颗粒明显增多.PM2.5是指大气中直径小于或等于2.5微米的颗粒物.
(1)、雾霾天气导致呼吸道病人增多,因为这种天气,空气中 大量增加;A.二氧化碳 B.一氧化碳 C.可吸入颗粒物 D.二氧化硫
(2)、防PM2.5专用口罩使用了活性炭的 作用;(3)、请你提出一条防治空气污染的合理建议: .四、实验题
-
26. 我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献。其生产工艺流程示意图如下:
 (1)、粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的① NaOH溶液、② Na2CO3溶液、③ BaCl2溶液及适量的盐酸等除杂、精制。则加入试剂合理的顺序为 (填字母序号)。A、①②③ B、③②① C、①③②(2)、加盐酸的作用是(用方程式表示)、。(3)、制碱原理可看作是由① CO2 + NH3 + H2O = NH4HCO3和② NaCl + NH4HCO3 = NaHCO3+ NH4Cl两个反应加合而成。反应②为复分解反应,请根据复分解反应发生的条件及表1中相关物质20℃时的溶解度,分析反应②为何能顺利进行?。
(1)、粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的① NaOH溶液、② Na2CO3溶液、③ BaCl2溶液及适量的盐酸等除杂、精制。则加入试剂合理的顺序为 (填字母序号)。A、①②③ B、③②① C、①③②(2)、加盐酸的作用是(用方程式表示)、。(3)、制碱原理可看作是由① CO2 + NH3 + H2O = NH4HCO3和② NaCl + NH4HCO3 = NaHCO3+ NH4Cl两个反应加合而成。反应②为复分解反应,请根据复分解反应发生的条件及表1中相关物质20℃时的溶解度,分析反应②为何能顺利进行?。表1 相关物质的溶解度(20℃)(单位:g)
NaCl
NH4HCO3
NaHCO3
NH4Cl
36.0
21.7
9.6
37.2
(4)、操作2为洗涤、煅烧。晶体应在以下装置中(填字母序号)进行“洗涤”操作。
在上述操作中,如何判断晶体已经洗涤干净。
(5)、X的化学式为 , 若X直接排放到空气中会造成的后果是。(6)、Y是滤液中最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为 , Y的化学式为 , 写出Y的一种用途。27. 化学兴趣小组探究金属的性质时,将一段去除氧化膜的镁条,放入一定量的稀盐酸中,有气泡产生,充分反应后静置,发现试管中有灰白色沉淀.【提出问题】
灰白色沉淀是什么物质?
【猜想假设】
小华认为灰白色沉淀为碳酸镁(MgCO3),其他同学认为不需要实验就能否定小华的猜想,理由是 .
小宇认为由于反应后氯化镁的生成量偏多,灰白色沉淀为不能再溶解的氯化镁固体.
小彤认为灰白色沉淀为脱落的镁粉细颗粒.
【实验探究1】
实验操作
现象
结论
①取试管中的上层清液,加入适量的氯化镁固体
氯化镁固体
(选填“溶解”或“不溶解”)
小宇猜想错误
②取适量白色沉淀加入足量稀盐酸中
(选填“有”或“没有”)气泡冒出
小彤猜想错误
基于以上探究与分析,原有猜想均遭到了否定.
【查阅资料】
HCl+AgNO3═HNO3+AgCl↓,AgCl是一种白色沉淀.
【实验探究2】
他们又另取灰白色沉淀放入试管中加热,将蘸有硝酸银溶液的玻璃棒伸入试管内,玻璃棒上的溶液出现白色浑浊,证明产生了气体.再将湿润的蓝色石蕊试纸悬于试管口,试纸变色.
同学们请教老师后得知,足量的镁与稀盐酸反应时,溶液会经历从酸性到碱性且碱性逐步增强的过程,从而生成了碱式氯化镁沉淀.据文献介绍,碱式氯化镁存在多种组成结构,化学通式可表示为Mgx(OH)yClz•mH2O(其中2x﹣y﹣z=0,0≤m≤6).
【反思拓展】
①做镁与稀盐酸反应的实验时,镁条的用量宜少不宜多.
②铁片和铜片放入稀硫酸中产生的现象也不相同,据此推测出铁的活性比铜 . 还可根据铁和硫酸铜溶液的反应来确定这两种金属的活动性强弱,该反应的化学方程式为 .
五、推断题
-
28. 有一包不纯的K2CO3粉末,可能含有Na2CO3、BaSO4、CuCl2、KCl、KNO3、Ca(NO3)2中的一种或几种,为分析含有的杂质,现进行如下实验
(1)取样溶于水,无固体残留,得无色溶液.则粉末中一定不含有 、 、 .
(2)取上述溶液适量,滴加AgNO3溶液,有白色沉淀,再加入足量稀HNO3 , 沉淀部分溶解,则此粉末中一定含有的杂质是 .
(3)为确定Na2CO3是否存在,某同学称取13.8g粉末溶于水,加入足量BaCl2溶液,充分反应生成19.7g沉淀质量,则原粉末中一定含有Na2CO3 . 你认为此结论(选填“是”或“否”)正确.
29.A~F是初中化学中常见的六种物质,其中B、C组成元素相同,C、D、E、F是不同类别的化合物,D和E的溶液均呈碱性,且E可用作建筑材料,它们相互间的关系如图所示,(图中“﹣”表示相连的物质两两之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件已略去)
请回答:
(1)E的化学式 ;C的化学式 .
(2)写出有关反应的化学方程式:
① ;
② .

六、综合题
-
30. p型透明导电化合物CuAlO2具有良好的热电性能,在热电转换领域具有广阔的应用前景.银铜合金广泛用于航空工业,以下为从航空切割废料中回收银并制备CuAlO2的工艺流程.
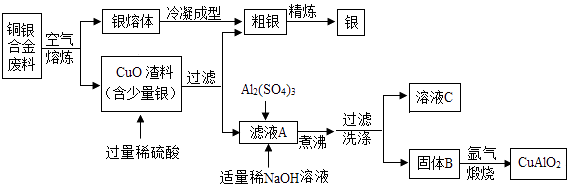
【资料】Ⅰ.难溶性碱受热易分解为两种氧化物,Cu(OH)2、Al(OH)3完全分解的温度分别为80℃和450℃;
Ⅱ.CuAlO2高温易分解、受热易氧化.银在空气中不易被氧化.
请回答下列问题:
(1)、CuAlO2中铜元素的化合价为 , 过滤后所得滤液A中的溶质为 .(2)、煮沸过程中发生反应的化学方程式为 .(3)、固体B在煅烧时发生的其中一个反应方程式为4CuO+2Al2O3 4CuAlO2+X↑,气体X的化学式为 .(4)、“煅烧”时温度须控制在1042﹣1085℃范围内且在氩气中进行,其原因是 .