八年级下册浙教版科学期中测试卷(1.1---3.3)
试卷更新日期:2018-04-19 类型:期中考试
一、单选题
-
1. 绿茶中的单宁酸具有抗癌等功效,其化学式为C76H52O46 , 下列说法不正确的是( )
A、单宁酸由碳、氢、氧三种元素组成 B、单宁酸中有52个氢原子 C、单宁酸分子中碳、氢、氧原子个数比为38∶26∶23 D、一个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成2.探月卫星“嫦娥一号”主要任务之一是探明月球上氦—3的储量。下图是氦—3原子结构示意图,以下说法错误的是( )
 A、氦原子的质子和中子还可分,它们由更小的微粒构成 B、氦—3原子由原子核和核外电子构成 C、氦—3原子核内有2个质子和1个中子 D、在元素周期表中,氦元素的原子序数为33.
A、氦原子的质子和中子还可分,它们由更小的微粒构成 B、氦—3原子由原子核和核外电子构成 C、氦—3原子核内有2个质子和1个中子 D、在元素周期表中,氦元素的原子序数为33.如图所示是硫和铁丝分别在氧气中燃烧的实验示意图。这两个反应( )
 A、都是分解反应 B、都生成气体 C、都放出热量 D、都产生蓝紫色火焰4. 分子和原子的主要区别是( )A、分子是构成物质的微粒,原子不是构成物质的微粒 B、分子由原子构成,所以分子的质量都大于原子质量 C、分子在不停地运动,原子在分子中不可能运动 D、分子在化学反应中可分,原子在化学反应中不可再分5. 氖气是一种稀有气体,若以●表示氖原子,则氖气可用下列( )模型表示A、
A、都是分解反应 B、都生成气体 C、都放出热量 D、都产生蓝紫色火焰4. 分子和原子的主要区别是( )A、分子是构成物质的微粒,原子不是构成物质的微粒 B、分子由原子构成,所以分子的质量都大于原子质量 C、分子在不停地运动,原子在分子中不可能运动 D、分子在化学反应中可分,原子在化学反应中不可再分5. 氖气是一种稀有气体,若以●表示氖原子,则氖气可用下列( )模型表示A、 B、
B、 C、
C、 D、
D、 6. 3•15晚会曾报道了一些制药企业的药用胶囊中重金属“铬”含量严重超标。“铬”在人体内蓄积具有致癌性并可能诱发基因病变。这里的“铬”是指 ( )
6. 3•15晚会曾报道了一些制药企业的药用胶囊中重金属“铬”含量严重超标。“铬”在人体内蓄积具有致癌性并可能诱发基因病变。这里的“铬”是指 ( )
A、 金属铬 B、铬元素 C、铬离子 D、铬原子7. 金属钛(Titanium)是航空、军工、电力等方面的必需材料,因为具有奇特的性能,被誉为“未来金属”。金属钛的元素符号是 ( )A、Ti B、TI C、ti D、tI8.如下图所示,有关测电笔的使用,下列说法正确的是( )
 A、氖管发光时测电笔接触的是零线 B、使用时手可以接触测电笔的任何部位 C、氖管发光时测电笔接触的是火线 D、测电笔与手接触的部分都是绝缘体9. 如左图所示,一根条形磁体左端为N极,右端为S极.下图所示的是从N极到S极磁性强弱变化情况,其中正确的是( )A、
A、氖管发光时测电笔接触的是零线 B、使用时手可以接触测电笔的任何部位 C、氖管发光时测电笔接触的是火线 D、测电笔与手接触的部分都是绝缘体9. 如左图所示,一根条形磁体左端为N极,右端为S极.下图所示的是从N极到S极磁性强弱变化情况,其中正确的是( )A、 B、
B、 C、
C、 D、
D、 10. 以下描述两个磁极间的磁感线分布图中,正确的是( )A、
10. 以下描述两个磁极间的磁感线分布图中,正确的是( )A、 B、
B、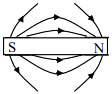 C、
C、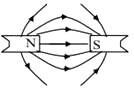 D、
D、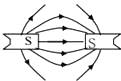 11. 按下列装置实验,能达到对应目的是( )
11. 按下列装置实验,能达到对应目的是( ) A、①② B、②③ C、③④ D、①④12. 有碳酸钙和氧化钙的混合物16g,其中含钙元素的质量分数为50%,与一定量某浓度的稀盐酸恰好完全反应,得到不饱和溶液157.2g,则所加稀盐酸的溶质质量分数为( )
A、①② B、②③ C、③④ D、①④12. 有碳酸钙和氧化钙的混合物16g,其中含钙元素的质量分数为50%,与一定量某浓度的稀盐酸恰好完全反应,得到不饱和溶液157.2g,则所加稀盐酸的溶质质量分数为( )
A、7.3% B、10% C、14.6% D、20%13. 在一定的条件下,向一密闭的容器内加入A,B,C,D四种物质各20g,充分反应后,测定其质量,得到数据如表:物 质
A
B
C
D
反应前质量(g)
20
20
20
20
反应后质量(g)
20
30
未知
14
下列说法不正确的是( )
A、其化学方程式为:2C+3D=5B B、物质A可能是该反应的催化剂 C、容器内发生了化合反应 D、反应后容器内C的质量为16g14. 已知某石灰石(主要含CaCO3)中碳元素的质量分数为9%(杂质中不含有碳元素),则该石灰石样品中CaCO3的质量分数是( )
A、12% B、40% C、75% D、90%15. 相对原子质量是一个比值.假设一个C-12原子质量的1/12为Mkg,以此为标准时,氧原子的相对原子质量是16。若以原子质量为2Mkg的某种原子作为标准,则氧原子的相对原子质量是( )
A、8 B、16 C、32 D、6416. 某家庭电路中安装有“220 V、5 A”的空气开关(未画出),下图是电路中的四种情况,开关全部闭合后,不会引起空气开关“跳闸”的是( )
A、 B、
B、 C、
C、 D、
D、 17.
17.下图形象地表示了氯化钠的形成过程。下列相关叙述中正确的是( )
 A、钠原子失去一个电子形成阳离子,氯原子得到一个电子形成阴离子 B、钠原子与钠离子都不显电性 C、氯化钠分子由氯原子和钠原子构成 D、钠原子与钠离子的微观结构相同18.
A、钠原子失去一个电子形成阳离子,氯原子得到一个电子形成阴离子 B、钠原子与钠离子都不显电性 C、氯化钠分子由氯原子和钠原子构成 D、钠原子与钠离子的微观结构相同18.有人发明了一种“发电地板”,如左下图所示。 发电地板的主要部件由永磁体和线圈组成。行人或车辆通过时,挤压地板使永磁体和线圈发生相对运动,便能发电。 该发电地板的工作原理与下列哪个选项的实验原理相同( )
 A、
A、 B、
B、 C、
C、 D、
D、
二、填空题
-
19. Mg和Mg2+因具有相同的质子数,故属于同种元素,又因为它们具有不同的数,故属于两种不同的微粒。
20. 科学家曾通过测定古生物遗骸中碳-14含量来推断古生物的年代,已知碳-14原子的核电荷数为6,相对原子质量为14,则碳-14原子的原子核内有个中子,原子核外有个电子。
21. C3N4是一种新型材料,它的硬度比金刚石还大,可用作切割工具。在C3N4中C元素的化合价为+4,则N元素的化合价是 。
22. 用元素符号表示:
(1)、氧气
(2)、金属铜
(3)、硝酸铵
(4)、3个钙离子
23. 我国使用的燃料主要是煤炭和石油,产生的SO2遇到雨水成为酸雨.目前有一种较有效的方法,即用直升飞机喷洒碳酸钙粉末,脱硫效果可达85%,碳酸钙与SO2及空气中的氧反应生成硫酸钙和二氧化碳,写出化学方程式 .24. 配平下列化学方程式① C+Fe3O4 Fe+CO2↑
② CuSO4+NaOH═ Cu(OH)2↓+Na2SO4 .
25.如下图,闭合开关S,通电螺线管右侧的小磁针静止时,小磁针的N极指向左。则通电螺线管的左端为极,电源的右端为极。
 26.
26.氧气能与许多物质发生反应。小明同学学习了之后进行了如图整理。(部分反应条件已略去)。
 (1)、反应①硫在点燃的情况下伸入盛有氧气的集气瓶中,则生成物X的化学式为。
(1)、反应①硫在点燃的情况下伸入盛有氧气的集气瓶中,则生成物X的化学式为。
(2)、在反应③实验时,要预先在盛放氧气的集气瓶中放少量水或细沙子,其目的是。
(3)、由图可知氧气是化学性质比较(填“稳定”或“活泼”)的气体。27. 碘是由碘分子构成的非金属,某同学利用碘进行了如下的实验:①把少量的固体碘放在湿润的馒头上,发现馒头会变蓝色。
②再取少量的碘溶解在酒精中,将碘酒滴在馒头上,发现馒头也会变蓝色。请回答下列问题。
(1)、从微观角度分析,是保持碘化学性质的最小微粒 。(2)、取少量的碘放入烧杯中,用酒精灯加热,碘升华变成碘蒸气,把湿润的馒头放在碘蒸气中,馒头 (填“会”或“不会”)变蓝色。(3)、现在市场上买来的食盐大都是加碘盐,根据您的生活经验推测,加碘食盐中(填“存在”或“不存在”)碘分子。三、实验探究题
-
28.
卢瑟福用a粒子(α粒子是带两个单位正电荷的氦原子核)轰击金箔的实验,推翻了汤姆生在1903年提出的原子结构模型,为建立现代原子理论打下了基础,但通过该实验的下述三种现象(如图),不能获得核外电子带有负电荷的结论。
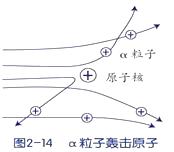
现象1:大多数α粒子能穿透金箔而不改变原来运动方向。
现象2:一小部分α粒子改变原来的运动方向。
现象3:极少数α粒子被弹了回来。
(1)、请你根据原子结构知识分析以上现象产生的原因。①现象1的原因:
②现象2的原因:
(2)、1919年,卢瑟福用加速了的高能α粒子轰击氮原子,结果有种微粒从氮原子被打出,而α粒子留在了氮原子中,使氮原子变成了氧原子,从现代观点看,被打出的微粒一定是 。
29. 磁感应强度表示磁场的强弱,用字母B表示,国际单位是特斯拉,符号是T。磁感应强度B越大,磁场越强。磁感线能形象、直观地描述磁场,磁感线越密,磁场越强。请据此知识回答下列问题:
(1)、用某种材料制成的磁敏电阻,其阻值R随磁感应强度B变化的图像如图甲所示。由图像可知磁敏电阻的阻值随磁感应强度B的增大而。图中的图像没过坐标原点是因为 。
 (2)、将该磁敏电阻接入图丙所示的电路中,电源电压保持不变,不改变滑动变阻器滑片的位置,仅将磁敏电阻由图乙所示的1位置移至2位置,则电流表的示数将。30.
(2)、将该磁敏电阻接入图丙所示的电路中,电源电压保持不变,不改变滑动变阻器滑片的位置,仅将磁敏电阻由图乙所示的1位置移至2位置,则电流表的示数将。30.为“测定空气里氧气体积含量”,小明同学取足量的红磷、镁条、木炭分别在等体积的A、B、C三瓶空气中同时燃烧;充分燃烧后恢复到常温再松开止水夹,发现集气瓶B中进水最多,C中进入水量很少。查阅资料:镁条既能与氧气反应生成氧化镁固体,还能与氮气反应生成

氮化镁(Mg3N2)固体。
(1)、实验中发现水停止倒吸后,B集气瓶中的水量明显高于A瓶的原因是 。
(2)、实验室中若用图A装置测定空气中氧气的体积分数,下列说法正确的是( )A.红磷一熄灭就可以打开夹子 B.实验中,水的量可以随意
C.红磷的量要足量 D.瓶中消耗掉的气体跟剩下的气体的体积比为1:4
31. 通过初中科学的学习,我们知道实验室有多种途径可以制取氧气。如:A. 过氧化氢溶液和二氧化锰 ;B. 加热氯酸钾和二氧化锰混合物 ;C. 加热高锰酸钾 。
(1)、从节能、环保的角度考虑,实验室制取氧气最好选用(选填字母)作反应物。
(2)、如下图是常用的气体发生装置和收集装置。若用装置A、C加热高锰酸钾制取氧气。实验结束时,发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是 ;
 (3)、一氧化氮是汽车尾气中的一种大气污染物,它是无色气体,难溶于水,密度比空气略大,常温下能与空气中的氧气迅速反应生成红色的二氧化氮气体,若要收集一瓶一氧化氮气体应选用的装置是。(选填字母)
(3)、一氧化氮是汽车尾气中的一种大气污染物,它是无色气体,难溶于水,密度比空气略大,常温下能与空气中的氧气迅速反应生成红色的二氧化氮气体,若要收集一瓶一氧化氮气体应选用的装置是。(选填字母)
32.在探究“影响电磁铁磁性强弱的因素”实验中,小明制成电磁铁甲、乙,并设计了如图所示的电路。
 (1)、根据图示的情境可知,其他条件不变时,越多,电磁铁磁性越强。
(1)、根据图示的情境可知,其他条件不变时,越多,电磁铁磁性越强。
(2)、当滑动变阻器滑片向左移动时,电磁铁甲、乙吸引大头针的个数都会增加,由此可得出的结论:。四、解答题
-
33. 乙醇俗称酒精.可用作医用消毒,也常作燃料。(1)、乙醇不完全燃烧会产生一氧化碳,实验测得反应前后各物质的质量如下表:
物质
乙醇
氧气
二氧化碳
水
一氧化碳
反应前质量(g)
4.6
8.8
0
0
0
反应后质量(g)
0
0
6.6
a
1.4
①表中a的值为。
②该实验发生反应的化学方程式为: +CO
(2)、乙醇完全燃烧的化学方程式可表示为:求:92g乙醇完全燃烧需消耗多少g氧气?
34.下图是某兴趣小组设计的一恒温箱的原理图。“控制电路”由热敏电阻R1、滑动变阻器R0、电磁铁(线圈电阻不计)、电源U1(U1=8V)、开关、导线等组成。热敏电阻的阻值随温度变化的规律如下表。当线圈中的电流大于或等于20mA时,电磁铁的衔铁被吸下。“工作电路”由电源U2(U2=220V)、发热电阻R2 (R2=110Ω)、导线等组成。

温度/℃
…
30
35
40
45
50
…
热敏电阻阻值/Ω
…
350
300
250
200
160
…
求:
(1)、为使恒温箱温度升高到一定值时,“工作电路”自动断开。则导线端点C最初应接(填A或B)接线柱。(2)、若设定恒温箱的温度最高为45℃,则“控制电路”中的滑动变阻器的阻值为多大?(3)、“控制电路”中用到了哪些科学知识?请说出两点(示例中的除外)。示例:控制电路中用到了“欧姆定律”的科学知识。
35. 食品添加剂是指用于改善食品口味、延长食品保存期甚至增加食品营养成分的一类天然或合成物质,但如果被过度使用,则会危害人的健康。食盐也是一种食品添加剂,其中的Na+既可增加食物的咸味,又是人体必需的无机盐。但卫生机构建议,人体每天钠元素的摄入量不宜超过2.3克。(1)、了解了有关食品添加剂知识后,当你在选购食品时应该 。A.尽量选择加工度低的食品,以免摄入过多的添加剂
B.尽量选择色、香、味俱全的食品,以保证口味
C.多关注食品营养表中添加剂的品种和用量
D.只关注食品的营养成分,不在乎是否含有添加剂
(2)、食盐中钠元素与氯元素的质量比为多少?(3)、如果人体所需的钠元素全部来自食盐,那么,一个人每天食盐的摄入量不宜超过多少克?36. 测电笔中有一个高阻值的电阻,这样可使测电笔测家庭电路(家庭电路的电压为220V)的火线时,加在人体身上的电压在安全电压(36伏)以内。若测电笔氖管发光时的电流为0.2毫安。则:
(1)、测电笔中的高阻值电阻与氖管是 (填“串联”或“并联”)。
(2)、测电笔中的高阻值电阻的电阻不应小于多少欧姆?(不计氖管电阻)