2015-2016学年安徽省蚌埠市固镇县九年级上学期期末化学试卷
试卷更新日期:2016-12-05 类型:期末考试
一、选择题
-
1. 下列生产生活中的变化,属于化学变化的是( )A、冰雪融化
 B、水的净化
B、水的净化 C、燃料燃烧
C、燃料燃烧 D、风力发电
D、风力发电 2. 下列微粒结构示意图中.表示阳离子的是( )A、
2. 下列微粒结构示意图中.表示阳离子的是( )A、 B、
B、 C、
C、 D、
D、 3. 如图表示三种物质在密闭容器中反应前后质量比例的变化,下列说法正确的是( )
3. 如图表示三种物质在密闭容器中反应前后质量比例的变化,下列说法正确的是( ) A、该反应中CaO起催化作用 B、该反应中CO2是生成物 C、该反应是分解反应 D、该反应是化合反应4. 下列关于碳及其氧化物的说法中,正确的是( )A、金刚石、石墨都是碳的单质,其硬度都是很大 B、CO有还原性,可用作冶炼金属 C、CO2可用作燃料 D、CO2通入紫色石蕊溶液,溶液变红,加热后溶液颜色不变5. 如图为元素周期表第4周期的第一部分,据此判断下列说法错误的是( )
A、该反应中CaO起催化作用 B、该反应中CO2是生成物 C、该反应是分解反应 D、该反应是化合反应4. 下列关于碳及其氧化物的说法中,正确的是( )A、金刚石、石墨都是碳的单质,其硬度都是很大 B、CO有还原性,可用作冶炼金属 C、CO2可用作燃料 D、CO2通入紫色石蕊溶液,溶液变红,加热后溶液颜色不变5. 如图为元素周期表第4周期的第一部分,据此判断下列说法错误的是( )26 Fe
铁
55.85
27 Co
钴
58.93
28 Ni
镍
58.69
29 Cu
铜
63.55
A、铁原子中的质子数为26 B、钴的相对原子质量是58.39g C、从左到右元素的原子序数依次增大 D、各元素都属于金属元素6. 如图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球.下列能说明CO2密度大于空气且能与水反应的现象是( )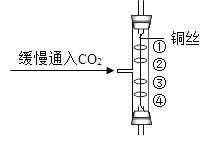 A、①变红,③不变红 B、④变红,③不变红 C、①、④变红,②、③不变红 D、④比①先变红,②、③不变红7. 下列实验操作中的玻璃棒没有起到搅拌作用的是( )A、
A、①变红,③不变红 B、④变红,③不变红 C、①、④变红,②、③不变红 D、④比①先变红,②、③不变红7. 下列实验操作中的玻璃棒没有起到搅拌作用的是( )A、 过滤液体
B、
过滤液体
B、 溶解固体
C、
溶解固体
C、 蒸发溶液
D、
蒸发溶液
D、 稀释浓硫酸
8. 如图为汽车尾气净化装置中发生反应的微观示意图,有关叙述错误的是( )
稀释浓硫酸
8. 如图为汽车尾气净化装置中发生反应的微观示意图,有关叙述错误的是( ) A、该装置可净化汽车尾气 B、图中单质的化学式为N2 C、反应后分子总数减少 D、该反应是置换反应9. 除去下列各物质中的少量杂质,所用试剂、方法正确的是( )
A、该装置可净化汽车尾气 B、图中单质的化学式为N2 C、反应后分子总数减少 D、该反应是置换反应9. 除去下列各物质中的少量杂质,所用试剂、方法正确的是( )选项
物质
杂质
除去杂质的试剂或方法
A
CO2
CO
点燃
B
Fe粉
炭粉
稀盐酸,过滤
C
MnO2
KCl
足量水,过滤
D
CuSO4溶液
FeSO4溶液
过量铁粉,过滤
A、A B、B C、C D、D10. 一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量见表,下列税说法正确的是( )物质
a
b
c
d
反应前物质质量/g
18
1
2
32
反应后物质质量/g
待测
26
2
12
A、待测数据是23 B、参加反应a、d的质量比为4:1 C、该反应的基本类型为化合反应 D、c物质一定是该反应的催化剂二、简答题
-
11. 在“氧气、醋酸、氯化钠、二氧化碳、氮气”中选择适当的物质填空;(1)、可用于医疗急救的是(2)、能使澄清石灰水变浑浊的是(3)、焊接金属常用作保护气的是(4)、除去水壶中的水垢(水垢主要成分是碳酸钙)需用 .12. 如图为自来水厂净水过程示意图.回答下列问题:
 (1)、在这个过程中,未涉及的净水方法是 (填序号)A、过滤 B、沉淀 C、煮沸 D、吸附(2)、水体污染日益严重,造成水体污染的来源主要有工业污染、农业污染和 .(3)、自然界中的水有硬水和软水,常用来区分.(4)、铁酸钠(Na2FeO4)是一种新型净水剂,具有絮凝和杀菌消毒作用.其中Fe元素的化合价为 , 请将下列制取铁酸钠的化学方程式补充完整;
(1)、在这个过程中,未涉及的净水方法是 (填序号)A、过滤 B、沉淀 C、煮沸 D、吸附(2)、水体污染日益严重,造成水体污染的来源主要有工业污染、农业污染和 .(3)、自然界中的水有硬水和软水,常用来区分.(4)、铁酸钠(Na2FeO4)是一种新型净水剂,具有絮凝和杀菌消毒作用.其中Fe元素的化合价为 , 请将下列制取铁酸钠的化学方程式补充完整;2Fe(NO3)3+16NaOH+3Cl2═6NaNO3+6NaCl+2Na2FeO4+
(5)、节约水资源仪成为人类的共识,请举例一种可行的节水方法13. 实验室中各种不同仪器,可以组装成多种不同的装置,结合下列实验装置图回答问题: (1)、实验室用石灰石和稀盐酸反应制取二氧化碳,反应的化学方程式为 , 该反应生成的二氧化碳气体中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的G装置除去氯化氢气体,请从上图装置中选择并组装一套制取干燥纯净的二氧化碳的装置,正确的连接顺序为(用接口处字母填写).要证明CO2不支持燃烧,密度比空气大的性质,你认为(填“H”或“I”)装置操作效果更好.(2)、实验室用氯酸钾和二氧化锰加热制取氧气应选择的制取装置(填装置编号),若用高锰酸钾为原料制取氧气,则需要在试管口处放 , 防止堵塞导管,实验室常用H2O2在二氧化锰催化作用下制取O2 , 其反应的化学方程式是 .14. 在过氧化氢溶液的分解反应中,二氧化锰能作催化剂.(1)、下列有关催化剂的说法正确的是 (填序号).A、在化学反应后其质量减小 B、在化学反应后其化学性质发生了变化 C、能增大生成物的质量 D、能改变化学反应速率(2)、某化学兴趣小组的同学知道二氧化锰能做过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质是否也可作过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白.
(1)、实验室用石灰石和稀盐酸反应制取二氧化碳,反应的化学方程式为 , 该反应生成的二氧化碳气体中常混有少量氯化氢气体,可通过盛有饱和碳酸氢钠溶液的G装置除去氯化氢气体,请从上图装置中选择并组装一套制取干燥纯净的二氧化碳的装置,正确的连接顺序为(用接口处字母填写).要证明CO2不支持燃烧,密度比空气大的性质,你认为(填“H”或“I”)装置操作效果更好.(2)、实验室用氯酸钾和二氧化锰加热制取氧气应选择的制取装置(填装置编号),若用高锰酸钾为原料制取氧气,则需要在试管口处放 , 防止堵塞导管,实验室常用H2O2在二氧化锰催化作用下制取O2 , 其反应的化学方程式是 .14. 在过氧化氢溶液的分解反应中,二氧化锰能作催化剂.(1)、下列有关催化剂的说法正确的是 (填序号).A、在化学反应后其质量减小 B、在化学反应后其化学性质发生了变化 C、能增大生成物的质量 D、能改变化学反应速率(2)、某化学兴趣小组的同学知道二氧化锰能做过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质是否也可作过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白.【提出问题】在过氧化氢溶液的分解反应中,除了二氧化锰,是否有其他物质也能作催化剂?
【查阅资料】在过氧化氢溶液的分解反应中,氧化铜也能作催化剂.
【实验探究】
实验操作
实验现象
实验结论
实验一
有少量气泡
木条不复燃
常温下过氧化氢溶液分解速率很慢.
实验二
在装有过氧化氢溶液的试管中加入少量氧化铜,然后将带火星的木条伸入试管中
在过氧化氢的分解反应中氧化铜改变分解速率
(3)、【得出结论】氧化铜能作过氧化氢分解的催化剂.【反思提高】经过讨论,有的同学认为只有上述实验,不能证明氧化铜能作过氧化氢分解的催化剂,还要补充一个探究实验三:
【实验三目的】探究氧化铜在反应前后质量是否改变.
【实验步骤】①准确称量氧化铜(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤、洗涤、、称量,在过滤实验中使用的玻璃棒一起有烧杯、玻璃棒、;④对比反应前后氧化铜的质量.
(4)、【交流讨论】如果在反应前后氧化铜质量 , 则说明氧化铜可以作过氧化氢分解的催化剂.(5)、【提出新的问题】但还有同学认为,要证明氧化铜能作过氧化氢分解的催化剂,上述三个实验还不准确够,还需要再增加一个探究实验四:【实验四目的】探究 .
(6)、【拓展探究】同学们对二氧化锰和氧化铜对过氧化氢溶液分解的催化作用能力做了更深入的探究,设计如下四组实验进行比较,其中观察效果最差的是 (选填序号)



第一组
第二组
第三组
第四组
A、第一组同时实验,观察比较反应过程中两个气球体积的变化 B、第二组同时实验,观察比较反应过程中两个试管内产生气泡的快慢 C、第三组分两次实验,看木条是否能复燃 D、第四组分两次实验,比较收集一定体积的气体所需要的时间.15. 如图1是某化学课外活动小组设计的探究工业炼铁原理实验,其中A装置的作用是二氧化碳和炭粉在高温下转化为一氧化碳.回答下列问题: (1)、写出装置A玻璃管中发生反应的化学方程式:;(2)、整套装置还有一个明显的不足之处是: .(3)、B中得到的黑色产物W,该活动小组同学根据图2对产物W的成分进行探究.
(1)、写出装置A玻璃管中发生反应的化学方程式:;(2)、整套装置还有一个明显的不足之处是: .(3)、B中得到的黑色产物W,该活动小组同学根据图2对产物W的成分进行探究.【提出问题】黑色粉末W可能是什么呢?
【查阅资料】
①铁的氧化物有氧化铁,氧化亚铁和四氧化三铁等,其中氧化铁为红棕色,其余都为黑色.
②铁的氧化物中四氧化三铁有磁性,能被磁铁吸引.
③铁的氧化物都难溶于水,却都能与稀盐酸反应而被溶解.
④铁的氧化物通常情况下不与CuSO4溶液反应.
【进行猜想】
①甲同学认为黑色粉末W全部是铁粉.请写出生成铁的化学反应方程式 . 该反应利用了CO的性.
②乙同学认为甲同学的猜想是错误的,理由是 .
③丙同学认为黑色粉末W中不含Fe2O3 , 理由是 . 丙同学提出如下猜想,请你结合所学知识帮他补充完整.
猜想1:黑色粉末W由铁粉和四氧化三铁(Fe2O3)组成;
猜想2:黑色粉末W由铁粉和氧化亚铁(FeO)组成;
猜想3:黑色粉末W由 .
【实验探究】
方案
实验操作
可能的现象
结论
①
取适量黑色粉末W用磁铁吸引
黑色粉末全部被吸引
猜想1正确
②
取适量黑色粉末W用磁铁吸引
黑色粉末部分被吸引
猜想2正确
③
取适量黑色粉末R用加入足量稀盐酸
黑色粉末全部溶解
猜想3正确
④
取适量黑色粉末R用磁铁吸引
猜想3正确
【得出结论】在高温下一氧化碳和氧化铁反应可生成铁、氧化亚铁、四氧化三铁.
【反思提高】
丁同学认为方案②和方案③中得出的结论不正确,其理由是 .
查阅资料知道:
Fe3O4溶于稀盐酸生成FeCl3、FeCl2和水,其反应方程式可表示为
Fe3O4也能溶于稀硝酸(HNO3),反应生成Fe(NO3)3、NO和水,试写出反应的化学方程式 .
三、计算题
-
16. 某石灰水中含有氢氧化钙1.48g,要使石灰水中含有氢氧化钙全部转化为碳酸钙沉淀,生成的沉淀质量是多少?标准状况下需要通入二氧化碳气体体积是多少升?(标准状况下二氧化碳气体的密度是1.96g/L)