人教版高中化学选修五 第三章第一节:醇 酚
试卷更新日期:2018-04-13 类型:同步测试
一、单选题
-
1. 酒后驾车是引起交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是橙色的酸性K2Cr2O7水溶液遇乙醇迅速生成绿色的Cr3+。下列对乙醇的描述与此测定原理有关的是( )
①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧衍生物
A、②④ B、②③ C、①③ D、①④2. 下列有关乙烯气体和乙醇蒸气的说法正确的是( )A、等物质的量完全燃烧消耗等量的氧气 B、分子中所有的原子都处于同一个平面上 C、能相互转化且反应属于可逆反应 D、可用酸性高锰酸钾溶液鉴别3. 下列物质中可使酸性高锰酸钾溶液褪色,不能使溴水褪色的是( )A、甲烷 B、乙烯 C、乙醇 D、苯4. 发生催化氧化反应后,产物是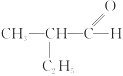 的醇是( ) A、
的醇是( ) A、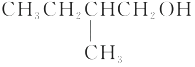 B、
B、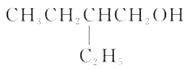 C、
C、 D、
D、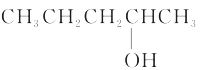 5. 19.己烯雌酚(结构简式如下图所示),是一种激素类药物。下列叙述不正确的是( )
5. 19.己烯雌酚(结构简式如下图所示),是一种激素类药物。下列叙述不正确的是( ) A、己烯雌酚的分子式为C18H20O2 B、己烯雌酚与NaOH溶液、NaHCO3溶液均能反应 C、1 mol己烯雌酚最多能与2mol Na发生反应 D、己烯雌酚与饱和溴水可以发生加成反应和取代反应6. 下列物质中,不能与金属钠反应生成气体的是( )A、CH3CH2OH B、CH3CH3 C、CH3COOH D、
A、己烯雌酚的分子式为C18H20O2 B、己烯雌酚与NaOH溶液、NaHCO3溶液均能反应 C、1 mol己烯雌酚最多能与2mol Na发生反应 D、己烯雌酚与饱和溴水可以发生加成反应和取代反应6. 下列物质中,不能与金属钠反应生成气体的是( )A、CH3CH2OH B、CH3CH3 C、CH3COOH D、 7. 下列关于苯酚的叙述中不正确的是( )A、苯酚显弱酸性,它能与氢氧化钠溶液反应 B、在苯酚钠溶液中通入二氧化碳气体,可得到苯酚 C、除去苯中混有的少量苯酚,可用溴水作试剂 D、苯酚有毒,但药皂中掺有少量苯酚8. 用16g某饱和一元醇跟足量金属钠完全反应,产生5.6L氢气(标准状况),该醇是( )A、甲醇 B、乙醇 C、丙醇 D、丁醇9. 下列各醇,能发生催化氧化反应生成醛,同时可发生消去反应的是( )A、CH3OH B、(CH3CH2)2CHCH2OH C、(CH3CH2)3CCH2OH D、(CH3CH2)3COH10. 已知:CH3CH2CH2CH2OH CH3CH2CH2CHO
7. 下列关于苯酚的叙述中不正确的是( )A、苯酚显弱酸性,它能与氢氧化钠溶液反应 B、在苯酚钠溶液中通入二氧化碳气体,可得到苯酚 C、除去苯中混有的少量苯酚,可用溴水作试剂 D、苯酚有毒,但药皂中掺有少量苯酚8. 用16g某饱和一元醇跟足量金属钠完全反应,产生5.6L氢气(标准状况),该醇是( )A、甲醇 B、乙醇 C、丙醇 D、丁醇9. 下列各醇,能发生催化氧化反应生成醛,同时可发生消去反应的是( )A、CH3OH B、(CH3CH2)2CHCH2OH C、(CH3CH2)3CCH2OH D、(CH3CH2)3COH10. 已知:CH3CH2CH2CH2OH CH3CH2CH2CHO利用如图装置用正丁醇合成正丁醛.相关数据如表:
物质
沸点/℃
密度/(g•cm﹣3)
水中溶解性
正丁醇
117.2
0.8109
微溶
正丁醛
75.7
0.8017
微溶
下列说法中,不正确的是( )
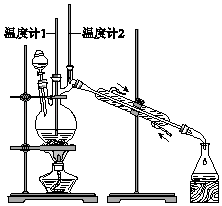 A、为防止产物进一步氧化,应将酸化的Na2Cr2O7溶液逐滴加入正丁醇中 B、当温度计1示数为90~95℃,温度计2示数在76℃左右时,收集产物 C、反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出 D、向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇
A、为防止产物进一步氧化,应将酸化的Na2Cr2O7溶液逐滴加入正丁醇中 B、当温度计1示数为90~95℃,温度计2示数在76℃左右时,收集产物 C、反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出 D、向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇二、填空题
-
11. 把卷成螺旋状的铜丝在酒精灯外焰上加热,使表面变黑,然后迅速伸到无水酒精中,有什么现象铜丝在反应中起的作用,写出这个反应的化学方程式 .12. 如图所示的操作和实验现象,能验证苯酚的两个性质.则:
 (1)、性质Ⅰ是 , 操作1是 , 操作2是 .(2)、性质Ⅱ是 , 操作1是 , 操作2是 .(3)、写出所发生反应的化学方程式: , .
(1)、性质Ⅰ是 , 操作1是 , 操作2是 .(2)、性质Ⅱ是 , 操作1是 , 操作2是 .(3)、写出所发生反应的化学方程式: , .三、实验探究题
-
13. 乙烯是重要的化工原料,可制备很多有机物.实验室制取乙烯的装置如图所示:
 (1)、①实验室制取乙烯的化学反应方程式为;②此反应属于反应;烧瓶中加入碎瓷片的作用是(2)、某化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了下图实验装置,以确认上述混合气体中有C2H4和SO2 . 回答下列问题:
(1)、①实验室制取乙烯的化学反应方程式为;②此反应属于反应;烧瓶中加入碎瓷片的作用是(2)、某化学课外兴趣小组学生在实验室里制取的乙烯中常混有少量的二氧化硫,老师启发他们并由他们自己设计了下图实验装置,以确认上述混合气体中有C2H4和SO2 . 回答下列问题:①Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放不同的试剂,其中:
Ⅰ是Ⅳ是(填试剂的序号)
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
②能说明SO2气体存在的现象是
③确定含有乙烯的现象是
(3)、实践中可以根据原子核磁共振谱(PMR)中观察到的氢原子给出的峰情况,确定有机物的结构.用核磁共振谱的方法来研究C2H6O的结构,若峰面积比为(填比值),则为CH3CH2OH;若只有一个峰,则为CH3OCH3 .
(4)、由乙醇可制取乙酸乙酯,书写有关反应方程式(注明反应条件):①由乙醇催化氧化制乙醛: .
②乙醛与新制Cu(OH)2反应:(产物酸化后得乙酸).
③乙酸与乙醇制乙酸乙酯: .
四、综合题
-
14. 为了确定乙醇分子的结构简式是CH3—O—CH3还是CH3CH2OH,实验室利用如图所示的实验装置,测定乙醇与钠反应(ΔH<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。试回答下列问题:
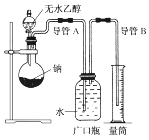 (1)、指出实验装置中的错误:。(2)、若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将(填“偏大”“偏小”或“不变”)。(3)、请指出能使该实验安全、顺利进行的关键实验步骤(至少指出两个关键步骤)
(1)、指出实验装置中的错误:。(2)、若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将(填“偏大”“偏小”或“不变”)。(3)、请指出能使该实验安全、顺利进行的关键实验步骤(至少指出两个关键步骤)。
15. 为探究乙烯与溴的加成反应,某小组同学用浓硫酸和乙醇制取的气体通入溴水中,发现溶液褪色.甲同学认为乙烯与溴水发生了加成反应;乙同学发现褪色后的溶液中有硫酸根离子,推测在制得的乙烯中还可能有少量还原性气体杂质,由此他提出必须先除去杂质,再与溴水反应.请回答:(1)、甲同学认为溴水褪色的主要方程式为;(2)、该小组同学设计的实验(填“能”或“不能”)验证乙烯与溴水发生加成反应,理由是;A.使溴水褪色反应未必是加成反应B.使溴水褪色反应就是加成反应
C.使溴水褪色的物质未必是乙烯D.使溴水褪色的物质就是乙烯
(3)、乙同学推测乙烯中必定含有的一种气体是SO2 , 可以用来验证,SO2与溴水反应的化学方程式是;(4)、为验证这一反应是加成而不是取代,丙同学提出可用pH试纸来测试反应后溶液的酸性,理由是 .16.某市拟投资建设一个工业酒精厂,目的是用工业酒精与汽油混合制成“乙醇汽油”,以节省石油资源,减少大气污染.已知制酒的方法有三种:
①在催化剂作用下乙烯与水反应
②CH3CH2Br+H2O
 CH3CH2OH+HBr
CH3CH2OH+HBr③(C6H10O5)n(淀粉)+nH2O
 nC6H12O6(葡萄糖)
nC6H12O6(葡萄糖)C6H10O6(葡萄糖)
 2C2H5OH+2CO2↑(1)、方法①反应的化学方程式是 .反应类型为 ,方法②的化学反应类型是(2)、为缓解石油短缺带来的能源危机,你认为该市应选用哪一种方法生产工业酒精?请简述理由(3)、如果从绿色化学(“原子利用率”最大化)的角度看,制酒精最好的一组方法是 (填序号)
2C2H5OH+2CO2↑(1)、方法①反应的化学方程式是 .反应类型为 ,方法②的化学反应类型是(2)、为缓解石油短缺带来的能源危机,你认为该市应选用哪一种方法生产工业酒精?请简述理由(3)、如果从绿色化学(“原子利用率”最大化)的角度看,制酒精最好的一组方法是 (填序号)A.①B.③C.①③D.①②③
-