2015-2016学年山东省淄博市沂源县八年级下学期期末化学试卷(五四学制)
试卷更新日期:2016-12-02 类型:期末考试
一、选择题
-
1. 下列变化过程属于物理变化的是( )A、牛奶变质 B、石油分馏 C、葡萄酿酒 D、煤的液化2. 李克强总理在2015年3月5日两会《政府工作报告》中强调:打好节能减排和环境治理攻坚战;要求今年二氧化碳排放强度要降低3.1%以上.下列说法或做法不符合“低碳减排,绿色生活”理念的是( )A、日常生活提倡用布袋代替塑料袋 B、公交出行,少用私车 C、为便于使用,电脑一直处于待机状态 D、随手关灯,节约用电3. 成语“釜底抽薪”的本意包含着灭火的原理,下列灭火方法也依据这个原理的是( )A、砍掉树木形成隔离带 B、用二氧化碳灭火器灭火 C、用锅盖盖灭着火的油锅 D、消防队员用高压水枪灭火4. 化学反应前后肯定没有变化的是( )
①原子的数目 ②分子的数目 ③元素的种类④参加化学反应各物质的质量总和 ⑤物质种类 ⑥原子的种类.
A、①④⑥ B、①③⑤ C、①③④⑥ D、①③④⑤⑥5. 氢氟酸(HF)对玻璃有腐蚀作用,可用在玻璃上雕刻各种精美图案,也可用在玻璃仪器上标注刻度及文字.氢氟酸与玻璃发生的反应可以表示为:SiO2+4HF═X↑+2H2O,关于物质X的组成,下列说法正确的是( )A、可能含有氢元素 B、可能含有氧元素 C、一定含有硅元素、氟元素 D、X是一种氧化物6. 下列属于二氧化碳在自然界中消耗途径的是( )A、植物呼吸作用 B、植物光合作用 C、海水释放 D、化石燃料燃烧7. 下列场所必须张贴如图所示的标志是( )①煤矿;②液化气站;③加油站;④面粉厂;⑤纺织厂;⑥化工厂.
 A、①②③④ B、②③④⑤⑥ C、①②④⑤⑥ D、全部8. 化学方程式不能提供的信息是( )A、化学反应的速度快慢 B、在什么条件下发生反应 C、各物质之间的质量比 D、哪些物质参加反应9. 质量守恒定律是研究和学习化学的重要依据之一.下列现象能够用质量守恒定律解释的是( )A、湿衣服在太阳下晾干 B、50mL水和50mL酒精混合后的混合液体积小于100mL C、铁丝在氧气中燃烧后生成物的质量增大了 D、20g食盐溶于80g水中后,得到100g食盐水10. 我国有在元宵节燃放孔明灯(如图)祈福的风俗,孔明灯燃气的火焰温度可达300℃,但纸质(着火点约170℃)灯罩却没被点燃.原因是( )
A、①②③④ B、②③④⑤⑥ C、①②④⑤⑥ D、全部8. 化学方程式不能提供的信息是( )A、化学反应的速度快慢 B、在什么条件下发生反应 C、各物质之间的质量比 D、哪些物质参加反应9. 质量守恒定律是研究和学习化学的重要依据之一.下列现象能够用质量守恒定律解释的是( )A、湿衣服在太阳下晾干 B、50mL水和50mL酒精混合后的混合液体积小于100mL C、铁丝在氧气中燃烧后生成物的质量增大了 D、20g食盐溶于80g水中后,得到100g食盐水10. 我国有在元宵节燃放孔明灯(如图)祈福的风俗,孔明灯燃气的火焰温度可达300℃,但纸质(着火点约170℃)灯罩却没被点燃.原因是( ) A、灯罩的材料不是可燃物 B、灯罩没有与氧气充分接触 C、风将热全吹散后纸质灯罩的着火点降低了 D、风将热量吹散使纸质灯罩处温度低于纸的着火点11. 下列关于燃烧与灭火的说法中,正确的是( )
A、灯罩的材料不是可燃物 B、灯罩没有与氧气充分接触 C、风将热全吹散后纸质灯罩的着火点降低了 D、风将热量吹散使纸质灯罩处温度低于纸的着火点11. 下列关于燃烧与灭火的说法中,正确的是( )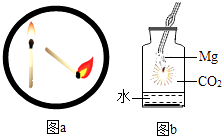 A、将大块煤粉碎后再燃烧,其目的是延迟煤燃烧的时间 B、如图a,火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点 C、由图b中的现象可知,金属镁引起的火灾不能用二氧化碳灭火 D、蜡烛用扇子一扇即灭,是因为闪走了蜡烛周围的空气12. “生命可贵,安全第一”下列采取的安全措施错误的是( )A、晚上煤气泄漏,立即开窗通风 B、点燃氢气前,应先检验氢气的纯度 C、用煤炉取暖,在煤炉上放一壶水以防止煤气中毒 D、进入久未开启的菜窑,先用蜡烛做灯火实验13. 李明同学的化学复习笔记本上有如下记录,你认为正确的是( )A、在实验室中不能用排水法收集二氧化碳气体,是因为二氧化碳易溶于水 B、验证质量守恒定律时,必须都在密闭容器内进行 C、二氧化碳能灭火是由于它能降低可燃物的着火点,且密度比空气大 D、配平化学方程式的依据是质量守恒定律14. 纸比煤易点燃的原因是( )A、纸比煤跟空气接触面积大 B、纸比煤着火点高 C、纸比煤着火点低 D、纸比煤密度小15. 下列化学方程式书写正确的是( )A、Mg+O2 MgO2 B、4Fe+3O2 2Fe2O3 C、C+O2 CO2↑ D、2HgO 2Hg+O2↑16. 2014年4月6日凌晨,丽江束河古镇发生火灾.经查明是一家成都冒菜馆的蜂窝煤惹的祸.我国家庭用经过了从“煤球“到“蜂窝煤”的变化,其目的是( )
A、将大块煤粉碎后再燃烧,其目的是延迟煤燃烧的时间 B、如图a,火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点 C、由图b中的现象可知,金属镁引起的火灾不能用二氧化碳灭火 D、蜡烛用扇子一扇即灭,是因为闪走了蜡烛周围的空气12. “生命可贵,安全第一”下列采取的安全措施错误的是( )A、晚上煤气泄漏,立即开窗通风 B、点燃氢气前,应先检验氢气的纯度 C、用煤炉取暖,在煤炉上放一壶水以防止煤气中毒 D、进入久未开启的菜窑,先用蜡烛做灯火实验13. 李明同学的化学复习笔记本上有如下记录,你认为正确的是( )A、在实验室中不能用排水法收集二氧化碳气体,是因为二氧化碳易溶于水 B、验证质量守恒定律时,必须都在密闭容器内进行 C、二氧化碳能灭火是由于它能降低可燃物的着火点,且密度比空气大 D、配平化学方程式的依据是质量守恒定律14. 纸比煤易点燃的原因是( )A、纸比煤跟空气接触面积大 B、纸比煤着火点高 C、纸比煤着火点低 D、纸比煤密度小15. 下列化学方程式书写正确的是( )A、Mg+O2 MgO2 B、4Fe+3O2 2Fe2O3 C、C+O2 CO2↑ D、2HgO 2Hg+O2↑16. 2014年4月6日凌晨,丽江束河古镇发生火灾.经查明是一家成都冒菜馆的蜂窝煤惹的祸.我国家庭用经过了从“煤球“到“蜂窝煤”的变化,其目的是( ) A、增大可燃物的热值 B、增大可燃物与空气的接触面积 C、提高可燃物的着火点 D、提高空气中氧气的含量17. 当代社会几乎离不开化石燃料,关于人类使用化石燃料的“利”与“弊”,下列说法正确的是( )A、只有“利”而无“弊”,因为人类的生活和生产根本就离不开化石燃料,也离不开以化石燃料为原料生产的塑料、橡胶、纤维、药物、化肥、农药等 B、只有“弊”而无“利”,因为化石燃料的燃烧产生许多有害物质,导致气候变暖,酸雨、空气中可吸入颗粒物含量急剧上升 C、“弊”大于“利”,虽然化石燃料为人类提供了能源和物质,但使用化石燃料带来了严重的环境问题 D、“利”大于“弊”,虽然使用化石燃料带来了一定的环境问题,但化石燃料是当今社会重要的能源和物质资源,只要合理利用,就可以趋利避害18. 逻辑推理是化学学习常用的思维方法.以下推理正确的是( )A、化学反应常常伴随着能量的变化,因此有能量变化的都是化学反应 B、含碳元素的物质燃烧会生成二氧化碳,所以燃烧能生成二氧化碳的物质一定含有碳元素 C、水能灭火,所以电脑一旦失火应立即用水浇灭 D、纸张燃烧后余烬的质量比原纸张的质量小,所以该反应不符合质量守恒定律19. 《美国化学会志》报道了中国科学家以二氧化碳和钠在一定条件制得金刚石,其他化学方程式为3CO2+4Na═2X+C(金刚石),则X的化学式为( )A、Na2O2 B、Na2CO3 C、Na2O D、Na4C2O620. 某化合物R与氧气放于密闭的容器中引燃,充分反应后,生成二氧化碳和水.实验测得的反应前后物质质量如表所示.
A、增大可燃物的热值 B、增大可燃物与空气的接触面积 C、提高可燃物的着火点 D、提高空气中氧气的含量17. 当代社会几乎离不开化石燃料,关于人类使用化石燃料的“利”与“弊”,下列说法正确的是( )A、只有“利”而无“弊”,因为人类的生活和生产根本就离不开化石燃料,也离不开以化石燃料为原料生产的塑料、橡胶、纤维、药物、化肥、农药等 B、只有“弊”而无“利”,因为化石燃料的燃烧产生许多有害物质,导致气候变暖,酸雨、空气中可吸入颗粒物含量急剧上升 C、“弊”大于“利”,虽然化石燃料为人类提供了能源和物质,但使用化石燃料带来了严重的环境问题 D、“利”大于“弊”,虽然使用化石燃料带来了一定的环境问题,但化石燃料是当今社会重要的能源和物质资源,只要合理利用,就可以趋利避害18. 逻辑推理是化学学习常用的思维方法.以下推理正确的是( )A、化学反应常常伴随着能量的变化,因此有能量变化的都是化学反应 B、含碳元素的物质燃烧会生成二氧化碳,所以燃烧能生成二氧化碳的物质一定含有碳元素 C、水能灭火,所以电脑一旦失火应立即用水浇灭 D、纸张燃烧后余烬的质量比原纸张的质量小,所以该反应不符合质量守恒定律19. 《美国化学会志》报道了中国科学家以二氧化碳和钠在一定条件制得金刚石,其他化学方程式为3CO2+4Na═2X+C(金刚石),则X的化学式为( )A、Na2O2 B、Na2CO3 C、Na2O D、Na4C2O620. 某化合物R与氧气放于密闭的容器中引燃,充分反应后,生成二氧化碳和水.实验测得的反应前后物质质量如表所示.物质
R
氧气
二氧化碳
水
反应前质量/g
51
96
0
0
反应后质量/g
x
0
88
54
下列说法不正确的是( )
A、R中只含有碳氢元素 B、x的值为5 C、该反应属于氧化反应 D、生成的二氧化碳和水分子个数比为2:3二、理解与应用
-
21. 在人类社会发展过程中,能源起着重要的作用.(1)、天然气的主要成分为(填化学式),它与石油和均属于化石燃料.(2)、石油的炼制能得到很多产品.下列属于石油炼制产品的是(填序号).
①汽油 ②煤油 ③食用酒精
(3)、人们正在利用和开发太阳能、核能及(只填一种)等新能源.22. 学会分类是学习化学的重要方法.在①水;②液化石油气;③空气;④过氧化氢溶液;⑤四氧化三铁;⑥氧气.其中属于混合物的是 , 属于纯净物的是 , 属于单质的是 , 属于化合物的是 , 属于氧化物的是 .23. 为了加深对质量守恒定律的理解,某校化学实验小组以“镁条在空气中燃烧”实验进行了再探究:(1)、镁条在空气中燃烧时观察到的现象是;(2)、根据质量守恒定律,镁条在空气中燃烧后的质量(填“大于”、“等于”或“小于”之一)镁条的质量;原因是 .(3)、化学反应之所以遵循质量守恒定律,从微观上看,是因为 . 24. 如图是某同学设计的实验室验证二氧化碳性质的实验装置图.
24. 如图是某同学设计的实验室验证二氧化碳性质的实验装置图.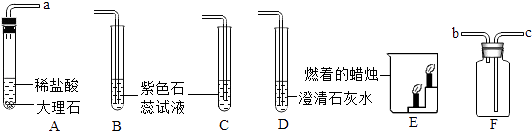
请回答下列问题:
(1)、将A、B装置连接,观察到的现象是 , 反应的化学方程式是;可验证二氧化碳的性质是;将反应后的试管B放在酒精灯上加热一会后观察到的现象是 , 该反应的化学方程式;在实验过程中C装置的作用是 .(2)、将A、D装置连接,可验证二氧化碳与氢氧化钙反应,该反应的实验现象为:、反应的化学方程式是 , 该实验可用来检验气体.(3)、将A、F装置连接可收集一瓶二氧化碳气体,应将A装置的导管a与F装置的导管(选填“b”或“c”)相连接,收集满后,取下双孔橡皮塞,将瓶中的气体沿E装置烧杯左侧内壁缓缓倒入,观察到的现象是 , 这些现象说明二氧化碳具有的物理性质是 , 化学性质是 .25. 已知A、B、C、D、E五种物质之间存在以下的转化关系.其中A、C两种物质的组成元素相同,且常温下都是液态;D是最理想的燃料;E是空气成分,是引起温室效应的主要气体.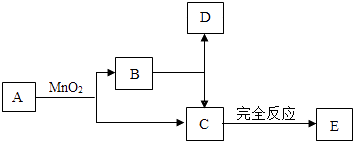
试回答:
(1)、写出C、D两种物质的化学式:C;D;(2)、写出A→B+C的化学方程式:;(3)、D作为最理想的燃料,最突出的优点是;(4)、写出E物质的一种用途 .三、实验与探究
-
26. 结合下列实验常用装置,回答有关问题.
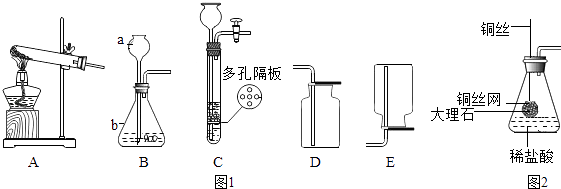 (1)、写出图1中标有字母的仪器的名称:a , b .(2)、实验室用氯酸钾(KClO3)在二氧化锰的催化下加热制取氧气,同时生成氯化钾(KCl)固体,应选用的发生装置;选择该装置的依据是、;写出实验室用氯酸钾固体制取氧气的化学方程式 , 该反应的基本反应类型为 .(3)、比较用过氧化氢溶液和用氯酸钾制取O2的方法,两者的共同点是 (填写编号).A、发生装置相同 B、都可以用MnO2作催化剂 C、反应的基本类型相同 D、完全反应后剩余物质的成分相同(4)、从图1中选择实验室制取二氧化碳的实验装置是;用D装置收集该气体,验满的方法是 .(5)、实验室可以用装置C代替装置B制取气体,该装置的优点是 . 下列反应适用于该装置的是 . (填序号)
(1)、写出图1中标有字母的仪器的名称:a , b .(2)、实验室用氯酸钾(KClO3)在二氧化锰的催化下加热制取氧气,同时生成氯化钾(KCl)固体,应选用的发生装置;选择该装置的依据是、;写出实验室用氯酸钾固体制取氧气的化学方程式 , 该反应的基本反应类型为 .(3)、比较用过氧化氢溶液和用氯酸钾制取O2的方法,两者的共同点是 (填写编号).A、发生装置相同 B、都可以用MnO2作催化剂 C、反应的基本类型相同 D、完全反应后剩余物质的成分相同(4)、从图1中选择实验室制取二氧化碳的实验装置是;用D装置收集该气体,验满的方法是 .(5)、实验室可以用装置C代替装置B制取气体,该装置的优点是 . 下列反应适用于该装置的是 . (填序号)①大理石和稀盐酸制二氧化碳 ②锌粒与稀硫酸制氢气
③过氧化氢溶液与二氧化锰制氧气
有同学设计了如图2所示实验室制取CO2装置,该装置是否具有C装置的作用(填“是”或“否”).
(6)、氨气是一种无色、有刺激性气味的气体,极易溶于水,密度比空气小.实验室常用加热氯化铵和熟石灰固体的方法制取.请写出氨气的一条物理性质 , 实验室制取并收集一瓶氨气的实验装置是(填序号).27. 某化学小组同学利用一下三组装置探究燃烧的条件.查阅资料:①过氧化钠(Na2O2)和碳酸钠(Na2CO3)不燃烧;
②二氧化碳能与过氧化钠在常温下反应,并伴有能量的释放,其反应的化学方程式是2Na2O2+2CO2═2Na2CO3+O2 .
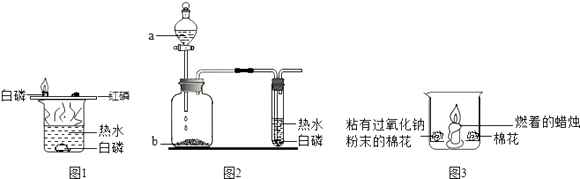 (1)、如图1所示,能燃烧的物质是(填字母序号).B、C两组比较可得出可燃物燃烧的条件是 .
(1)、如图1所示,能燃烧的物质是(填字母序号).B、C两组比较可得出可燃物燃烧的条件是 .A.水中的白磷 B.铜片上的白磷 C.铜片上的红磷
(2)、如图2所示,将液体a滴入瓶中并与固体b接触,能观察到白磷燃烧,则瓶内发生反应的化学方程式为 , 此实验说明了物质燃烧必须 .(3)、如图3所示,在空气中放置时,两团棉花均不燃烧;若将足量二氧化碳倒入烧杯时,可以观察到的现象有:①;②粘有过氧化钠的棉花燃烧;③未粘有过氧化钠的棉花不燃烧.通过上述实验的对比分析,写出产生现象②的原因 .完成三组实验之后,同学成功探究出了燃烧所需要的条件.
四、分析与计算
-
28. 某校化学兴趣小组同学测定大理石样品中碳酸钙的质量分数.准确称量20g大理石样品放入烧杯中,向烧杯中加入100mL过量的稀盐酸(杂质不反应),立即将烧杯放到电子秤上称量,记录数据如下.
时间/min
0
1
2
3
4
5
6
质量/g
170.00
166.00
164.00
163.00
162.40
162.08
162.08
(1)、从表中可知,化学反应速度的变化趋势是 .(2)、计算大理石样品中碳酸钙的质量分数(写出计算过程).