山东省安丘市2017-2018学年九年级上学期化学期末考试试卷
试卷更新日期:2018-04-11 类型:期末考试
一、单选题
-
1. 下列各物质中,属于氧化物的是( )A、食盐 B、冰水混合物 C、液氧 D、氨气2. 下列关于溶液的叙述,正确的是( )A、无色透明的液体一定是溶液 B、溶液中各部分的性质均相同 C、植物油分散到水中可以形成溶液 D、溶液中只能有一种溶质3. 下列客机上使用的物品中,属于合成材料的是( )A、合金门把手 B、真皮椅套 C、塑料快餐盒 D、羊毛毯子4. 联合国确定2017年“世界水日”的宣传主题是“Wastewater(废水)”.我国纪念2017年“世界水日”和“中国水周”活动的宣传主题为“落实绿色发展理念,全面推行河长制”.下列做法正确的是( )
 A、工业废水的任意排放,不会污染水体 B、保护水资源,禁止使用化肥、农药 C、城市浇花使用喷灌、滴灌技术 D、富含氮、磷的生活污水直接排放5. 盛烧碱的试剂瓶上应该贴有下列哪种标志( )A、
A、工业废水的任意排放,不会污染水体 B、保护水资源,禁止使用化肥、农药 C、城市浇花使用喷灌、滴灌技术 D、富含氮、磷的生活污水直接排放5. 盛烧碱的试剂瓶上应该贴有下列哪种标志( )A、 B、
B、 C、
C、 D、
D、 6. 下图是生活中常见洗涤用品的 pH, 混用会降低去污效果的组合是( )
6. 下图是生活中常见洗涤用品的 pH, 混用会降低去污效果的组合是( ) A、洁厕灵和消毒液 B、肥皂水和炉具清洁剂 C、消毒液和肥皂水 D、消毒液和炉具清洁剂7. 如下图向试管里的水中加入某种物质后,原来U型管内两臂在同一水平上的红墨水,右边液面降低了些,左边的液面上升了些,则加入的物质是( )
A、洁厕灵和消毒液 B、肥皂水和炉具清洁剂 C、消毒液和肥皂水 D、消毒液和炉具清洁剂7. 如下图向试管里的水中加入某种物质后,原来U型管内两臂在同一水平上的红墨水,右边液面降低了些,左边的液面上升了些,则加入的物质是( ) A、活性炭 B、生石灰 C、硝酸铵 D、氢氧化钠8. 元素周期表中,硫元素的信息如图所示,从图中获得的信息不正确的是( )
A、活性炭 B、生石灰 C、硝酸铵 D、氢氧化钠8. 元素周期表中,硫元素的信息如图所示,从图中获得的信息不正确的是( ) A、在硫原子的核外电子排布中a=2和b=8 B、一个硫原子的相对原子质量是32.06g C、硫原子在化学反应中易获得2个电子形成硫离子,硫离子中:质子数<电子数 D、硫是非金属元素9. 表格中盐和其用途对应错误的是( )
A、在硫原子的核外电子排布中a=2和b=8 B、一个硫原子的相对原子质量是32.06g C、硫原子在化学反应中易获得2个电子形成硫离子,硫离子中:质子数<电子数 D、硫是非金属元素9. 表格中盐和其用途对应错误的是( )选项
盐
用途
A
含亚硝酸钠的工业盐
制香肠
B
碳酸钙
做补钙剂
C
氯化钠
配制生理盐水
D
碳酸氢钠
做焙制糕点的发酵粉
A、A B、B C、C D、D10. 下列化学实验操作正确的是( )A、 稀释浓硫酸
B、
稀释浓硫酸
B、 检查气密性
C、
检查气密性
C、 过滤
D、
过滤
D、 测定pH
11. 对下列事实解释错误的是( )
测定pH
11. 对下列事实解释错误的是( )选项
事实
解释
A
干冰升华
分子间间隔增大
B
水通电分解
分子在化学变化中可以再分
C
变瘪的乒乓球放入热水中能鼓起来
球内气体分子受热膨胀变大
D
闻到远处花香
分子在不断运动
A、A B、B C、C D、D12. 化学实验过程中要规范操作,注意安全。下列有关做法正确的是( )A、稀硫酸沾到皮肤或衣物上,如果浓度不大,可暂不处理,或用水冲一下即可 B、实验室中的药品经确认无毒无害的,可以品尝一下以感受其味道 C、给烧杯中的液体加热时,烧杯下面垫石棉网 D、称量药品时,为避免药品腐蚀托盘,应将药品放在纸上称量13. 抗病毒处方药磷酸奥可他韦能够有效治疗甲型和乙型流感,分子式为C16H28N2O4•H3PO4下列说法正确的是( )A、分子式中含7种元素 B、C16H28N2O4中C,O元素的质量比为4:1 C、H3PO4由3个氢原子、1个磷原子、4个氧原子构成的 D、H3PO4和H2SO4的相对分子质量相同14. 化学实验中常用到木条或火柴梗,下列实验方案或操作不能达到目的的是( )A、用带火星的木条检验氧气 B、用燃着的木条区分氮气和二氧化碳 C、用木条蘸少量浓硫酸验证浓硫酸有腐蚀性 D、用火柴梗迅速平放蜡烛火焰中,约1s后取出,比较火焰各层温度15. 现有等质量甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价均为+2价).则下列说法中不正确的是( ) A、生成氢气的质量:甲>乙>丙 B、相对原子质量:乙>丙>甲 C、金属活动性:乙>甲>丙 D、消耗硫酸的质量:甲>乙>丙16. 推理是化学学习中常用的思维方法。下列推理正确的是( )A、中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 B、原子核是由质子和中子构成的,所以原子核中都一定含有质子和中子 C、单质一定是由同种元素构成的物质,所以由同种元素组成的物质一定是单质 D、镁、锌、铁能与盐酸反应生成氢气,所以它们与稀硫酸反应也能生成氢气17. 化学实验操作中常常有许多“先后”之分,否则就会出现事故或者使实验失败,下列实验操作的先后顺序不正确的是( )A、实验室制取氧气时,先检查装置的气密性,后装入药品 B、用滴管吸取液体时,先在空气中挤捏胶帽排出空气,后伸入液体中吸取 C、向试管内的加入固体和液体药品时,应先加入固体药品,后加入液体药品 D、用排水法收集氧气时,先熄灭酒精灯,后移出导气管18. 下列根据实验目的所设计的实验方案中,正确的是( )
A、生成氢气的质量:甲>乙>丙 B、相对原子质量:乙>丙>甲 C、金属活动性:乙>甲>丙 D、消耗硫酸的质量:甲>乙>丙16. 推理是化学学习中常用的思维方法。下列推理正确的是( )A、中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 B、原子核是由质子和中子构成的,所以原子核中都一定含有质子和中子 C、单质一定是由同种元素构成的物质,所以由同种元素组成的物质一定是单质 D、镁、锌、铁能与盐酸反应生成氢气,所以它们与稀硫酸反应也能生成氢气17. 化学实验操作中常常有许多“先后”之分,否则就会出现事故或者使实验失败,下列实验操作的先后顺序不正确的是( )A、实验室制取氧气时,先检查装置的气密性,后装入药品 B、用滴管吸取液体时,先在空气中挤捏胶帽排出空气,后伸入液体中吸取 C、向试管内的加入固体和液体药品时,应先加入固体药品,后加入液体药品 D、用排水法收集氧气时,先熄灭酒精灯,后移出导气管18. 下列根据实验目的所设计的实验方案中,正确的是( )选项
实验目的
实验方案
A
除去稀硫酸中的FeSO4
加入适量铁粉
B
除去CO2中的CO
将气体通入NaOH 溶液
C
除去CaCl2溶液中的HCl
加过量CaCO3 , 过滤
D
除去NaCl中的Na2SO4
加过量BaCl2溶液,过滤
A、A B、B C、C D、D19. 甲、乙、丙三种物质的转化关系如右图所示(“→”表示反应一步实现,部分物质和反应条件已略去)。下列选项不能实现图示转化的是( )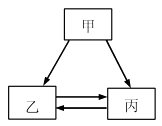
选项
甲
乙
丙
A
H2SO4
H2
H2O
B
C
CO
CO2
C
Ca(OH)2
CaCl2
CaCO3
D
NaOH
NaCl
NaNO3
A、A B、B C、C D、D20. 下列教材课外实验中,发生化学变化的是( )A、 石墨导电实验
B、
石墨导电实验
B、 自制汽水
C、
自制汽水
C、 自制白糖晶体
D、
自制白糖晶体
D、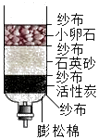 简易净水器
简易净水器
二、填空题
-
21. 根据下列图片信息回答问题:
 (1)、牛奶、鸡蛋富含的营养素是。(2)、食品包装时充氮气其主要目的是。(3)、大豆叶边缘发黄缺少(填化肥种类)肥,该类化肥可增强作物能力。(4)、用洗涤剂洗碗,洗涤剂的作用是。(5)、碘盐中的“碘”是指(选填“元素”、“原子“或“单质”).食用碘盐是为了预防疾病。(填字母)
(1)、牛奶、鸡蛋富含的营养素是。(2)、食品包装时充氮气其主要目的是。(3)、大豆叶边缘发黄缺少(填化肥种类)肥,该类化肥可增强作物能力。(4)、用洗涤剂洗碗,洗涤剂的作用是。(5)、碘盐中的“碘”是指(选填“元素”、“原子“或“单质”).食用碘盐是为了预防疾病。(填字母)a.贫血 b.甲状腺肿大 c.夜盲症
22. 金属在当前科技、生产中应用广泛。(1)、我国自行研发的大型客机选用铝合金做飞机机身而不选用纯铝,主要原因是铝合金硬度和强度(“大于“或小于”) 纯铝。(2)、开采海域“可燃冰”的钻井平台“蓝鲸一号”使用了大量的金属材料。下列措施中哪一项不能有效防止金属锈蚀?__________(填字母序号)A、在金属表面涂油或剧漆 B、制成耐腐蚀的合金 C、打磨掉铝制品表面的氧化膜(3)、某化工厂的废液中主要含有硝酸银、硝酸铜。取一定量的该废液样品,加入铁粉,充分反应后过滤,得到滤液和滤渣。写出铁与硝酸银溶液反应的化学方程式。反应后得到滤液的质量(填“小于”、“大于”或“等于”)反应前所取废液样品的质量。(4)、某钢铁厂每天需消耗4900t 含Fe2O3 76%的赤铁矿石,该厂理论上每天生产含Fe98%的生铁的质量是t。(5)、为比较铝和铁的金属活动性,某同学设计实验方案:将铝和铁分别放入盐酸中,比较反应的剧烈程度。你认为该方案(填“合理”或“不合理”),理由是。三、科学探究题
-
23. 南宋诗人赵师秀有诗“黄梅时节家家雨,青草池塘处处蛙。有约不来过夜半,闲敲棋子落灯花。”诗中“灯花”是蜡烛不完全燃烧产生的炭附着在蜡烛芯上的现象。(1)、现在制造蜡烛的原料是石蜡,石蜡属于(填序号)。
A.无机物 B.有机物 C.纯净物 D.混合物
石蜡工业上来自于石油,利用其中各成分的沸点不同,分离制备得到,此过程中发生的主要变化属于(填“物理”或“化学”) 变化。
(2)、已知石蜡的着火点约为190℃,蜡烛的火焰由气态石蜡燃烧形成。如图所示,在温度计示数为280℃以上时,快速推动活塞,会观察到蜡烛立即熄灭。蜡烛熄灭的主要原因是__________(填序号)。 A、移走可燃物 B、隔绝氧气 C、降低温度至着火点以下(3)、家用石油液化气(主要成分是C3H8、C4H10、C3H6、C4H8) 与石蜡属于同类物质,在空气中充分燃烧生成二氧化碳和水。C4H10中H 的质量分数为 , C4H10燃烧主要是将化学能转化为能;写出C4H10在空气中完全燃烧的化学方程式。24. 学科思想在化学素养发展中起着重要的作用。
A、移走可燃物 B、隔绝氧气 C、降低温度至着火点以下(3)、家用石油液化气(主要成分是C3H8、C4H10、C3H6、C4H8) 与石蜡属于同类物质,在空气中充分燃烧生成二氧化碳和水。C4H10中H 的质量分数为 , C4H10燃烧主要是将化学能转化为能;写出C4H10在空气中完全燃烧的化学方程式。24. 学科思想在化学素养发展中起着重要的作用。(一) 在物质的宏观性质、微观组成(或结构) 和表示符号之间建立联系是化学学科的特点。
 (1)、金刚石和石墨、C60都是由碳元素组成的单质,物理性质上却有很大差异,其原因是。(2)、硅在地壳中储量排在第二位。写出硅原子结构示意图;如图是1表示硅单质制备的微观示意图(如图1)。反应的化学方程式为;反应类型为反应。(3)、(二)图表法是一种常用的数据处理方法。综合所给图表回答下列问题:
(1)、金刚石和石墨、C60都是由碳元素组成的单质,物理性质上却有很大差异,其原因是。(2)、硅在地壳中储量排在第二位。写出硅原子结构示意图;如图是1表示硅单质制备的微观示意图(如图1)。反应的化学方程式为;反应类型为反应。(3)、(二)图表法是一种常用的数据处理方法。综合所给图表回答下列问题:氢氧化钠
碳酸钠
20℃
40℃
20℃
40℃
水
109g
129g
21.8g
49g
酒精
17.3g
40
不溶
不溶
若氢化钠固体中混有少量硝酸钾,提纯氯化钠的方法是(填“降温结晶”或“蒸发结晶”)。
(4)、如图2,现有40℃时等质量的硝酸钾、氯化钠饱和溶液,加热蒸发等质量的水后恢复至40℃,剩余溶液的质量关系大小为硝酸钾氯化钠(填”>”、“=“或“<“)。(5)、40℃时,若将50gNaOH 分别投入到100g水和100g酒精中,能形成饱和溶液的是在中,再将CO2通入所得NaOH的酒精溶液中,观察到的现象为。25. 某实验小组为探究酸的化学性质,由甲、乙、丙同学设计并完成了如图所示的实验。 (1)、甲同学实验中所发生反应的化学方程式为。丙同学实验试管中的反应现象。(2)、【在阅资料】CaCl2、NaCl的溶液是中性,Na2CO3溶液显碱性。
(1)、甲同学实验中所发生反应的化学方程式为。丙同学实验试管中的反应现象。(2)、【在阅资料】CaCl2、NaCl的溶液是中性,Na2CO3溶液显碱性。【实验报究一】确定甲、乙同学上述实验后所得溶液中的溶质。
取甲所得溶液少许,加入石蕊试液,溶液显红色,甲所得溶液中一定含有的溶质是(写化学式)
(3)、取乙所得溶液少许,加入酚酞试液,溶液显红色,乙所得溶液中一定含有的溶质是。(写化学式)(4)、【实验探究二】确定甲、乙同学上述实验所得溶液混合后的成分。甲、乙同学把上述实验所得溶液倒入同一废液缸中,观察到先有气泡产生,后有白色沉淀生成。该白色沉淀是(写化学式).同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究。
(5)、【提出猜想】甲同学猜想NaCl:乙同学猜想:NaCl、CaCl2:丙同学猜想:NaCl、CaCl2、HCl:
你的猜想:。
(6)、【交流讨论】你认为同学的猜想一定不正确,理由是。
(7)、【设计实验】请设计实验证明你的猜想正确。
实验步骤
实验现象
实验结论
取少量滤液于试管中,向其中滴加。
。
猜想成立。
四、实验题
-
26. 下列各图表示初中化学常见的实验装置,回答下列问题:
 (1)、A实验中集气瓶内预先装少量水的目的是。(2)、B 实验中该操作将导致所配溶液溶质质量分数(填“偏大”、“偏小”或“不变”)。(3)、C 实验中玻璃棒的作用是;时停止加热。(4)、仪器①的名称是。E装置正放桌面,用于收集D生成的O2 , 则a接(选填“b”或“c”);E装满水,用于收集D生成的H2 , 则a接(选填“b“或“c”)。(5)、如果要制取和收集干燥的CO2 , 需要在D装置之后连接两个E装置,则在前一个E装置内加入的试剂是。
(1)、A实验中集气瓶内预先装少量水的目的是。(2)、B 实验中该操作将导致所配溶液溶质质量分数(填“偏大”、“偏小”或“不变”)。(3)、C 实验中玻璃棒的作用是;时停止加热。(4)、仪器①的名称是。E装置正放桌面,用于收集D生成的O2 , 则a接(选填“b”或“c”);E装满水,用于收集D生成的H2 , 则a接(选填“b“或“c”)。(5)、如果要制取和收集干燥的CO2 , 需要在D装置之后连接两个E装置,则在前一个E装置内加入的试剂是。五、计算题
-
27. 兴趣小组同学为了测定某中碳酸钙的质量分数,称取25.0g珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
操作次数
第1次
第2次
第3次
第4次
剩余固体质量(g)
21.6
19.2
16.2
16.2
试计算:
(1)、完全反应后生成二氧化碳的质量是g。(2)、求珍珠粉中碳酸钙的质量分数。(写出计算过程)
-