江苏省南京市溧水区2017-2018学年九年级上学期化学期末考试试卷
试卷更新日期:2018-04-08 类型:期末考试
一、单选题
-
1. 我国有关部门规定,自来水中含铁<0.3mg•L-1 , 含铜<1.0mg•L-1 , ……。其中的“铁、铜”指的是( )A、元素 B、分子 C、原子 D、金属单质2. 餐桌上的饮品种类丰富,下列饮品中属于溶液的是( )A、酸奶 B、玉米糊 C、冰水 D、可乐3. 下列物质中,由原子直接构成的是( )A、C60 B、金刚石 C、水 D、硫酸铜4. 下列生活用品用金属材料制作而成的是( )A、陶瓷杯 B、不锈钢碗 C、塑料盆 D、玻璃茶壶5. 下列实验装置或操作正确的是( )A、
 过滤
B、
过滤
B、 处理废弃固体药品
C、
处理废弃固体药品
C、 检查气密性
D、
检查气密性
D、 读液体体积
6. 用分子的相关知识解释生活中的现象,下列说法正确的是( )A、无风的校园中能闻到梅花的芳香说明分子在不断运动 B、压瘪的乒乓球放入热水中重新鼓起是因为分子体积增大 C、分离液态空气制氧气说明分子可以再分 D、冰融化成水,说明分子种类发生改变7. 化学用语是学好化学的工具。下列有关化学用语的说法正确的是( )A、H2O和H2O2中O的化合价相同 B、KMnO4和K2MnO4中有相同的原子团 C、Fe2+和Fe3+都属于铁元素,核外电子数不同 D、
读液体体积
6. 用分子的相关知识解释生活中的现象,下列说法正确的是( )A、无风的校园中能闻到梅花的芳香说明分子在不断运动 B、压瘪的乒乓球放入热水中重新鼓起是因为分子体积增大 C、分离液态空气制氧气说明分子可以再分 D、冰融化成水,说明分子种类发生改变7. 化学用语是学好化学的工具。下列有关化学用语的说法正确的是( )A、H2O和H2O2中O的化合价相同 B、KMnO4和K2MnO4中有相同的原子团 C、Fe2+和Fe3+都属于铁元素,核外电子数不同 D、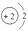 和
和  化学性质相同
8. 下列关于物质用途的叙述不正确的是( )A、用洗洁精洗涤餐桌上的油污 B、用活性炭净水除去水中的色素和异味 C、用硝酸铵溶于水放热的原理为“即食即型快餐”提供热能 D、用干冰营造云雾缭绕的舞台效果9. 发射“神州十一”号飞船的长征2F运载火箭的推进剂是偏二甲肼(C2H8N2)。下列关于偏二甲肼的说法不正确的是( )A、偏二甲肼中氢元素的质量分数最小 B、偏二甲肼中共有10原子 C、偏二甲肼由碳、氢、氮三种元素组成 D、偏二甲肼中碳、氢、氮元素的质量比为6:2:710. 根据铜锈蚀生成铜绿(Cu2(OH)2CO3),某同学猜想:铜锈蚀时除要有氧气和水外, 还必须有二氧化碳参与。为证明铜生锈“必须有二氧化碳参与”,需要进行下图所示实验中的( )
化学性质相同
8. 下列关于物质用途的叙述不正确的是( )A、用洗洁精洗涤餐桌上的油污 B、用活性炭净水除去水中的色素和异味 C、用硝酸铵溶于水放热的原理为“即食即型快餐”提供热能 D、用干冰营造云雾缭绕的舞台效果9. 发射“神州十一”号飞船的长征2F运载火箭的推进剂是偏二甲肼(C2H8N2)。下列关于偏二甲肼的说法不正确的是( )A、偏二甲肼中氢元素的质量分数最小 B、偏二甲肼中共有10原子 C、偏二甲肼由碳、氢、氮三种元素组成 D、偏二甲肼中碳、氢、氮元素的质量比为6:2:710. 根据铜锈蚀生成铜绿(Cu2(OH)2CO3),某同学猜想:铜锈蚀时除要有氧气和水外, 还必须有二氧化碳参与。为证明铜生锈“必须有二氧化碳参与”,需要进行下图所示实验中的( ) A、甲和乙 B、甲和丁 C、乙和丁 D、丙和丁11. 甲和乙反应生成丙和丁的微观示意图如下,下列说法正确的是( )
A、甲和乙 B、甲和丁 C、乙和丁 D、丙和丁11. 甲和乙反应生成丙和丁的微观示意图如下,下列说法正确的是( ) A、该反应前后分子的种类和数目一定不变 B、该反应属于置换反应 C、甲物质中只含有碳、氢两种元素 D、甲的化学式可能为CH2O12. 如下图所示,集气瓶中盛有少量澄清石灰水和一氧化碳,当插入灼热的薄铜片,一会后再用燃着的木条检验剩余气体。有关该实验的叙述不正确的是( )
A、该反应前后分子的种类和数目一定不变 B、该反应属于置换反应 C、甲物质中只含有碳、氢两种元素 D、甲的化学式可能为CH2O12. 如下图所示,集气瓶中盛有少量澄清石灰水和一氧化碳,当插入灼热的薄铜片,一会后再用燃着的木条检验剩余气体。有关该实验的叙述不正确的是( ) A、该实验可验证CO具有可燃性和还原性 B、图B的现象是:受热部分的铜片由亮红色变为黑色 C、图C实验一段时间后振荡,只能观察到澄清石灰水变浑浊的现象 D、图D用燃着的木条点燃瓶中的剩余气体,瓶口可能出现蓝色火焰13. 甲、乙两种不含结晶水的固体物质的溶解度曲线如下图,下列说法中正确的是( )
A、该实验可验证CO具有可燃性和还原性 B、图B的现象是:受热部分的铜片由亮红色变为黑色 C、图C实验一段时间后振荡,只能观察到澄清石灰水变浑浊的现象 D、图D用燃着的木条点燃瓶中的剩余气体,瓶口可能出现蓝色火焰13. 甲、乙两种不含结晶水的固体物质的溶解度曲线如下图,下列说法中正确的是( ) A、甲的溶解度比乙大 B、t1℃时,甲的饱和溶液中溶质与溶液的质量比为1∶5 C、t2℃时,甲、乙的两种饱和溶液中溶质的质量分数相等 D、将等质量甲、乙的两种溶液分别由t3℃降温至t2℃,析出甲的质量一定比析出乙的质量大14. 根据下列实验方案进行实验,能达到相应实验目的的是( )
A、甲的溶解度比乙大 B、t1℃时,甲的饱和溶液中溶质与溶液的质量比为1∶5 C、t2℃时,甲、乙的两种饱和溶液中溶质的质量分数相等 D、将等质量甲、乙的两种溶液分别由t3℃降温至t2℃,析出甲的质量一定比析出乙的质量大14. 根据下列实验方案进行实验,能达到相应实验目的的是( )编号
A
B
C
D
实验
装置




实验
目的
探究燃烧条件之一需要可燃物
探究影响物质溶解性的因素
探究铁钉生锈时O2是否参与反应
比较Zn和Fe的
金属活动性强弱
A、A B、B C、C D、D15. 下列各组物质中,存在如图所示的一步转化关系的是 A、A B、B C、C D、D
A、A B、B C、C D、D二、实验题
-
16. 根据下列装置图回答问题:
 (1)、图1中标号①仪器的名称是:。(2)、实验室制取气体时,组装好仪器后,应先 , 再添加药品。(3)、实验室用石灰石和稀盐酸制取二氧化碳时,应选用的发生装置是(选填图1中的装置序号),该反应的化学方程式为。(4)、实验室制取氢气的化学方程式是。(5)、在制取并用向上排空气法和排水法收集气体的对照实验中,用数字检测仪分别测得二氧化碳体积分数随时间的变化曲线关系图如图2。据图分析,二氧化碳(填“能”或“不能”)用排水法收集。17. 如下图是实验室配制一定溶质质量分数的KNO3溶液的流程图。请回答:
(1)、图1中标号①仪器的名称是:。(2)、实验室制取气体时,组装好仪器后,应先 , 再添加药品。(3)、实验室用石灰石和稀盐酸制取二氧化碳时,应选用的发生装置是(选填图1中的装置序号),该反应的化学方程式为。(4)、实验室制取氢气的化学方程式是。(5)、在制取并用向上排空气法和排水法收集气体的对照实验中,用数字检测仪分别测得二氧化碳体积分数随时间的变化曲线关系图如图2。据图分析,二氧化碳(填“能”或“不能”)用排水法收集。17. 如下图是实验室配制一定溶质质量分数的KNO3溶液的流程图。请回答: (1)、计算:用托盘天平应称量g KNO3。(2)、称量:若称量KNO3固体时指针向左偏转,则应________(填字母),直到天平平衡。A、增加砝码 B、移动游码 C、减少KNO3固体 D、增加KNO3固体(3)、量取:量取水时,应选择(填“10mL”、“50mL”或“100mL”)的量筒。(4)、溶解:若KNO3已结块,为了较快地溶解,合理的方法有(填数字序号)。
(1)、计算:用托盘天平应称量g KNO3。(2)、称量:若称量KNO3固体时指针向左偏转,则应________(填字母),直到天平平衡。A、增加砝码 B、移动游码 C、减少KNO3固体 D、增加KNO3固体(3)、量取:量取水时,应选择(填“10mL”、“50mL”或“100mL”)的量筒。(4)、溶解:若KNO3已结块,为了较快地溶解,合理的方法有(填数字序号)。①将硝酸钾研碎 ②用热水溶解 ③加入更多的水 ④用玻璃棒搅拌
三、简答题
-
18. 金属材料与我们生活息息相关。(1)、从物质分类角度看,合金属于(填“纯净物”或“混合物”)。(2)、将硬铝片和铝片互相刻画,(填“硬铝”或“铝”)片上留下明显划痕。(3)、“辽宁”号航母舰体外壳涂上防锈漆可防止生锈,其原理是。(4)、C919大飞机制造中,用纯铝太软,在铝中加入了少量的锂(Li)等金属熔成合金,这样既轻便,又能增强它的和抗腐蚀性。(5)、锂电池广泛用于手机和笔记本电脑等电子产品中。锂-氯化银电池反应的化学方程式式为:Li+AgCl=LiCl+Ag,可知Li的金属活动性比Ag的(填“强”或“弱”)。(6)、回收利用废旧的铁锅、铝锅的意义是。(答一点即可)(7)、钢是铁的合金。取11.4g钢样,向其中加入足量稀硫酸,产生氢气0.4g(不考虑钢样中其他成分与稀硫酸的反应)。计算此钢样中铁的质量分数(百分数保留一位小数)。19. 2017年5月4日《光明日报》报道了中科院大连化学物理研究所研制出一种新型多功能复合催化剂,首次实现了二氧化碳直接加氢制取高辛烷值汽油。请回答下列问题:(1)、“二氧化碳变汽油”的研究成果,使我国成为此领域的世界领跑者。据此,下列说法正确的是____________________(填字母编号)。A、该成果可有效缓解全球温室效应 B、此技术可减少对化石燃料的依赖 C、该转化过程中没有发生化学变化 D、催化剂对转化起着举足轻重作用(2)、通过如图示意的I、II、III三个环节,将二氧化碳成功转化为汽油。

在一定温度、一定压强和催化剂存在的条件下,环节I除生成CO外,还生成了一种化合物,则反应的化学方程式为。该反应中,氢气夺取了二氧化碳中的部分氧元素,二氧化碳发生了(填“氧化”或“还原”)反应。
(3)、氧化铟是新型多功能复合催化剂的成分之一。元素周期表中,铟(In)元素与铝元素位于同一族,写出氧化铟的化学式。20. 2017年 5月18日,我国在南海进行的可燃冰试采获得成功,中国成为全球最先掌握海底可燃冰试采技术的国家。通过对海底可燃冰矿藏进行降压使可燃冰分解,再通过沙、水、气分离技术获得连续稳定的天然气。(1)、天然气完全燃烧的化学方程式是。(2)、沙、水分离可采用的方法是。(3)、研究表明甲烷的温室效应是CO2的21倍,因此可燃冰开采应注意。四、推断题
-
21. 如下图中的A~I是初中化学中常见的九种物质,是由C、H、O、Fe、Cu五种元素组成的单质或氧化物,其中C、F、H、I为氧化物,且C中氧元素的质量分数为20%;B、H为红色固体;通常D→B是在溶液中发生的反应。图中“—”表示两端的物质间能发生化学反应:“→”表示物质间存在转化关系;部分反应物或生成物已略去。
 (1)、H的化学式为。(2)、F—H反应的化学方程式为: , 该反应的用途是。(3)、写出D→B的化学方程式 , 该基本反应类型是。
(1)、H的化学式为。(2)、F—H反应的化学方程式为: , 该反应的用途是。(3)、写出D→B的化学方程式 , 该基本反应类型是。五、科学探究题
-
22. 镁是20世纪才发展起来的年轻金属,广泛应用于航空、汽车、船舶、通讯电子和国防工业等。兴趣小组同学对金属镁进行了如下探究。
(一)有关金属镁的化学性质探究
兴趣小组同学根据金属的化学性质,知道金属镁能与O2、稀盐酸和CuSO4溶液反应,并设计了如下实验进行验证(以下实验用镁条、镁条均已除去氧化膜)。
(1)、兴趣小组同学把镁粉轻轻洒在酒精灯的火焰上,观察到火焰上跳动闪烁着点点银色火花,如绽放的美丽烟花。该反应的化学方程式是。(2)、兴趣小组同学探究镁与稀盐酸的反应,除观察到预期现象外,还观察到有灰白色沉淀生成的“异常”现象。于是进行了以下探究。【实验1】向4份相同体积与浓度的稀盐酸中分别加入一定长度的某种镁带,现象如下:

【实验结论1】据表分析,是实验出现“异常”的因素之一。
(3)、【实验2】向4份相同体积与浓度的稀硫酸中分别加入一定长度的某种镁带,现象如下:
【实验结论2】对比实验1和实验2,是实验出现“异常”的因素之一。
(4)、兴趣小组同学取一支试管,放入一根镁条,加入一定量硫酸铜溶液,观察到镁条表面有少量气泡产生,且有黑色物质生成。同学们对此实验的现象感到意外和困惑,于是查阅到了相关资料:资料1:硫酸铜溶液在配制时加入了少量稀硫酸;
资料2:当金属粉末颗粒很小时,容易成为黑色;
资料3:生成的黑色物质可能是CuO、Cu中的一种或两种。
①镁条与硫酸铜溶液反应的实验中产生的气体可能为(写化学式)。
②同学们进一步设计实验确定黑色物质的成分,请在下表中补全实验方案。
实验操作
实验现象
结论
将黑色物质过滤、晾干后,分成两份
/
/
将其中一份装入硬质玻璃管中,向其中通入CO后,加热,并将生成的气体通入澄清石灰水中
黑色粉末中
含有CuO
将另一份置于坩埚中,称其质量为m1 , 在空气中加热一段时间后冷却,称其质量为m2
m1m2(填“>”、“<”或“=”)
黑色粉末中
含有Cu
通过以上探究,兴趣小组同学确定了黑色物质为Cu和CuO两种。
(5)、(二)有关镁条表面灰黑色“外衣”组成的探究【发现问题】镁是一种银白色有金属光泽的金属,但久置的镁条总有一层灰黑色的“外衣”,这层灰黑色的“外衣”是什么物质呢?
【查阅资料】
①灰黑色“外衣”的成分是碱式碳酸镁晶体,化学式为:xMgCO3•yMg(OH)2•zH2O;
②Mg(OH)2:白色固体,难溶于水,受热会分解生成两种氧化物;
③MgCO3:白色固体,微溶于水,受热会分解生成两种氧化物;
④相同条件下,Mg(OH)2受热分解的温度比MgCO3分解的温度更低。
【组成测定】为精确测量碱式碳酸镁晶体的组成,兴趣小组同学取4.66g该晶体用热重分析仪对进行加热,使得各成分在不同温度下逐个分解(加热首先失去结晶水),测定剩余固体质量与分解温度之间关系(如下图所示)。

请回答下列问题:
①晶体中结晶水的质量为g。
②t4~t5段中,固体为(写化学式)。
③t5~t6段反应的化学方程式为。
④根据图中数据计算xMgCO3•yMg(OH)2•zH2O中x:y:z =(填最简比)。
-