粤教版化学九年级下册 7.4 结晶现象 同步测试
试卷更新日期:2018-03-28 类型:同步测试
一、单选题
-
1. 将相同质量的甲、乙两种不同溶质的溶液同时蒸发掉10g水,并冷却到T℃时,分别析出2g甲和3g乙物质(均不带结晶水),则下列说法正确的是( )
A、T℃时,甲、乙两种物质的溶解度可能相同 B、T℃时,甲物质的溶解度一定大于乙 C、T℃时,甲物质的溶解度一定小于乙 D、将析出晶体后的甲、乙两种饱和溶液混合后(甲、乙不反应),溶液仍饱和2. 对结晶之后的溶液,下列说法中正确的是( )A、一定是饱和溶液 B、一定是不饱和溶液 C、一定是浓溶液 D、一定是稀溶液3. 2017年4月22日,货运飞船“天舟一号”升入太空和“天宫二号”完成第一次交会对接.高氯酸钾(KClO4)可用作火箭推进剂,如表是高氯酸钾在不同温度时的溶解度.下列说法正确的是( )温度/℃
20
40
60
80
溶解度/g
1.68
3.73
7.3
13.4
A、20℃时高氯酸钾的溶解度为1.68 B、40℃时,将4g高氯酸钾溶于100g水可得到104g溶液 C、80℃的高氯酸钾饱和溶液冷却至40℃有结晶现象 D、高氯酸钾的溶解度随温度升高而减小4. 如图为a、b、c三种物质的溶解度曲线,等质量的a、b、c三种物质的饱和溶液温度由50℃降为30℃,析出晶体最多的是( )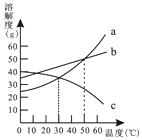 A、a B、b C、c D、a和b5. 下列实验操作图示不正确的是( )A、
A、a B、b C、c D、a和b5. 下列实验操作图示不正确的是( )A、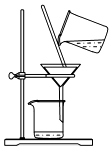 过滤悬浊液
B、
过滤悬浊液
B、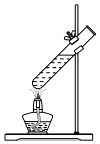 加热液体
C、
加热液体
C、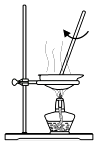 蒸发溶液
D、
蒸发溶液
D、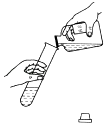 倾倒液体
6. 实验室有一包含有少量氯化钠杂质的硝酸钾固体,某校化学兴趣小组的同学为了得到纯净的硝酸钾,设计了如图所示的操作,下列有关分析中正确的是( )
倾倒液体
6. 实验室有一包含有少量氯化钠杂质的硝酸钾固体,某校化学兴趣小组的同学为了得到纯净的硝酸钾,设计了如图所示的操作,下列有关分析中正确的是( )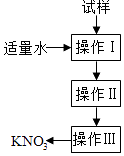 A、操作Ⅰ~Ⅲ分别是溶解、加热蒸发、过滤 B、操作Ⅰ是过滤,将氯化钠固体从溶液中分离除去 C、操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠 D、操作Ⅲ是过滤,将硝酸钾晶体从溶液中分离出来
A、操作Ⅰ~Ⅲ分别是溶解、加热蒸发、过滤 B、操作Ⅰ是过滤,将氯化钠固体从溶液中分离除去 C、操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠 D、操作Ⅲ是过滤,将硝酸钾晶体从溶液中分离出来二、填空题
-
7. 人们通常把的过程叫做结晶.结晶的方法主要有和法.法是适用于一切把可溶于水的物质从溶液中分离出来的方法;法则特别适用于溶解度受温度影响大的物质,如等.8. A、B两种固体物质的溶解度曲线如图所示.
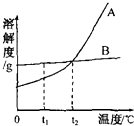
①t1℃时,A和B的溶解度大小关系是
②把t1℃时A的饱和溶液变成不饱和溶液,除了升高温度外,还可以采取的方法有 .
③t2℃时A的溶解度为25g,在t2℃时,向50g水中加入20g的A物质,充分溶解所得溶液的溶质质量分数为 .
④A中混有少量的杂质B,若想得到较为纯净的A,可以采用的方法是 .
三、综合题
-
9. 图中的A、B、C曲线分别是三种物质的溶解度曲线,根据曲线图回答:
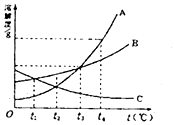 (1)、在℃时,A和C物质的溶解度相等.(2)、在t1℃时,A,B,C三种物质溶解度大小的关系(用“>”、“<”或“=”表示)是 .(3)、在t4℃时,3只烧杯中各盛100g水,然后分别溶解A、B、C三种物质配制成饱和溶液.将溶液都降温到0℃,析出溶质最多的是 , 变成不饱和溶液的是 .(4)、从A、C的饱和溶液中提取A,应采取的方法是 . (填“冷却结晶”或“蒸发结晶”)
(1)、在℃时,A和C物质的溶解度相等.(2)、在t1℃时,A,B,C三种物质溶解度大小的关系(用“>”、“<”或“=”表示)是 .(3)、在t4℃时,3只烧杯中各盛100g水,然后分别溶解A、B、C三种物质配制成饱和溶液.将溶液都降温到0℃,析出溶质最多的是 , 变成不饱和溶液的是 .(4)、从A、C的饱和溶液中提取A,应采取的方法是 . (填“冷却结晶”或“蒸发结晶”)四、实验探究题
-
10. 如图1是硝酸钾和氯化钾固体的溶解度曲线
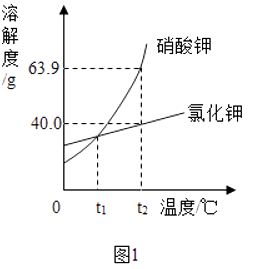 (1)、①t1℃时,硝酸钾溶解度(填“大于”、“等于”、或“小于”)氯化钾.
(1)、①t1℃时,硝酸钾溶解度(填“大于”、“等于”、或“小于”)氯化钾.②t2℃时,将等质量的两种固体分别加入100g水中,充分搅拌后观察到:硝酸钾完全溶解、氯化钾有剩余.则加入的固体质量(m)的取值范围是 .
③将t2℃时的两杯各盛有100g硝酸钾、氯化钾饱和溶液分别降温到t1℃,下列叙述正确的是(填标号).
A、析出硝酸钾晶体质量小于氯化钾
B、硝酸钾溶液与氯化钾溶液的溶质质量分数相等
C、硝酸钾溶液中溶剂质量大于氯化钾溶液中溶剂质量
(2)、某化学小组欲从含有少量氯化钾的硝酸钾样品中,提纯硝酸钾固体.①可采用的提纯方法是(填标号).
A、冷却热饱和溶液 B、蒸发结晶
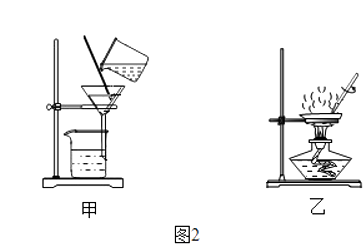
②在提纯过程中,应选择图2中(填“甲”或“乙”)装置进行分离,该操作中玻璃棒的作用是 .
③为检验得到的硝酸钾固体是否含有氯化钾,可使用酸化的硝酸银(AgNO3)溶液来检验,该检验方法的原理为(用化学方程式表示).
-