江苏省苏州市2017-2018学年九年级下学期化学开学考试试卷
试卷更新日期:2018-03-27 类型:开学考试
一、单选题
-
1. 生活中处处有化学,在实际生活中下列过程中利用了物质的化学性质的是( )A、液氮作制冷剂 B、乙炔与氧气形成高温氧炔焰 C、干冰用于人工降雨 D、石墨用于制铅笔2. 小明在厨房实验自制了一瓶“汽水”,所加入的四种物质中属于混合物的是( )A、蔗糖 B、苏打 C、柠檬酸 D、果汁3. 下列所示实验操作正确的是( )A、
 氧气验满
B、
氧气验满
B、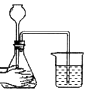 检查气密性
C、
检查气密性
C、 给液体加热
D、
给液体加热
D、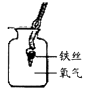 铁丝在氧气中燃烧
4. 下列化学用语表述正确的是( )A、2O—两个氧元素 B、2N2—两个氮气分子 C、Ca2+—钙元素显+2价 D、FeSO4硫酸铁5. 对有关实验现象的描述错误的是( )A、木炭燃烧产生使石灰水变浑的气体 B、干冰在空气中升华周围出现白雾 C、镁条在空气中燃烧发出耀眼的白光 D、铁丝在空气中剧烈燃烧,火星四射6. 科学家经过确认,存在一种化学式为N5的分子,这一发现可能开辟世界能源的新领域,它可能成为我国未来发射火箭的一种新型燃料,下列说法正确的是( )A、N5是一种化合物 B、N5分子是由氮元素组成的 C、N5具有可燃性 D、N5这种物质是由5个氮原子构成的7. 下列有关分子、原子、离子的说法正确的是( )A、分子是化学变化中的最小粒子 B、物质都是由分子构成的 C、原子都是由原子核、中子、电子构成的 D、原子得失电子后形成离子8. 氯吡脲(化学式为C12H10ClN3O)是西瓜膨大剂的主要成分。下列有关叙述,正确的是( )A、含有碳、氢、氧、氯、氮五个元素 B、相对分子质量为247.5g C、属于氧化物 D、每个分子中含有27个原子9. 根据下图的有关信息判断,下列说法错误的是( )
铁丝在氧气中燃烧
4. 下列化学用语表述正确的是( )A、2O—两个氧元素 B、2N2—两个氮气分子 C、Ca2+—钙元素显+2价 D、FeSO4硫酸铁5. 对有关实验现象的描述错误的是( )A、木炭燃烧产生使石灰水变浑的气体 B、干冰在空气中升华周围出现白雾 C、镁条在空气中燃烧发出耀眼的白光 D、铁丝在空气中剧烈燃烧,火星四射6. 科学家经过确认,存在一种化学式为N5的分子,这一发现可能开辟世界能源的新领域,它可能成为我国未来发射火箭的一种新型燃料,下列说法正确的是( )A、N5是一种化合物 B、N5分子是由氮元素组成的 C、N5具有可燃性 D、N5这种物质是由5个氮原子构成的7. 下列有关分子、原子、离子的说法正确的是( )A、分子是化学变化中的最小粒子 B、物质都是由分子构成的 C、原子都是由原子核、中子、电子构成的 D、原子得失电子后形成离子8. 氯吡脲(化学式为C12H10ClN3O)是西瓜膨大剂的主要成分。下列有关叙述,正确的是( )A、含有碳、氢、氧、氯、氮五个元素 B、相对分子质量为247.5g C、属于氧化物 D、每个分子中含有27个原子9. 根据下图的有关信息判断,下列说法错误的是( ) A、氯原子的核电荷数为17 B、钠的原子结构示意图中X=8 C、氯原子的相对原子质量为35.45 D、在化学反应中,钠原子容易得到1个电子10. 下列对一些事实的解释中,不合理的是( )
A、氯原子的核电荷数为17 B、钠的原子结构示意图中X=8 C、氯原子的相对原子质量为35.45 D、在化学反应中,钠原子容易得到1个电子10. 下列对一些事实的解释中,不合理的是( )选项
事 实
解 释
A
碘和碘蒸气都能使淀粉变蓝色
分子能保持物质的化学性质
B
湿衣服晾晒在太阳下更易晒干
温度越高,分子运动速率越快
C
将墨汁滴入一杯清水中,清水很快变黑
分子在不断运动
D
25m3的氧气可以装入0.024m3的钢瓶中
氧分子的体积变小
A、A B、B C、C D、D11. 在一定条件下,下列物质的转化不能一步实现的是( )A、Fe—Fe3O4 B、Fe2O3—Fe C、H2O2—H2 D、CO2—O212. 下列有关实验操作的叙述正确的是( )①用托盘天平和药匙称取5.6 g食盐
②用表面皿、玻璃棒和酒精灯等仪器加热蒸发浓氯化钠溶液获取食盐晶体
③用温度计搅拌并测量硝酸铵和氢氧化钠固体溶于水时的温度变化
④用10mL量筒和滴管量取8.8mL水
A、①②③ B、②③④ C、①④ D、②③13. 下列有关溶液的叙述中正确的是( )A、任何溶液都具有导电性 B、溶液中的溶质可以是一种或多种 C、升高温度均能使饱和溶液变为不饱和溶液 D、析出晶体后的溶液一定是稀溶液14. 在毕业联欢晚会上,某同学表演了精彩魔术——“烧不坏的布手帕”。他先将布手帕放入白酒中浸透,后取出轻轻挤干,再用坩埚钳夹住,从下方点燃,待火焰熄灭后,布手帕依然完好。下列说法正确的是( ) A、布手帕不是可燃物,不能燃烧 B、空气不充足,布手帕不会燃烧 C、布手帕被白酒浸湿,导致着火点降低 D、白酒中水蒸发时吸热,温度达不到布手帕着火点15. 如图所示为某化学反应的微观示意图,其中“○”和“●”表示两种不同元素的原子。下列说法不正确的是( )
A、布手帕不是可燃物,不能燃烧 B、空气不充足,布手帕不会燃烧 C、布手帕被白酒浸湿,导致着火点降低 D、白酒中水蒸发时吸热,温度达不到布手帕着火点15. 如图所示为某化学反应的微观示意图,其中“○”和“●”表示两种不同元素的原子。下列说法不正确的是( ) A、是两种单质反应生成一种化合物 B、可表示氢气和氧气的反应 C、反应前后原子种类没有发生变化 D、反应前后元素化合价发生了变化16. 小明同学对部分化学知识归纳如下,其中完全正确的一组是( )
A、是两种单质反应生成一种化合物 B、可表示氢气和氧气的反应 C、反应前后原子种类没有发生变化 D、反应前后元素化合价发生了变化16. 小明同学对部分化学知识归纳如下,其中完全正确的一组是( )A.化学与人体健康
B.资源的利用和保护
①人体缺钙会导致骨质疏松症
②人体缺锌会导致甲状腺肿大
①保护空气要禁止开采燃烧石油
②爱护水资源要节约用水和防止水体污染
C.“低碳经济”的措施
D.日常生活经验
①改造或淘汰高能耗、高污染产业
②研制和开发新能源替代传统能源
①可以用食醋除去热水瓶中的水垢
②硬水比软水更适合洗衣服
A、A B、B C、C D、D17. 某同学根据铜绿的成分Cu2(OH)2CO3作出猜想:铜的锈蚀除氧气和水外,二氧化碳也参与了反应。为证明“铜的锈蚀反应有二氧化碳参加”,需要进行如图所示实验中的( ) A、甲和乙 B、甲和丁 C、乙和丁 D、丙和丁18. 探究铁的冶炼原理实验装置和炼铁高炉的示意图如下,下列叙述正确的是( )
A、甲和乙 B、甲和丁 C、乙和丁 D、丙和丁18. 探究铁的冶炼原理实验装置和炼铁高炉的示意图如下,下列叙述正确的是( )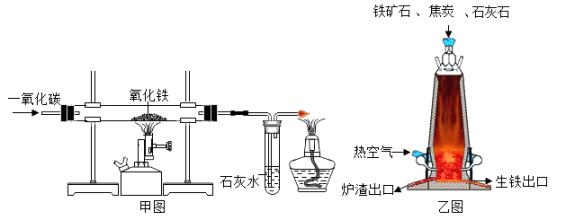 A、甲图中实验结束时,应先停止通一氧化碳再熄灭酒精喷灯 B、乙图中高炉炼铁的原料中焦炭的作用只是利用其燃烧提供热量 C、乙图中为了使焦炭燃烧生成一氧化碳,只需通入少量的热空气 D、完全反应后,甲、乙图中得到产物的区别是甲图得到的是纯净物,乙图得到的是混合物19. 在一密闭容器中,有X, O2, CO2, H2O四种物质,在一定条件下发生某种化学变化,一段 时间后,测得反应前后各物质的质量如下表。下列说法正确的是( )
A、甲图中实验结束时,应先停止通一氧化碳再熄灭酒精喷灯 B、乙图中高炉炼铁的原料中焦炭的作用只是利用其燃烧提供热量 C、乙图中为了使焦炭燃烧生成一氧化碳,只需通入少量的热空气 D、完全反应后,甲、乙图中得到产物的区别是甲图得到的是纯净物,乙图得到的是混合物19. 在一密闭容器中,有X, O2, CO2, H2O四种物质,在一定条件下发生某种化学变化,一段 时间后,测得反应前后各物质的质量如下表。下列说法正确的是( )物质
X
O2
CO2
H2O
反应前的质量/g
19
34
6
2
反应后的质量/g
11
2
待测
20
A、X中只含有C, H元素 B、表中的待测值为32 C、该反应是置换反应 D、反应中生成CO2和H2O的质量比为22:920. 括号内是区别下列各组常见物质的方法,其中错误的是( )A、面粉和蔗糖(加水,振荡) B、硬水与软水(加肥皂水,振荡) C、蒸馏水与食盐水(过滤) D、白酒和食醋(闻气味)21. 将10g溶质质量分数为10%的氯化钠溶液变为20%,下列操作正确的是( )A、加入氯化钠固体1 g B、蒸发5 g水 C、倒出一半溶液 D、加入10g溶质质量分数为20%的氯化钠溶液22. 下图为A物质的溶解度曲线。M、N两点分别表示A物质的两种溶液。下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水) ( )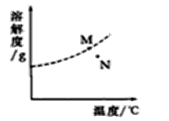 A、从N→M:先向N中加入适量固体A再降温 B、从N→M:先将N降温再加入适量固体A C、从M→N:先将M升温再将其蒸发掉部分水 D、从M→N:先将M降温,过滤后再将其升温23. 下列有关燃烧和灭火说法正确的是( )A、油锅着火后向锅中放入菜叶目的是降低油的着火点 B、家用煤加工成蜂窝煤是力了增大煤与氧气的接触面积 C、高层建筑物起火立即乘电梯撤离 D、不慎碰倒了酒精灯,酒精在桌面燃烧,用水来灭火24. 将水库的水净化为自来水的过程中,下列描述缺乏科学性的是( )A、加入明矾使悬浮小颗粒凝聚 B、投药杀菌消毒 C、通过活性炭吸附色素和异味 D、通过过滤除去可溶性杂质
A、从N→M:先向N中加入适量固体A再降温 B、从N→M:先将N降温再加入适量固体A C、从M→N:先将M升温再将其蒸发掉部分水 D、从M→N:先将M降温,过滤后再将其升温23. 下列有关燃烧和灭火说法正确的是( )A、油锅着火后向锅中放入菜叶目的是降低油的着火点 B、家用煤加工成蜂窝煤是力了增大煤与氧气的接触面积 C、高层建筑物起火立即乘电梯撤离 D、不慎碰倒了酒精灯,酒精在桌面燃烧,用水来灭火24. 将水库的水净化为自来水的过程中,下列描述缺乏科学性的是( )A、加入明矾使悬浮小颗粒凝聚 B、投药杀菌消毒 C、通过活性炭吸附色素和异味 D、通过过滤除去可溶性杂质二、填空题
-
25. 用化学符号填空
(1)、构成氯化钠的阳离子;(2)、硫酸铁(3)、地壳中含量最多的元素;(4)、氧化铜中铜元素的化合价。26. 写出下列反应的化学方程式,并回答有关问题:(1)、加热碳酸氢铵:。(2)、铁丝在氧气中燃烧:。(3)、铁单质与硫酸铜溶液反应: , 其基本反应类型是。(4)、铝具有自我保护的原理:。(5)、木炭的不完全燃烧 , 该反应属于(选填“放热”或“吸热”)反应。三、实验题
-
27. 实验是进行科学探究的重要方式,请根据下图回答问题:
 (1)、用A图所示装置净化黄泥水时,玻璃棒的作用是。(2)、通过B图所示酸的性质实验,可认识到:虽然酸类物质具有相似的化学性质,但由于不同的酸溶于水时电离出的不同,其性质也存在差异。(3)、通过实验C探究,可燃物燃烧的条件是 (一个即可)。(4)、请你总结出铁制品发生锈蚀的主要条件:。28. 请你根据所学知识并结合下图所示装置回答有关问题:
(1)、用A图所示装置净化黄泥水时,玻璃棒的作用是。(2)、通过B图所示酸的性质实验,可认识到:虽然酸类物质具有相似的化学性质,但由于不同的酸溶于水时电离出的不同,其性质也存在差异。(3)、通过实验C探究,可燃物燃烧的条件是 (一个即可)。(4)、请你总结出铁制品发生锈蚀的主要条件:。28. 请你根据所学知识并结合下图所示装置回答有关问题: (1)、用过氧化氢溶液取氧气的化学方程式为 , 可以用E装置收集氧气,现象时,说明氧气已收满。(2)、制取并收集一定量的二氧化碳,应选择装置是 , 欲制得干燥的二氧化碳,还需将气体通过盛有﹙填药品名称)的洗气瓶F。(3)、用收集到的氧气和二氧化碳分别完成如图G、H所示实验,G中集气瓶底部盛有少量水的原因是 , H中喷水的紫色纸花变色。
(1)、用过氧化氢溶液取氧气的化学方程式为 , 可以用E装置收集氧气,现象时,说明氧气已收满。(2)、制取并收集一定量的二氧化碳,应选择装置是 , 欲制得干燥的二氧化碳,还需将气体通过盛有﹙填药品名称)的洗气瓶F。(3)、用收集到的氧气和二氧化碳分别完成如图G、H所示实验,G中集气瓶底部盛有少量水的原因是 , H中喷水的紫色纸花变色。四、简答题
-
29. 如下图为几种固体的溶解度曲线,回答下列问题:
 (1)、CuSO4的溶解度约为20g时,其对应的温度是℃;若想使该饱和溶液转化为不饱和溶液,可采取的方法是(写出一种即可),用此方法后,溶液的质量分数(填“有”或“没有”)发生变化。(2)、80℃时,140g NaNO3溶于100g水形成的溶液 是溶液(填“饱和”或“不饱和”)。(3)、20℃时,NH4NO3溶液的溶质质量分数最大为(计算结果保留到0.1%)。(4)、若KNO3溶液中混有少量的NaCl杂质,可以采 取方法获得较纯净的KNO3固体。(5)、60℃时分别将等质量的KNO3、NaCl、CuSO4 的 饱和溶液各500g恒温蒸发掉100g水,析出晶体 最多的是。(6)、60℃时,10g NaCl和90g KNO3完全溶解于100g 蒸馏水中,冷却到30℃后,(“有”或“没有”)NaCl析出,有g KNO3结晶析出。
(1)、CuSO4的溶解度约为20g时,其对应的温度是℃;若想使该饱和溶液转化为不饱和溶液,可采取的方法是(写出一种即可),用此方法后,溶液的质量分数(填“有”或“没有”)发生变化。(2)、80℃时,140g NaNO3溶于100g水形成的溶液 是溶液(填“饱和”或“不饱和”)。(3)、20℃时,NH4NO3溶液的溶质质量分数最大为(计算结果保留到0.1%)。(4)、若KNO3溶液中混有少量的NaCl杂质,可以采 取方法获得较纯净的KNO3固体。(5)、60℃时分别将等质量的KNO3、NaCl、CuSO4 的 饱和溶液各500g恒温蒸发掉100g水,析出晶体 最多的是。(6)、60℃时,10g NaCl和90g KNO3完全溶解于100g 蒸馏水中,冷却到30℃后,(“有”或“没有”)NaCl析出,有g KNO3结晶析出。五、综合题
-
30. 天然水净化为自来水的主要流程如下:
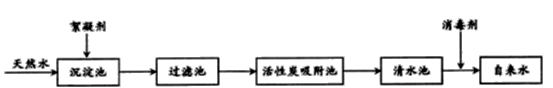 (1)、下列说法不正确的是__________(填字母)。A、过滤池可以除去难溶性杂质 B、活性炭吸附池可以除去水中的色素和臭味 C、清水池中一定是软水(2)、明矾[KAl(SO4 )m·12H2O]能作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝。m= , 氢氧化铝的化学式为。(3)、目前不少自来水用液氯(Cl2)作为消毒剂,液氯注入水后发生反应的示意图如下:
(1)、下列说法不正确的是__________(填字母)。A、过滤池可以除去难溶性杂质 B、活性炭吸附池可以除去水中的色素和臭味 C、清水池中一定是软水(2)、明矾[KAl(SO4 )m·12H2O]能作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝。m= , 氢氧化铝的化学式为。(3)、目前不少自来水用液氯(Cl2)作为消毒剂,液氯注入水后发生反应的示意图如下:
其中“
 ”“
”“  ”“●”代表不同原子,产物D为次氯酸(HClO),有杀菌作用。液氯与水反应的化学方程式是。(4)、天然水中微生物使有机物(以C6H10O5表示)转化为CO2和H2O的过程中所需O2的量叫做生化需氧量(BOD,单位为mg ·L-1)。反应的化学方程式为 ,测得20℃时1L某天然水样中含有有机物(C6H10O5)的质量为10. 8mg,则该水样的BOD值是。
”“●”代表不同原子,产物D为次氯酸(HClO),有杀菌作用。液氯与水反应的化学方程式是。(4)、天然水中微生物使有机物(以C6H10O5表示)转化为CO2和H2O的过程中所需O2的量叫做生化需氧量(BOD,单位为mg ·L-1)。反应的化学方程式为 ,测得20℃时1L某天然水样中含有有机物(C6H10O5)的质量为10. 8mg,则该水样的BOD值是。六、计算题
-
31. 某化学小组为测定一瓶失去标签的盐酸的溶质质量分数,分别采用两种不同的实验方案进行测定。
方案Ⅰ:取石灰石粉末5g于烧杯中,加入20g该盐酸溶液,充分反应后,过滤、洗涤、干燥,称量得剩余固体3g。
方案Ⅱ:取石灰石粉末5g于锥形瓶中,再通过分液漏斗加入盐酸溶液,利用测定产生二氧化碳的体积(200C、标准大气压)计算盐酸的溶质质量分数,装置示意图如下:
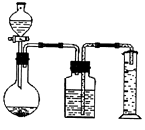 (1)、请利用方案Ⅰ数据计算(写出计算过程):
(1)、请利用方案Ⅰ数据计算(写出计算过程):①该盐酸的溶质质量分数;
②反应后所得溶液溶质质量分数。(结果保留至0.1 %)
(2)、经过多次实验发现方案Ⅱ计算结果略大于方案Ⅰ,原因。
-
-