湖南省祁阳县2016-2017学年九年级化学二模考试试卷
试卷更新日期:2018-03-19 类型:中考模拟
一、单选题
-
1. 永州市有许多优秀的制作工艺,下列工艺中不包含化学变化的是:( )A、浯溪石碑的雕刻 B、祁阳臭豆腐的制作 C、金洞红薯酒的酿造 D、海螺水泥的烧制2. 实验操作正确的是( )A、测溶液pH
 B、熄灭酒精灯
B、熄灭酒精灯  C、取用固体药品
C、取用固体药品  D、过滤操作
D、过滤操作  3. 下列物质的用途中,利用其物理性质的是( )A、氧气用于炼钢 B、硫酸用于除铁锈 C、干冰用作制冷剂 D、碳酸氢钠用于治疗胃酸过多症4. 海水提镁的反应之一:MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓,该反应属于( )A、化和反应 B、复分解反应 C、置换反应 D、分解反应5. 某同学制作的试剂标签如下,其中化学式书写不正确的是( )A、
3. 下列物质的用途中,利用其物理性质的是( )A、氧气用于炼钢 B、硫酸用于除铁锈 C、干冰用作制冷剂 D、碳酸氢钠用于治疗胃酸过多症4. 海水提镁的反应之一:MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓,该反应属于( )A、化和反应 B、复分解反应 C、置换反应 D、分解反应5. 某同学制作的试剂标签如下,其中化学式书写不正确的是( )A、 B、
B、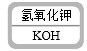 C、
C、 D、
D、 6. 祁阳县在“创国卫”活动中,要求市民禁止燃放鞭炮,下列安全标志中,符合该主题的是:( )A、
6. 祁阳县在“创国卫”活动中,要求市民禁止燃放鞭炮,下列安全标志中,符合该主题的是:( )A、 B、
B、 C、
C、 D、
D、 7. 受损元素周期表中某元素的残留信息如图所示,根据残留信息得出的下列说法中错误的是( )
7. 受损元素周期表中某元素的残留信息如图所示,根据残留信息得出的下列说法中错误的是( ) A、该元素是金属元素,原子序数为11 B、该元素符号为Mg C、该元素的原子结构示意图为
A、该元素是金属元素,原子序数为11 B、该元素符号为Mg C、该元素的原子结构示意图为 D、该元素的原子在化学反应中易失去电子
8. NH4Cl和Na2SO4的溶解度表及溶解度曲线如下,下列说法正确的是:( )
D、该元素的原子在化学反应中易失去电子
8. NH4Cl和Na2SO4的溶解度表及溶解度曲线如下,下列说法正确的是:( ) A、甲为NH4Cl B、t2时,甲溶液的溶质质量分数一定比乙大 C、甲、乙饱和溶液从t3降温到t2 , 溶质的质量分数都变小 D、等质量的甲、乙饱和溶液从t1升温到t3 , 为使其溶液恰好饱和,加入的甲、乙固体质量相等9. 下列实验操作能达到实验目的的是:( )
A、甲为NH4Cl B、t2时,甲溶液的溶质质量分数一定比乙大 C、甲、乙饱和溶液从t3降温到t2 , 溶质的质量分数都变小 D、等质量的甲、乙饱和溶液从t1升温到t3 , 为使其溶液恰好饱和,加入的甲、乙固体质量相等9. 下列实验操作能达到实验目的的是:( )选项
实验目的
实验操作
A
除去CO2中少量的CO
点燃
B
除去CuSO4溶液中的少量FeSO4
加入足量的铜粉
C
鉴别澄清石灰水和NaOH溶液
加入稀盐酸
D
除去CaCl2溶液中少量的HCl
加入足量的碳酸钙
A、A B、B C、C D、D10. 能验证Zn、Cu、Ag三种金属活动性顺序的一组试剂是( )A、Zn、Ag、CuSO4溶液 B、Zn、Cu、Ag、H2SO4溶液 C、Cu、Ag、ZnSO4溶液 D、Ag、ZnSO4溶液、CuSO4溶液二、简答题
-
11. 质量守恒定律的发现对化学的发展做出了重要贡献。(1)、通过称量下列各组试剂在密闭容器内混合前后的总质量,能验证质量守恒定律的是____(填标号)。A、蔗糖和水 B、氯化钠溶液和硝酸钾溶液 C、铁和氯化铜溶液(2)、在氧气中点燃红磷的实验过程,固体变化下图所示。

①从燃烧条件分析,固体质量在t1前没有发生变化的原因是;
②该反应的化学方程式为;
③参加反应的氧气质量为g。
12. 某实验小组的同学要探究酸碱盐中碳酸钠的化学性质,设计了如下实验装置及方案:实验装置 实验步骤及操作 实验现象 
①将注射器2中的溶液推入盛有稀盐酸的瓶中,至不再有气泡产生。 气球变瘪 ②将注射器3稍稍向外拉 澄清石灰水变浑浊 ③将注射器1中的溶液推入瓶中 气球鼓起 ④将注射器4中的溶液推入瓶中 溶液变浑浊 (1)、步骤①中气球变瘪的原因。(2)、步骤③中气球鼓起的原因。(3)、步骤④中发生反应的化学方程式。13. 硫酸铜溶液对过氧化氢的分解有催化作用。取一定质量8.5%的过氧化氢溶液倒入烧杯中,加入一定质量15%的硫酸铜溶液,过氧化氢完全分解。有关实验数据如下表所示(不考虑气体在水中的溶解)。请计算:反 应 前
反 应 后
实验
数据
烧杯和过氧化氢溶液的质量/g
硫酸铜溶液的质量/g
烧杯和烧杯中溶液的质量/g
60
3.3
62.5
(1)、生成氧气的质量为g。(2)、反应后烧杯中溶液溶质的质量分数为。(写出计算过程,结果精确到0.1%)三、填空题
-
14. 下图是常见固体物质的溶解度曲线,根据图示回答:
 (1)、t3℃时,A、B、C三种物质的溶解度由大到小的顺序为。(2)、t1℃时,将20g A物质放入100g水中,充分溶解后所得的溶液是(填“饱和”或“不饱和”)溶液.欲使t2℃时C物质的饱和溶液变为不饱和溶液,可采取的方法是(任填一种方法)。(3)、现有30℃的不饱和KNO3溶液,与该溶液有关的量有:
(1)、t3℃时,A、B、C三种物质的溶解度由大到小的顺序为。(2)、t1℃时,将20g A物质放入100g水中,充分溶解后所得的溶液是(填“饱和”或“不饱和”)溶液.欲使t2℃时C物质的饱和溶液变为不饱和溶液,可采取的方法是(任填一种方法)。(3)、现有30℃的不饱和KNO3溶液,与该溶液有关的量有:①水的质量 ②溶液中KNO3的质量 ③KNO3的质量分数
④30℃时KNO3的溶解度 ⑤溶液的质量
Ⅰ.在该不饱和溶液中加硝酸钾至饱和,不变的量有(填序号,下同),
Ⅱ.将该不饱和溶液恒温蒸发至饱和,不变的量有。
四、科学探究题
-
15. 镁条在空气中久置表面会变黑。某小组同学设计并进行实验,探究镁条变黑的条件。
【查阅资料】常温下,亚硫酸钠(Na2SO3)可与O2发生化合反应。
【猜想与假设】常温下,镁条变黑可能与O2、CO2、水蒸气有关。
【进行实验】通过控制与镁条接触的物质,利用如图装置(镁条长度为3cm,试管容积为20mL),分别进行下列5个实验,并持续观察20天。
【解释与结论】编号 主要实验操作 实验现象 ① 先充满用NaOH浓溶液洗涤过的空气
再加入2mL浓硫酸镁条始终无明显变化 ② 加入2mL NaOH浓溶液 镁条始终无明显变化 ③ 先加入2mL浓硫酸
再通入约4mL CO2镁条始终无明显变化 ④ 先加入4mL饱和Na2SO3溶液
再充满CO2镁条始终无明显变化 ⑤ 先加入2mL蒸馏水
再通入约4mL CO2镁条第3天开始变黑
至第20天全部变黑(1)、实验1和2中,NaOH浓溶液的作用是(用化学方程式表示)。(2)、实验1的目的是。(3)、得出“镁条变黑一定与CO2有关”结论,依据的两个实验是(填编号)。(4)、【反思与评价】欲进一步证明镁条表面的黑色物质中含有碳酸盐,所需要的试剂是。
-