江西省高安市2015-2016学年九年级化学二模考试试卷
试卷更新日期:2018-03-19 类型:中考模拟
一、单选题
-
1. 下列生活里的常见现象中,一定涉及化学变化的是( )A、放在衣柜里的樟脑丸逐渐变小 B、冰箱中放入木炭后,异味消失 C、自行车淋湿一段时间后出现锈渍 D、夏天带到学校的咸菜表面有时出现食盐2. 下列实验操作正确的是( )A、
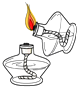 点燃酒精灯
B、
点燃酒精灯
B、 闻药品的气味
C、
闻药品的气味
C、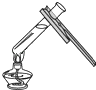 加热液体
D、
加热液体
D、 读取液体体积
3. 下列物质按单质、氧化物、化合物、混合物的顺序排列的是( )
读取液体体积
3. 下列物质按单质、氧化物、化合物、混合物的顺序排列的是( )
A、金刚石、生石灰、粗食盐、冰水 B、水银、干冰、熟石灰、天然气 C、苛性钠、铁锈、纯碱、石油 D、硫磺、液态氧、粗食盐、胆矾4. 高铁酸钠(Na2FeO4)是一种新型高效的净水剂。高铁酸钠中铁元素的化合价是( )A、+2 B、+3 C、+4 D、+65. 一些食物的近似pH如下:其中显碱性的是( )
A、鸡蛋清:7.6~8.0 B、葡萄汁:3.5~4.5 C、牛奶:6.3~6.6 D、苹果汁:2.9~3.36. 钛具有硬度大、密度小、熔点高、抗腐蚀性强等优良性能,被誉为“未来金属”。钛铁矿石的主要成分是钛酸亚铁(FeTiO3)。冶炼金属钛时,主要发生以下两个反应:①2FeTiO3+6C+7Cl2 2X+2TiCl4+6CO,②TiCl4+2Mg Ti + 2MgCl2
则X为( )
A、FeCl2 B、FeCl3 C、Fe2O3 D、FeCO37. 苏州的“碧螺春”享誉全国。“碧螺春”茶叶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46。下列说法错误的是( )
A、单宁酸由碳、氢、氧三种元素组成 B、一个单宁酸分子是由76个碳原子、52个氢原子和46个氧原子构成 C、单宁酸中碳、氧元素的质量比为57∶23 D、单宁酸中氢元素的质量分数最小8. 氧化汞受热分解生成汞和氧气的反应前后,发生改变的是( )
A、分子种类 B、原子种类 C、元素种类 D、原子数目9. 在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色,有关判断正确的是( )A、滤渣中一定有银、没有铜和锌 B、滤渣中一定有银和锌,可能有铜 C、滤液中一定有硝酸锌、硝酸铜、硝酸银 D、滤液中一定有硝酸锌、硝酸铜,可能有硝酸银10. 将等质量的镁、铁、锌,分别放入三份溶质质量分数相同的稀盐酸中,反应生成的H2质量与反应时间的关系如图所示.根据图中的信息,作出的判断不正确的是( ) A、图线x表示镁的反应情况 B、铁消耗的稀盐酸质量最大 C、镁、锌一定过量,铁可能反应完 D、镁一定过量,锌、铁可能反应完11. 下列物质中,属于有机合成材料的是( )
A、图线x表示镁的反应情况 B、铁消耗的稀盐酸质量最大 C、镁、锌一定过量,铁可能反应完 D、镁一定过量,锌、铁可能反应完11. 下列物质中,属于有机合成材料的是( )A.塑料 B.棉花
C.羊毛 D.
12. 下列物质放入水中,能形成溶液的是( )A.蔗糖 B.植物油
C.面粉 D.
13. 下列物质由离子构成的是( )A.铜 B.二氧化碳
C.氯化钠 D.
14. 农作物生长需要含较多氮、磷、钾元素的化肥,下列化肥属于复合肥料的是( )A.NH4NO3 B.Ca(H2PO4)2 C.(NH4)2HPO4 D.
15. 除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案可行的是( )A.木炭粉(CuO)——在空气中灼烧
B.KCl溶液(CaCl2)——通入过量的CO2气体,过滤
C. H2气体(HCl气体)——依次通过足量的NaOH溶液和浓硫酸
D.NaCl溶液(Na2CO3)——加入适量的 , 过滤
二、填空题
-
16. 用化学用语填空:
(1)、磷的元素符号为;(2)、两个锌离子;(3)、二氧化硫中硫元素显+4价;17. 元素周期表是学习和研究化学的重要工具。回答下列问题:(1)、元素周期表中不同元素间最本质的区别是 (填字母)。A、质子数不同 B、中子数不同 C、相对原子质量不同(2)、1869年, (填字母)发现了元素周期律并编制出元素周期表。A、张青莲 B、门捷列夫 C、拉瓦锡(3)、元素周期表中氟元素的有关信息如下图所示,下列说法正确的是 (填字母)。 A、氟属于非金属元素 B、氟的原子序数是9 C、氟的相对原子质量是19.00g(4)、氟原子结构示意图为
A、氟属于非金属元素 B、氟的原子序数是9 C、氟的相对原子质量是19.00g(4)、氟原子结构示意图为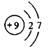 ,氟原子在化学反应中易(填“得到” 或“失去”)电子,由钠元素和氟元素组成的化合物氟化钠的化学式为。
,氟原子在化学反应中易(填“得到” 或“失去”)电子,由钠元素和氟元素组成的化合物氟化钠的化学式为。
18. 水是一种重要的资源。(1)、电解水实验揭示了水的组成。右图实验中得到氧气的试管是(填“1”或“2”)。 (2)、自来水厂净水过程中用到活性炭,其作用是。(3)、海水淡化可缓解淡水资源匮乏的问题。下图为太阳能海水淡化装置示意图。
(2)、自来水厂净水过程中用到活性炭,其作用是。(3)、海水淡化可缓解淡水资源匮乏的问题。下图为太阳能海水淡化装置示意图。
①水变成水蒸气的过程中,不发生变化的是(填字母序号,2分)。
A.分子质量 B.分子种类 C.分子间隔
②利用该装置将一定量的海水暴晒一段时间后,剩余海水中氯化钠的质量会(填“变大”、“变小”或“不变”,2分)
19. 甲和乙两种固体物质的溶解度曲线如右图所示。回答下列问题: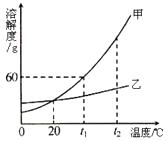
①在℃时,甲和乙两种物质的溶解度相等。
②将t2℃时等质量的甲和乙两种物质的饱和溶液分别降温到0℃,析出固体质量较少的是(填“甲”或“乙”)。
③t1℃时,将60 g甲、乙物质分别放入100 g 水中,充分搅拌,所得溶液的溶质质量分数大小关系为甲乙(填>、<、=)
20. A、B、C、D、E、F、G、H、I都是初中化学学过的物质.其中E、F、H均为黑色固体,B为紫红色固体,D为混合物.他们之间有如图的转化关系(部分生成物已省去). (1)、用化学式表示C的组成 ;(2)、A→B的基本反应类型;(3)、写出F→E的化学方程式;(4)、指出B的一种用途 .21. 下图是实验室制取气体常用的装置,请结合装置回答有关问题:
(1)、用化学式表示C的组成 ;(2)、A→B的基本反应类型;(3)、写出F→E的化学方程式;(4)、指出B的一种用途 .21. 下图是实验室制取气体常用的装置,请结合装置回答有关问题: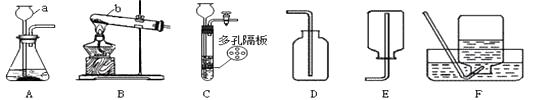 (1)、写出图中标号仪器的名称:①;② .(2)、实验室可加热KClO3和MnO2的固体混合物制取氧气,请写出该反应的化学方程式: , 应选择的气体发生装置是(填字母).(3)、若实验室用C、F装置组合制取某种气体,应满足的条件是
(1)、写出图中标号仪器的名称:①;② .(2)、实验室可加热KClO3和MnO2的固体混合物制取氧气,请写出该反应的化学方程式: , 应选择的气体发生装置是(填字母).(3)、若实验室用C、F装置组合制取某种气体,应满足的条件是Ⅰ.反应物是块状固体和液体
Ⅱ.反应在常温下进行
Ⅲ.制得气体密度比空气大
Ⅳ.制得气体密度比空气小
Ⅴ.制得气体难(不易)溶于水
Ⅵ.制得气体易溶于水
三、实验题
-
22. 小明在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了探究。
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】①6H2SO4(浓)+2Fe Fe2(SO4)3+6 H2O +3SO2↑
②SO2可使品红溶液的红色褪去。
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫。
(1)、【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验。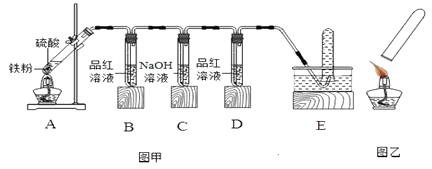
请帮助小明完成下表:
A中硫
酸浓度
实验现象
A中生成气体成分
B中品
红溶液
D中品
红溶液
爆鸣实验
实验一
98%
褪色
不褪色
无爆鸣声
只有SO2
实验二
45%
稍有褪色
不褪色
有爆鸣声
实验三
25%
不褪色
只有H2
【实验结论】铁与不同浓度的硫酸溶液反应,生成的气体产物可能不同,当硫酸浓度达到足够大时,生成的气体产物中有二氧化硫。
(2)、【交流反思】①写出实验三中铁与硫酸反应的化学方程式:。②实验一中C装置中反应的化学方程式:。
(3)、【拓展延伸】在初中化学教材中也有反应物浓度不同,生成的产物不同的例子23. 学习完“酸、喊、盐的性质”后,老师将两瓶未贴标签的饱和石灰水、饱和碳酸钠溶液摆放在实验桌上,让同学们区分.下面是“雄鹰小组”同学们的探究过程:(1)、【讨论交流】李壮(组长):区分两种物质的原理是:依据物质的性质,选择一种试剂与两种物质混合,产生两种不同的现象。大家椐此来说一说,区分这两种溶液应选用哪种试剂,并说明理由;
王志:我认为可以选择稀盐酸,理由是稀盐酸与碳酸钠反应有气泡产生,稀盐酸与氢氧化钙反应无明显现象。
马凌:我选择的是碳酸钠溶液.理由是 .
(2)、【实验探究】大家按照王志的方案进行了如图所示的实验:
①实验中同学们根据现察到的现象,判断出甲试管中原溶液为碳酸钠溶液,乙试管中原溶液为石灰水。则乙试管中反应的化学方程式为
②实验后王志将甲、乙两试管中的废液倒入烧杯中,发现烧杯中液体澄清,大家对烧杯中溶液的溶质成分产生了探究兴趣,请你和他们一起探究:
①取少量烧杯中的溶液于试管中,滴入几滴无色酚酞溶液,发现溶液仍为无色,由此可知溶液中一定含有(填化学式)可能含有HCl。
②另取少量溶液于试管中,加入 , 观察到有气泡产生,说明该废液中还含有HCl。
(3)、【反思评价】欲从烧杯废液中得到纯净的NaCl,可先向烧杯中加入适量的溶液,经过滤后进行蒸发即可得到纯净的NaCl。
探究活动结束了,同学们充分体验到合作探究的乐趣和学习成功的喜悦!
四、简答题
-
24. 石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下表:
实验次数
第一次
第二次
第三次
第四次
稀盐酸的用量
5g
5g
5g
5g
剩余固体的质量
3g
2g
1g
1g
(1)、该石灰石样品中碳酸钙的质量分数是;
(2)、计算该稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%).
(3)、第三次加入5g稀盐酸后所得溶液的质量为 。