备考2018年中考 化学一轮基础复习:专题九 质量守恒定律
试卷更新日期:2018-03-07 类型:一轮复习
一、单选题
-
1. 下列有关说法错误的是( )A、氯化钠、硫酸铵、氯酸钾都属于盐 B、过氧化氢和水的化学性质不同,是因为它们的分子构成不同 C、氢氧化钠和氢氧化钙的化学性质相似,是因为它们的水溶液中都含有氢氧根离子 D、某物质在空气中燃烧生成二氧化碳和水,说明该物质一定含有碳、氢、氧三种元素2. 下列关于化学方程式H2SO3+2H2=S↓+3H2O的理解,错误的是( )A、生成物有沉淀 B、反应物是H2SO3和H2 , 生成物是S和H2O C、该反应中,反应前后原子的种类和数目都不变 D、每1份质量的H2SO3和2份质量的H2完全反应,生成1份质量的S和3份质量的H2O3. 加热氢氧化钙与氯化铵固体发生如下反应:2NH4Cl+Ca(OH)2 CaCl2+2X↑+2H2O,试推测X的化学式是( )A、NO2 B、H3N C、HCl D、NH34. 质量守恒定律是自然界基本的规律之一.下列装置及实验(天平未画出)能用来验证质量守恒定律的是( )A、
 B、
B、 C、
C、 D、
D、 5. 硫在氧气中燃烧的化学方程式是:S+O2 SO2 , 从这个化学方程式获得的信息错误的是( )A、反应前后元素种类不变 B、该反应的生成物中含有氧气 C、该反应的反应物是硫和氧气 D、该反应发生所需要的条件是点燃6. a克木炭在b克氧气中燃烧,生成二氧化碳的质量( )A、大于(a+b)克 B、小于(a+b)克 C、等于(a+b)克 D、小于或等于(a+b)克7. 下列图象能正确反映其对应变化关系的时是( )A、
5. 硫在氧气中燃烧的化学方程式是:S+O2 SO2 , 从这个化学方程式获得的信息错误的是( )A、反应前后元素种类不变 B、该反应的生成物中含有氧气 C、该反应的反应物是硫和氧气 D、该反应发生所需要的条件是点燃6. a克木炭在b克氧气中燃烧,生成二氧化碳的质量( )A、大于(a+b)克 B、小于(a+b)克 C、等于(a+b)克 D、小于或等于(a+b)克7. 下列图象能正确反映其对应变化关系的时是( )A、 加热一定质量的碳酸氢钠固体
B、
加热一定质量的碳酸氢钠固体
B、 向盛有少量硫酸溶液的烧杯中滴加一定质量的水
C、
向盛有少量硫酸溶液的烧杯中滴加一定质量的水
C、 向盛有一定质量二氧化锰的烧杯中加入过氧化氢溶液
D、
向盛有一定质量二氧化锰的烧杯中加入过氧化氢溶液
D、 向盛有一定质量NaOH和Na2CO3混合溶液的烧杯中滴加稀盐酸
8. 室温下,过氧化氢溶液中加入少量二氧化锰后立即产生氧气.下列各图中与该反应事实最相符的是( )A、
向盛有一定质量NaOH和Na2CO3混合溶液的烧杯中滴加稀盐酸
8. 室温下,过氧化氢溶液中加入少量二氧化锰后立即产生氧气.下列各图中与该反应事实最相符的是( )A、 B、
B、 C、
C、 D、
D、 9. 在一个密闭容器内有A、B、C、D四种物质,经过反应一段时间后,测得反应前后各物质的质量如下表所示:
9. 在一个密闭容器内有A、B、C、D四种物质,经过反应一段时间后,测得反应前后各物质的质量如下表所示:物质
甲
乙
丙
丁
反应前质量/克
34
2
5
5
反应后质量/克
0
x
5
21
以下说法正确的是( )
A、该反应是化合反应 B、x的值为18 C、该反应是分解反应 D、丙一定是催化剂10. 在一定的条件下,向一密闭的容器内加入A、B、C、D四种物质各20g,充分反应后,测定其质量,得到数据如下:物质
A
B
C
D
反应前质量(g)
20
20
20
20
反应后质量(g)
20
30
未知
14
下列说法不正确的是( )
A、A物质可能是该反应的催化剂 B、容器内发生了化合反应 C、反应后容器内C的质量为16g D、其化学方程式为:2C+3D=5B二、填空题
-
11. 化学与能源密切相关.氢化镁可作氢动力汽车的能源提供剂:MgH2+2X=Mg(OH)2+2H2↑,则X的化学式为.2017年5月,我国成为第一个实现海域开采可燃冰(主要含有甲烷水合物)并连续稳定产气的国家,甲烷充分燃烧的化学方程式为 . 相等质量的氢气、甲烷完全燃烧需要氧气的质量比为 .12.
构建和谐社会,建设社会主义新农村的目标之一是让农民饮用清洁的自来水.自来水消毒过程中常会发生甲、乙化学反应,其反应的微观过程可用如图表示:

(
 表示氯原子,
表示氯原子,  表示氧原子,
表示氧原子,  表示氢原子)
表示氢原子)①从图中可以看出化学变化的实质是;
②乙图发生反应的基本反应类型是 .
③生活中常用方法鉴别硬水和软水,生活中通常采用的方法降低水的硬度.
三、计算题
-
13. 在实验室加热32.5g二氧化锰和氯酸钾的固体混合物制取氧气时,剩余固体物质的质量变化如下图所示。请计算:
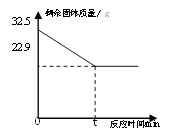 (1)、完全反应时,生成氧气的质量为。(2)、完全反应后,剩余固体物质属 (填纯净物、混合物)。(3)、原固体混合物中氯酸钾的质量为 (列式计算)。
(1)、完全反应时,生成氧气的质量为。(2)、完全反应后,剩余固体物质属 (填纯净物、混合物)。(3)、原固体混合物中氯酸钾的质量为 (列式计算)。四、实验探究题
-
14. 根据如图所示实验回答问题.
 (1)、A实验中,气球的作用是(写一点).(2)、B实验中,除了要控制集气瓶大小规格相同外,还要控制相同.(3)、C实验中,通电一段时间后玻璃管a、b所收集的气体体积比为 , 该实验说明水是由组成.15. 化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如图),同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体.
(1)、A实验中,气球的作用是(写一点).(2)、B实验中,除了要控制集气瓶大小规格相同外,还要控制相同.(3)、C实验中,通电一段时间后玻璃管a、b所收集的气体体积比为 , 该实验说明水是由组成.15. 化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如图),同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体. (1)、请写出镁条燃烧的化学方程式;(2)、同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量,有人认为这个反应不遵循质量守恒定律.你认为出现这样实验结果的原因可能是:(3)、小红按右下图装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体.
(1)、请写出镁条燃烧的化学方程式;(2)、同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量,有人认为这个反应不遵循质量守恒定律.你认为出现这样实验结果的原因可能是:(3)、小红按右下图装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体.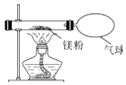
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应产生黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
实验操作
实验现象及结论
(4)、【反思与交流】①氮化镁中氮元素的化合价是;②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2 , 合理的解释是: .
③同学们又联想到氯气在氯气中能够燃烧,于是对燃烧条件又有了新的认识: .
-