2017_2018学年高中化学人教版选修三 课时训练11溶解性、手性、无机含氧酸分子的酸性
试卷更新日期:2018-03-05 类型:同步测试
一、物质的溶解性
-
1. 根据物质的溶解性“相似相溶”的一般规律,说明溴、碘单质在四氯化碳中的溶解度比在水中的大。下列说法正确的是( )A、溴、碘单质和四氯化碳中都含有卤素 B、溴、碘是单质,四氯化碳是化合物 C、Br2、I2是非极性分子,CCl4也是非极性分子,而水是极性分子 D、以上说法都不对2. 用一带静电的玻璃棒靠近A、B两种纯液体流,据图分析,这两种液体分子的溶解性正确的是( )
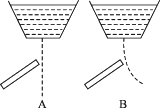 A、A极易溶于水 B、B极易溶于水 C、A与B能相互溶解 D、A和B都难溶于水3. 关于CS2、SO2、NH3三种物质的说法中正确的是 ( )A、CS2在水中的溶解度很小,是由于其属于极性分子 B、SO2和NH3均易溶于水,原因之一是它们都是极性分子 C、CS2为非极性分子,所以其在三种物质中熔、沸点最低 D、NH3在水中溶解度很大是因为NH3分子有极性4. 下列物质易溶于水的是 , 易溶于CCl4的是。(均填编号)
A、A极易溶于水 B、B极易溶于水 C、A与B能相互溶解 D、A和B都难溶于水3. 关于CS2、SO2、NH3三种物质的说法中正确的是 ( )A、CS2在水中的溶解度很小,是由于其属于极性分子 B、SO2和NH3均易溶于水,原因之一是它们都是极性分子 C、CS2为非极性分子,所以其在三种物质中熔、沸点最低 D、NH3在水中溶解度很大是因为NH3分子有极性4. 下列物质易溶于水的是 , 易溶于CCl4的是。(均填编号)①NH3 ②CH4 ③
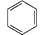 ④HCl ⑤C2H4
④HCl ⑤C2H4⑥Br2 ⑦HNO3 ⑧H2S
二、手性碳原子的判断
-
5. 有且只有一个手性碳原子的有机物分子为手性分子,下列有机物分子中属于手性分子的是( )
①新戊烷[(CH3)4C] ②乳酸[CH3CH(OH)COOH]
③甘油 ④
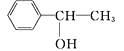 A、①②③ B、②和④ C、①和③ D、②③④6. 下列化合物分子中含2个手性碳原子的是( )A、
A、①②③ B、②和④ C、①和③ D、②③④6. 下列化合物分子中含2个手性碳原子的是( )A、 B、
B、 C、
C、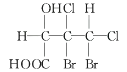 D、
D、 7. 下列有机物中含有手性碳原子的是( )A、
7. 下列有机物中含有手性碳原子的是( )A、 B、
B、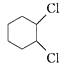 C、
C、 D、
D、
三、无机含氧酸分子的酸性
-
8. 元素X和Y属于同一个主族。元素X和氢组成的化合物(X显-2价)在通常状况下是一种液体,其中X的质量分数为88.9%;元素X和元素Y可以形成两种化合物。在这两种化合物中,X的质量分数分别为50%和60%,下列说法正确的是( )A、两种元素分别为C和Si,且酸性:H2CO3>H2SiO3 B、两种元素分别为N和P,且酸性:HNO3>H3PO4 C、两种元素分别为O和S,且酸性:H2SO4>H2SO3 D、两种元素分别是Mg和Ca,且碱性:Ca(OH)2>Mg(OH)29. 下列物质的酸性强弱比较中,错误的是( )A、HClO4>HBrO4>HIO4 B、HClO4>H2SO4>H3PO4 C、HClO4>HClO3>HClO D、H2SO3>H2SO4>H2S2O310. 试比较下列含氧酸的酸性强弱(填“>”“<”或“=”):H2SO4H2SO3;HNO2HNO3;HClOHClO2;HClO3HClO4;H3PO4H3PO3。
四、达标训练
-
11. 下列物质中,属于易溶于水的一组是( )A、CH4、CCl4、CO2 B、NH3、HCl、HBr C、Cl2、H2、N2 D、H2S、C2H6、SO212. 根据“相似相溶”规律,你认为下列物质在水中溶解度较大的是( )A、乙烯 B、二氧化碳 C、二氧化硫 D、氢气13. 均由两种短周期元素组成的A、B、C、D化合物分子,都含有18个电子,它们分子中所含原子的数目依次为2、3、4、6;A和C分子中的原子个数比为1∶1,B和D分子中的原子个数比为1∶2;D可作为火箭推进剂的燃料。下列说法正确的是( )A、分子中相对原子质量较大的四种元素第一电离能由大到小排列的顺序为A>B>C>D B、A与HF相比,其熔、沸点:A>HF C、B分子在水中的溶解度较大 D、若设A的中心原子为X,B的中心原子为Y,则酸性:HXO>HXO3>HXO414. 下列对分子性质的解释中,不正确的是( )A、碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 B、乳酸(
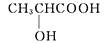 )存在对映异构体,因为其分子中含有一个手性碳原子
C、在NH3分子中存在极性共价键和配位键
D、由下图知酸性:H3PO4>HClO,因为H3PO4分子中有非羟基氧原子
)存在对映异构体,因为其分子中含有一个手性碳原子
C、在NH3分子中存在极性共价键和配位键
D、由下图知酸性:H3PO4>HClO,因为H3PO4分子中有非羟基氧原子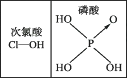 15. 小明同学在学习钠的化合物性质时,记录了以下四个化学方程式:
15. 小明同学在学习钠的化合物性质时,记录了以下四个化学方程式:①Na2SiO3+H2O+CO2=Na2CO3+H2SiO3↓
②Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
③Na2CO3+H2SO3=Na2SO3+H2O+CO2↑
④Na2SO3+H2SO4=Na2SO4+H2O+SO2↑
请你根据学过的知识判断4个反应中的4种含氧酸,其中酸性最强的是( )
A、H2SO4 B、H2SO3 C、H2SiO3 D、H2CO316. 下列物质性质的变化规律,与键能无关的是( )①HF、HCl、HBr、HI的热稳定性依次减弱
②NH3易液化
③F2、Cl2、Br2、I2的熔、沸点逐渐升高
④H2S的熔、沸点小于H2O的熔、沸点
⑤NaF、NaCl、NaBr、NaI的熔点依次降低
A、①③④ B、③④ C、②③④ D、①②③④17. 有机物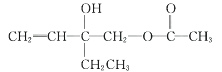 具有手性,发生下列反应后,分子仍有手性的是( )
具有手性,发生下列反应后,分子仍有手性的是( ) ①与H2发生加成反应 ②与乙酸发生酯化反应
③发生水解反应 ④发生消去反应
A、①② B、②③ C、①④ D、②④18. 已知水分子结构可看作H—OH,常温下在水中溶解性最好的是( )A、苯酚 B、甲醇 C、丁醇 D、乙烯19. PtCl2(NH3)2可以形成两种固体,一种为淡黄色,在水中的溶解度较小,另一种为黄绿色,在水中的溶解度较大。请回答下列问题。(1)、PtCl2(NH3)2是(填“平面四边形”或“四面体”)结构。(2)、请在以下横线上画出这两种固体分子的立体构型图:淡黄色固体 , 黄绿色固体。(3)、淡黄色固体物质由(填“极性分子”或“非极性分子”,下同)组成,黄绿色固体物质由组成。(4)、黄绿色固体在水中的溶解度比淡黄色固体的大,原因是 。20. 短周期的5种非金属元素,其中A、B、C的特征电子排布可表示为:A:asa,B:bsbbpb,C:csccp2c,D与B同主族,E在C的下一周期,且是同周期元素中电负性最大的元素。请回答下列问题。(1)、由A、B、C、E四种元素中的两种元素可形成多种分子,下列分子①BC2 ②BA4 ③A2C2 ④BE4,其中属于极性分子的是(填序号)。(2)、C的氢化物比下周期同族元素的氢化物沸点还要高,其原因是。(3)、B、C两元素都能和A元素组成两种常见的溶剂,其分子式为、。DE4在前者中的溶解度(填“大于”或“小于”)在后者中的溶解度。(4)、BA4、BE4和DE4的沸点从高到低的顺序为(填化学式)。(5)、A、C、E三种元素可形成多种含氧酸,如AEC、AEC2、AEC3、AEC4等,以上列举的四种酸其酸性由强到弱的顺序为(填化学式)。