湖北省洪湖市2016-2017学年九年级化学一模(3月月考)考试试卷
试卷更新日期:2018-02-28 类型:中考模拟
一、单选题
-
1. 下列变化中不涉及化学变化的是( )A、生石灰吸水变成粉末 B、用粮食发酵酿酒 C、金刚石刀具切割玻璃 D、用铁矿石在高炉中炼铁2. 下列有关氧气的说法中,不正确的是( )A、用燃烧法来测定空气中氧气的含量,可燃物常用红磷 B、氧气约占空气体积的21% C、用带火星的木条是否复燃来检验氧气 D、鱼能在水中生活,证明氧气易溶于水3. 关于催化剂的下列说法中,正确的是( )A、化学反应后催化剂本身的质量减少 B、化学反应后催化剂本身的质量增加 C、催化剂可改变化学反应速率 D、化学反应后催化剂的化学性质发生变化4. 下列说法正确的是( )A、空气是由空气分子构成的 B、墙内开花墙外香说明分子在不断运动 C、含有氧元素的化合物都是氧化物 D、不同种元素最本质的区别是中子数不同5. 野外生存训练课上,某同学设计了几种获得饮用水的方法,其中最不合理的是( )A、融化积雪,煮沸后使用 B、用沙子和木炭处理海水,煮沸后使用 C、过滤泥水,煮沸后使用 D、收集雨水,煮沸后使用6. 水在通电条件下生成氢气和氧气,下列有关叙述错误的是( )A、水是由氢元素和氧元素组成的 B、水是由氢原子和氧原子构成的 C、分子在化学变化中可以再分 D、原子是化学变化中的最小粒子7. 等质量的镁、铝、锌分别与相同质量20%的盐酸充分反应,产生氢气的质量大小关系的猜测:①Al>Mg>Zn; ②Al=Mg=Zn; ③Al=Mg>Zn; ④Al=Zn>Mg; ⑤Al>Mg=Zn.其中错误的个数为( )A、5个 B、2个 C、3个 D、4个8. 金属R放入稀硫酸中,没有气泡产生,放入硫酸铜溶液中,表面有红色物质析出。下列关于R的金属活动性判断不正确的是( )A、R>Cu B、R>Mg C、Zn>R D、R>Ag9. 某化学小组向一定量AgNO3 和Cu(NO3)2的混合溶液中加入一定量的Zn粉,充分反应后过滤得溶液A和固体B,滤液A中所含的溶质不可能的情况是( )A、Zn(NO3)2 B、Zn(NO3)2 、Cu(NO3)2 、AgNO3 C、Zn(NO3)2 、Cu(NO3)2 D、Zn(NO3)2 、AgNO310. 两个烧杯中装有等质量的金属锌和镁,然后分别逐渐加入同浓度的稀硫酸,产生氢气的质量与加入硫酸的质量关系如图所示。下列说法正确的是( )
 A、a点时,两个烧杯中的酸都恰好完全反应 B、b点时,两个烧杯中产生氢气的质量相同 C、c点时,两个烧杯中都有金属剩余 D、该图反映出镁比锌的金属活动性强11. 要将一瓶接近饱和的石灰水变成饱和溶液,小明选择了如下方法,其中可行的是( )
A、a点时,两个烧杯中的酸都恰好完全反应 B、b点时,两个烧杯中产生氢气的质量相同 C、c点时,两个烧杯中都有金属剩余 D、该图反映出镁比锌的金属活动性强11. 要将一瓶接近饱和的石灰水变成饱和溶液,小明选择了如下方法,其中可行的是( )①加入CaO;②加入Ca(OH)2 ;③升高温度;④降低温度
A、②③ B、②④ C、①②④ D、①②③12. 高氯酸钾(KClO4)可用作火箭推进剂,其溶解度如下表,下列说法正确的是( )温度/℃
20
40
60
80
溶解度/g
1.68
3.73
7.3
13.4
A、高氯酸钾的溶解度随温度升高而减小 B、20℃时,将2g高氯酸钾溶解于98g水可配制2%的溶液 C、60℃时,高氯酸钾饱和溶液中溶质的质量分数是7.3% D、80℃的高氯酸钾饱和溶液冷却至40℃有结晶现象二、填空题
-
13. 用适当的化学方程式说明或解释下列问题:(1)、铜的金属活动性比银强;(2)、工业制二氧化碳;(3)、用石灰浆粉刷墙面,干燥后变得坚硬;(4)、高炉炼铁的主要反应原理。14. 氧原子的结构示意图如图所示:
 (1)、该元素的原子核内质子数为;在化学反应中该原子容易电子(填“得到”或“失去”),其化合价通常为价。(2)、由该元素组成的一种气体单质能供给呼吸,写出实验室制取该气体的一个化学方程式。15. 甲、乙、丙三种固体物质的溶解度曲线如下图所示。据图回答问题:
(1)、该元素的原子核内质子数为;在化学反应中该原子容易电子(填“得到”或“失去”),其化合价通常为价。(2)、由该元素组成的一种气体单质能供给呼吸,写出实验室制取该气体的一个化学方程式。15. 甲、乙、丙三种固体物质的溶解度曲线如下图所示。据图回答问题: (1)、80℃时,甲物质的溶解度是。
(1)、80℃时,甲物质的溶解度是。
(2)、t2℃时,把甲、乙、丙三种物质的饱和溶液降温到t1℃,溶质质量分数不变的是。(3)、t2℃时,把20g 乙物质加到50g水中,充分搅拌后所得溶液的质量是g;若要让乙物质从它的饱和溶液中全部结晶析出,应采取的方法是。
16. 有图所示的仪器和KClO3、MnO2、稀H2SO4、石灰石、稀盐酸等药品供选择,若在实验室完成如下实验.请填写下列空白处: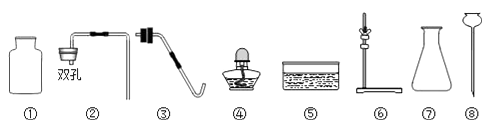 (1)、制取并收集CO2气体,你选择的仪器和药品是(仪器填序号).(2)、若再补充一种药品,也可用上述制CO2的装置来制O2 , 你补充的药品是 .(3)、若再补充一种仪器,并选择上述原有的仪器和药品制取并收集O2 , 你认为需要补充的仪器是 , 你选择的药品是 .
(1)、制取并收集CO2气体,你选择的仪器和药品是(仪器填序号).(2)、若再补充一种药品,也可用上述制CO2的装置来制O2 , 你补充的药品是 .(3)、若再补充一种仪器,并选择上述原有的仪器和药品制取并收集O2 , 你认为需要补充的仪器是 , 你选择的药品是 .三、推断题
-
17. 由C、H、O、Fe四种元素组成的初中常见物质间有如下图所示的关系,其中A、B、C是单质,甲、乙是化合物。图中“—”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质。部分反应物、生成物及反应条件略去。请回答下列问题:

写出下列物质的化学式:A、C、甲;写出A→B反应的化学方程式
四、流程题
-
18. 黄铜是以Zn为主要添加元素的铜合金。黄铜渣中约含Zn 7%、ZnO 31%、Cu 50%、CuO 5%,其余为杂质。处理黄铜渣可得到硫酸锌,其主要流程如下(杂质不溶于水、也不参与反应):
已知:ZnO+H2SO4=ZnSO4+H2O CuO+H2SO4=CuSO4+H2O
 (1)、步骤Ⅰ中产生气体的化学方程式。(2)、溶液A中的金属阳离子有(填化学用语)。(3)、步骤Ⅰ、Ⅱ中均包含的操作名称为。
(1)、步骤Ⅰ中产生气体的化学方程式。(2)、溶液A中的金属阳离子有(填化学用语)。(3)、步骤Ⅰ、Ⅱ中均包含的操作名称为。
(4)、溶液A(填“大于”、“小于”或“等于”)溶液C的质量。五、简答题
-
19. 已知碳酸亚铁在隔绝空气的条件下,受热易分解生成氧化亚铁和二氧化碳;在空气中加热,则生成氧化铁和二氧化碳。某化学兴趣小组用下图所示的装置模拟炼铁过程,并测定某样品中碳酸亚铁的含量(该装置气密性良好,B中氢氧化钠溶液足量)。
 实验过程中,先打开K通入一氧化碳再加热;装置A中固体质量不再减少后,停止加热,待装置A冷却到室温后关闭K;实验测得装置A中固体质量减少了a g,装置B中液体质量增加了b g。请回答下列问题:(1)、写出装置A中发生反应的化学方程式、。(2)、能判断生成的二氧化碳全部被装置B吸收的依据是:装置B且装置C。(3)、若生成的二氧化碳全部被装置B吸收,不考虑水的蒸发且该样品中所含杂质不参加反应,则a b(填“>”、“=”或“<”)。(4)、D处为收集尾气的装置,应选择装置(填“甲”、“乙”或“丙”)。
实验过程中,先打开K通入一氧化碳再加热;装置A中固体质量不再减少后,停止加热,待装置A冷却到室温后关闭K;实验测得装置A中固体质量减少了a g,装置B中液体质量增加了b g。请回答下列问题:(1)、写出装置A中发生反应的化学方程式、。(2)、能判断生成的二氧化碳全部被装置B吸收的依据是:装置B且装置C。(3)、若生成的二氧化碳全部被装置B吸收,不考虑水的蒸发且该样品中所含杂质不参加反应,则a b(填“>”、“=”或“<”)。(4)、D处为收集尾气的装置,应选择装置(填“甲”、“乙”或“丙”)。六、计算题
-
20. 某氢氧化钠样品中混有氯化钠,为测定样品中氢氧化钠的质量分数,在20℃时,称取5 g样品,加入27 g水完全溶解后,缓慢加入稀盐酸,至恰好完全反应时,用去10%的稀盐酸36.5 g。(该反应的化学方程式为:NaOH+HCl=NaCl+H2O)
试计算:
(1)、样品中氢氧化钠的质量分数。(2)、反应后所得溶液中溶质的质量分数。(3)、已知20℃时,氯化钠的溶解度为36 g,试通过简单计算确定反应后所得溶液是否为20℃时该溶质的饱和溶液。
-
-
-