江西省会昌县2014-2015学年九年级化学一模考试试卷
试卷更新日期:2018-02-28 类型:中考模拟
一、单选题
-
1. 实验室里几种物质在互相谈论。你认为它们的叙述中属于化学变化的是( )A、试管:同学们不爱惜我,我被摔碎了 B、铁钉:好难受啊,我在潮湿空气中生锈了 C、灯泡:我通电后发光了,给学生带来光明 D、蜡烛:我受热就会熔化,遇冷我又会凝固2. 春光明媚的校园,百花盛开,阵阵花香,沁人心脾。花香四溢的现象主要说明( )A、分子种类发生了变化 B、原子本身发生了改变 C、原子在化学变化中可分 D、分子是不断运动的3. 科学实验中,药品和仪器的存放应符合一定的规范.下列物质存放在对应的容器中,符合规范的是( )
A、碳酸钙固体 B、氢氧化钠溶液
B、氢氧化钠溶液  C、氢气
C、氢气  D、稀盐酸溶液
D、稀盐酸溶液  4. 2014年4月14日,科学家约翰•帕特森向人们展示了一款真正意义上的原子手表,它内置了一个芯片级的铯原子钟,每1000年仅有1秒的误差.已知这种铯原子核内质子数为55,相对原子质量为133,则其核外电子数和中子数分别为( )A、188 55 B、78 78 C、55 78 D、23 555. 化肥对农业的高产丰收具有重要的作用。下列物质中,能用作磷肥的是( )
4. 2014年4月14日,科学家约翰•帕特森向人们展示了一款真正意义上的原子手表,它内置了一个芯片级的铯原子钟,每1000年仅有1秒的误差.已知这种铯原子核内质子数为55,相对原子质量为133,则其核外电子数和中子数分别为( )A、188 55 B、78 78 C、55 78 D、23 555. 化肥对农业的高产丰收具有重要的作用。下列物质中,能用作磷肥的是( )
A、Ca(H2PO4)2 B、NH4Cl C、K2SO4 D、KNO36. 避免家庭装修造成室内空气污染已经成为一个热门话题,经研究发现,纳米级新型材料TiOX能够有效除去因为装修带来的多种有害气体。已知Ti的化合价是+4,则X是( )A、1 B、2 C、3 D、47. 银制容器在空气中放置一段时间后表面会变黑,原因是银和空气中的微量硫化物等物质发生反应,其化学反应方程式为4Ag + 2H2S + O=2X+ 2H2O,则X的化学式为( )A、AgS B、Ag2O C、Ag2S D、Ag2O28. 化学小组利用如图所示的实验装置测定空气中氧气的含量(部分固定装置已略去,注射器内装有50mL水,导管中的空气可忽略),关于该实验有下列说法:
①向烧杯中加水是为了提高烧杯内的温度;
②白磷燃烧会放出大量的白雾;
③白磷的量不足,会使测定的结果偏大;
④实验中可观察到,注射器的活塞先向右移动,后向左移动;
⑤若试管内净容积为50mL,反应后冷却至室温,活塞停止在40mL附近.其中正确的是( )
A、①④⑤ B、①②③ C、②③⑤ D、③④⑤9. 推理是一种重要的化学思维方法,以下推理合理的是( )
A、酸碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 B、酸溶液中都含有氢离子,所以含有氢元素的物质一定是酸 C、有机物都含有碳元素,所以含有碳元素的化合物一定是有机物 D、化合物是由不同元素组成的纯净物,所以只含一种元素的物质一定不是化合物10. 下列四个装置都能制取二氧化碳,其中能随时控制反应的发生和停止的是( )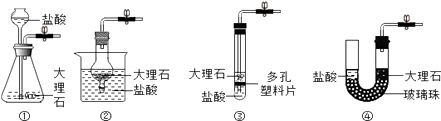 A、①②④ B、①③④ C、①②③ D、②④11. 为改善中小学生营养状况,我县农村学校实施了“蛋奶工程”和“营养午餐”。某校的“营养午餐”含有下列食品,其中含蛋白质丰富的是
A、①②④ B、①③④ C、①②③ D、②④11. 为改善中小学生营养状况,我县农村学校实施了“蛋奶工程”和“营养午餐”。某校的“营养午餐”含有下列食品,其中含蛋白质丰富的是A.小炒青菜 B.肉酿豆腐 C.红烧猪肉 D.
12. 2014年6月10日是“全国低碳日”,“节能减排,低碳生活”的主题旨在倡导节约能源和利用清洁能源,减少温室气体二氧化碳的排放。下列做法符合“主题是
A.提倡焚烧树叶增加肥料 B.推广使用一次性竹筷
C.提倡使用太阳能热水器 D
13. 番茄中含有大量的维生素C(化学式为C6H8O6)。维生素C能有效预防牙龈出血,但它遇空气或加热都易引起变质。下列说法正确的是A.蒸熟的番茄可以补充大量维生素C
B.维生素C由6个碳原子、8个氢原子和6个氧原子构成
C.鲜榨的番茄汁密封保存可减少维生素C的流失
D.维生素C中氧元素的质量分数为
14. 如图所示装置,将X滴加到固体Y中,U形管中的液面变得右高左低,则X、Y对应的试剂组是
 15. 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是
15. 等质量的M、N两种金属,分别与相同质量分数的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气质量和反应时间的关系如图所示,下列叙述正确的是
A.相对原子质量较大的是N
B.生成H2的质量M<N
C.M、N两种金属中较活泼的是N
D.
二、填空题
-
16. 化学学科有自己独特的语言。请用数字和化学符号填空:
(1)、2个银原子;(2)、天然气主要成分;(3)、5个钠离子;(4)、3个水分子;(5)、2个铵根离子 ;(6)、 17. 认识物质是化学学习的重要内容。
17. 认识物质是化学学习的重要内容。从①氮气 ②二氧化硫 ③一氧化碳 ④氯化钠 ⑤氢 氧化钙 ⑥碳酸钠
等六种物质中,选出符合题意的物质,用序号填空:
(1)、常用的调味品是;(2)、在食品中,常用作保护气的是;(3)、用于改良酸性土壤的是;(4)、污染空气,形成酸雨的是;(5)、吸烟产生的一种有害气体;(6)、广泛用于玻璃生产的是。18. 我县自来水的处理过程如图所示: (1)、步骤①网格净水原理类似于操作;(2)、步骤②所起的作用是 (填序号);A、杀死水中的细菌 B、加快过滤速度 C、使泥沙沉积至底部 D、分解有毒物质(3)、步骤④中的消毒剂除氯气以外,还可用一氯胺(NH2Cl)、二氧化氯等物质。
(1)、步骤①网格净水原理类似于操作;(2)、步骤②所起的作用是 (填序号);A、杀死水中的细菌 B、加快过滤速度 C、使泥沙沉积至底部 D、分解有毒物质(3)、步骤④中的消毒剂除氯气以外,还可用一氯胺(NH2Cl)、二氧化氯等物质。①二氧化氯的化学式为。
②NH2Cl中氮、氢、氯三种元素的质量比是(结果以最简整数比表示)。
(4)、生活中将自来水软化的常用方法是 , 区分软水和硬水的试剂是 。19. 如图为A、B、C三种物质的溶解度曲线。 (1)、t2℃时,A、B、C三种物质的溶解度由大到小顺序是;(2)、m点的含义是:;(3)、20℃时,将30g A物质放入50g水中,充分搅拌,所得溶液质量为g;(4)、t2℃时,将等质量的A、B、C饱和溶液分别降温到0℃时,析出溶质最多的是 , 无溶质析出的是;20. A、B、C、D、E是初中化学常见的物质,它们之间的转化关系如左下图所示,部分反应条件、反应物及生成物已略去。下图所示的是A、B、D、E的相关信息(重叠部分表示两种物质的共同点)。请回答下列问题:
(1)、t2℃时,A、B、C三种物质的溶解度由大到小顺序是;(2)、m点的含义是:;(3)、20℃时,将30g A物质放入50g水中,充分搅拌,所得溶液质量为g;(4)、t2℃时,将等质量的A、B、C饱和溶液分别降温到0℃时,析出溶质最多的是 , 无溶质析出的是;20. A、B、C、D、E是初中化学常见的物质,它们之间的转化关系如左下图所示,部分反应条件、反应物及生成物已略去。下图所示的是A、B、D、E的相关信息(重叠部分表示两种物质的共同点)。请回答下列问题: (1)、C的化学式为 ;(2)、反应④的现象是;(3)、反应①的化学方程式为;(4)、反应②的化学方程式 , 其基本反应类型为。21. 在复习氧气、二氧化碳制取和性质时,某小组同学收集了以下装置进行气体制取和性质的练习编制,请你来解答。
(1)、C的化学式为 ;(2)、反应④的现象是;(3)、反应①的化学方程式为;(4)、反应②的化学方程式 , 其基本反应类型为。21. 在复习氧气、二氧化碳制取和性质时,某小组同学收集了以下装置进行气体制取和性质的练习编制,请你来解答。 (1)、写出图中标号①的仪器名称:;(2)、实验室用高锰酸钾制取并收集氧气应选用的装置是(填序号,下同),反应的化学方程式为 . 检验装置气密性时,除了用手紧握的方法外,还可以采用的方法是;(3)、实验室可用氧化钙固体与浓氨水在常温下混合制取少量氨气,为了得到平稳的氨气流,应选择的发生装置是;(4)、为验证二氧化碳的性质,王露将制取的气体通入H装置中,能观察到H中有气泡逸出且溶液变浑浊,则该气体是从(选填“a”或“b”)通入装置H的,产生该现象的化学方程式为;22. 张华同学对酸、碱、盐的知识进行了以下的梳理。(1)、填写下表空格中的化学式。
(1)、写出图中标号①的仪器名称:;(2)、实验室用高锰酸钾制取并收集氧气应选用的装置是(填序号,下同),反应的化学方程式为 . 检验装置气密性时,除了用手紧握的方法外,还可以采用的方法是;(3)、实验室可用氧化钙固体与浓氨水在常温下混合制取少量氨气,为了得到平稳的氨气流,应选择的发生装置是;(4)、为验证二氧化碳的性质,王露将制取的气体通入H装置中,能观察到H中有气泡逸出且溶液变浑浊,则该气体是从(选填“a”或“b”)通入装置H的,产生该现象的化学方程式为;22. 张华同学对酸、碱、盐的知识进行了以下的梳理。(1)、填写下表空格中的化学式。氯化钾
氯化钙
氯化钠
氯化镁
氯化铝
氯化锌
氯化亚铁
氯化铜
KCl
CaCl2
NaCl
MgCl2
ZnCl2
FeCl2
思考:根据以上盐中的金属元素的排列,可以得出他是依据顺序归纳整理的。
(2)、为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了如图。请你在右边的圆圈中填入适当的化学式或离子符号: (3)、张华同学发现酸、碱、盐之间的反应都有盐类物质生成。请写出一个能生成MgCl2的复分解反应的化学方程式:。(4)、我们知道溶液酸碱度pH可显示的溶液的酸碱性;酸溶液pH<7,溶液显酸性;碱溶液pH>7,溶液显碱性.提出问题:盐溶液的pH怎样呢?盐溶液显什么性呢?
(3)、张华同学发现酸、碱、盐之间的反应都有盐类物质生成。请写出一个能生成MgCl2的复分解反应的化学方程式:。(4)、我们知道溶液酸碱度pH可显示的溶液的酸碱性;酸溶液pH<7,溶液显酸性;碱溶液pH>7,溶液显碱性.提出问题:盐溶液的pH怎样呢?盐溶液显什么性呢?猜想与假设:盐溶液的pH可能为:pH=7、pH<7、pH>7.
设计与实验:下列是两同学分别对相同的NaCl溶液、CuSO4溶液、K2CO3溶液的pH进行的测定实验:甲同学:取pH试纸放在玻片上,用玻棒蘸取测试液滴在pH试纸上,试纸显色后与pH标准比色卡比较.乙同学:取pH试纸放在玻片上,用蒸馏水将pH试纸润湿,再用玻棒蘸取测试液滴在pH试纸上,试纸显色后与pH标准比色卡比较.
记录数据:下表是两同学记录所测pH的实验数据:
NaCl溶液
CuSO4溶液
K2CO3溶液
甲同学
7
4
10
乙同学
7
5
9
结论:通过测定几种盐溶液的pH,可以得出的结论是: .
评价与反思:上述两同学测得的数据,反映了溶液真实pH的是同学。
三、实验探究题
-
23. 某教师设计的创新实验装置图如下,请完成下列探究:
 (1)、【实验内容】在500 mL的烧杯中放一金属圆柱体,注入400 mL热水,在圆柱体上放一小块白磷。在烧杯上盖一薄铜片,铜片的一端放一小堆红磷,另一端放一小块用滤纸吸干水后的白磷,观察。
(1)、【实验内容】在500 mL的烧杯中放一金属圆柱体,注入400 mL热水,在圆柱体上放一小块白磷。在烧杯上盖一薄铜片,铜片的一端放一小堆红磷,另一端放一小块用滤纸吸干水后的白磷,观察。【实验现象】铜片上的白磷燃烧,红磷不燃烧,能说明的燃烧条件是;铜片上的白磷燃烧后,用一小烧杯罩在白磷上方,燃烧就停止,说明灭火的可以采用 原理;取下铜片后,用一支空试管向下罩住水中的金属圆柱体,水中白磷燃烧,其化学方程式是 ;
(2)、【分析讨论】①铜片上放一小块白磷时,用滤纸将其表面的水吸干,原因是。
②铜片上的白磷燃烧后,用一小烧杯罩在白磷上方,最好在烧杯内壁沾一些水,其原因是。
(3)、【教师反思】教材P124[实验7-1]是一个对照鲜明,现象明显的探究实验。但是,该实验也存在不足。为了克服不足,在教学中,我对该实验进行的改进,改进后的优点有(写出一条即可)
四、简答题
-
24. 日常生活中接触的金属材料,大多属于合金。其中黄铜是以锌作主要添加元素的铜合金。已知组成某弹壳的黄铜中只含有锌和铜,现将22g该弹壳碾成粉末后放入盛有足量的稀硫酸烧杯中,测得反应过程中生成的氢气的质量(单位为g)与反应时间(单位为min)的关系如图所示。试计算:
 (1)、由题意可知,反应生成氢气的质量共g;(2)、弹壳中铜的质量(精确至0.1)(3)、若欲计算反应后所得溶液的质量,你认为至少还应该补充的一个条件是。
(1)、由题意可知,反应生成氢气的质量共g;(2)、弹壳中铜的质量(精确至0.1)(3)、若欲计算反应后所得溶液的质量,你认为至少还应该补充的一个条件是。
-