2017-2018学年新人教版必修二 高中化学第二章化学反应与能量2.2化学能与电能
试卷更新日期:2018-01-23 类型:同步测试
一、选择题
-
1. 有关原电池的下列说法中正确的是( )A、在外电路中电子由正极流向负极 B、在原电池中负极发生还原反应 C、原电池工作时,阳离子向正极方向移动 D、原电池中正极一定是不活泼金属2. 对化学电源的叙述正确的是( )A、化学电源比火力发电对化学能的利用率高 B、化学电源所提供的电能居于人类社会现阶段总耗电量的首位 C、化学电源均是安全、无污染的 D、化学电源即为可充电电池3. 下列说法中正确的是( )
①燃料电池的反应物可不储存在电池的内部 ②锌锰干电池是一次电池,铅蓄电池是二次电池 ③锂电池是新一代可充电电池 ④燃料电池作为汽车驱动能源已研制成功
A、②③④ B、①②③④ C、①②③ D、①③④4. 如右图所示装置,电流表指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )
A、A是Zn,B是Cu,C为稀硫酸 B、A是Cu,B是Zn,C为稀硫酸 C、A是Fe,B是Ag,C为稀AgNO3溶液 D、A是Ag,B是Fe,C为稀AgNO3溶液5. 将纯锌片和纯铜片按图所示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是( ) A、两烧杯中铜片表面均无气泡产生 B、甲中铜片是正极,乙中铜片是负极 C、两烧杯中溶液的pH均增大 D、产生气泡的速度甲比乙慢6. 有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
A、两烧杯中铜片表面均无气泡产生 B、甲中铜片是正极,乙中铜片是负极 C、两烧杯中溶液的pH均增大 D、产生气泡的速度甲比乙慢6. 有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
由此可判断这四种金属的活动性顺序是( )
A、a>b>c>d B、b>c>d>a C、d>a>b>c D、a>b>d>c7. 按下图装置进行实验,若x轴表示流入正极的电子的物质的量,则y轴可以表示( )
①c(Ag+) ②c(NO3-) ③a棒的质量 ④b棒的质量 ⑤溶液的质量
A、①③ B、②④ C、①③⑤ D、②④⑥8. 已知空气—锌电池的电极反应为锌片:Zn+2OH--2e-=ZnO+H2O;
碳棒:O2+H2O+2e-=2OH- ,
据此判断,锌片是( )
A、正极并被还原 B、正极并被氧化 C、负极并被还原 D、负极并被氧化9. 燃料电池是燃料(如CO、H2、CH4等)跟氧气(或空气)起反应将化学能转变为电能的装置,若电解质溶液是强碱溶液,下面关于甲烷燃料电池的说法正确的是( )A、负极反应式:O2+2H2O+4e-=4OH- B、负极反应式:CH4+8OH--8e-=CO2+6H2O C、随着放电的进行,溶液的氢氧根浓度不变 D、放电时溶液中的阴离子向负极移动10. 废电池处理不当不仅造成浪费,还会对环境造成严重污染,对人体健康也存在极大的危害。有同学想变废为宝,他的以下想法你认为不正确的是( )A、把锌皮取下洗净用于实验室制取氢气 B、碳棒取出洗净用作电极 C、把铜帽取下洗净回收利用 D、电池内部填有NH4Cl等化学物质,将废电池中的黑色糊状物作化肥施用二、非选择题
-
11. 由A、B、C、D四种金属按下表中装置进行实验。
装置
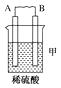
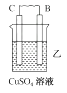
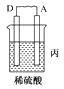
现象
二价金属A
不断溶解
C的质量增加
A上有气体产生
根据实验现象回答下列问题:
(1)、装置甲中负极的电极反应式是。(2)、装置乙中正极的电极反应式是。(3)、装置丙中溶液的pH(填“变大”“变小”或“不变”)。(4)、四种金属活动性由强到弱的顺序是。12. 利用反应Cu+2FeCl3=CuCl2+2FeCl2 , 设计一个原电池。
(1)、选用为负极,为正极,电解质溶液为。(2)、写出电极反应式:负极 , 正极。(3)、在方框中画出装置图: 13. Zn—MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。(1)、该电池的负极材料是。电池工作时,电子流向(填“正极”或“负极”)。(2)、若ZnCl2—NH4Cl混合溶液中含有杂质Cu2+ , 会加速其电极的腐蚀,其主要原因是。欲除去Cu2+ , 最好选用下列试剂中的(填字母)。
13. Zn—MnO2干电池应用广泛,其电解质溶液是ZnCl2-NH4Cl混合溶液。(1)、该电池的负极材料是。电池工作时,电子流向(填“正极”或“负极”)。(2)、若ZnCl2—NH4Cl混合溶液中含有杂质Cu2+ , 会加速其电极的腐蚀,其主要原因是。欲除去Cu2+ , 最好选用下列试剂中的(填字母)。A.NaOH B.Zn
C.Fe D.NH3·H2O
14. 如下图所示,可形成氢氧燃料电池。通常氢氧燃料电池有酸式(当电解质溶液为硫酸时)和碱式[当电解质溶液为NaOH(aq)或KOH(aq)时]两种。试回答下列问题: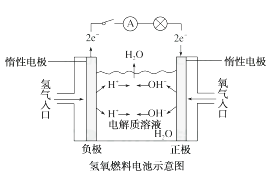 (1)、酸式电池的电极反应:负极 , 正极;电池总反应:;电解质溶液pH的变化(填“变大”、“变小”或“不变”)。(2)、碱式电池的电极反应:负极 , 正极;电池总反应:;电解质溶液pH的变化(填“变大”、“变小”或“不变”)。15. 氢气是未来最理想的能源。科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O 2H2↑+O2↑,制得的氢气可用于制作燃料电池。试回答下列问题:(1)、分解海水时,实现了光能转化为能。生成的氢气用于制作燃料电池时,实现了化学能转化为能。分解海水的反应属于反应(填“放热”或“吸热”)。(2)、某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质, A极上发生的电极反应为2H2+2O2--4e-=2H2O,则A极是电池的极,电子从该极(填“流入”或“流出”)。B极电极反应式为。
(1)、酸式电池的电极反应:负极 , 正极;电池总反应:;电解质溶液pH的变化(填“变大”、“变小”或“不变”)。(2)、碱式电池的电极反应:负极 , 正极;电池总反应:;电解质溶液pH的变化(填“变大”、“变小”或“不变”)。15. 氢气是未来最理想的能源。科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O 2H2↑+O2↑,制得的氢气可用于制作燃料电池。试回答下列问题:(1)、分解海水时,实现了光能转化为能。生成的氢气用于制作燃料电池时,实现了化学能转化为能。分解海水的反应属于反应(填“放热”或“吸热”)。(2)、某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质, A极上发生的电极反应为2H2+2O2--4e-=2H2O,则A极是电池的极,电子从该极(填“流入”或“流出”)。B极电极反应式为。