上海市浦东新区2016-2017学年九年级上学期化学期末考试试卷
试卷更新日期:2018-01-11 类型:期末考试
一、单选题
-
1. “Hg”的元素名称为( )
A、汞 B、贡 C、银 D、氢2. 地壳中含量最多的元素是( )A、Al B、O C、Fe D、Si3. 鱼类食物富含铁,此处“铁”指的是( )A、元素 B、原子 C、分子 D、单质4. 糖水属于( )A、悬浊液 B、乳浊液 C、溶液 D、纯净物5. 引起酸雨的主要物质是( )A、PM2.5 B、SO2 C、CO2 D、N26. 氧化铟(In2O3)可用于制作触摸屏,其中铟元素(In)的化合价为( )A、0 B、+2 C、+3 D、+67. 取用氯酸钾的仪器是( )A、燃烧匙 B、滴管 C、镊子 D、药匙8. 胆矾的化学式为( )A、CuO B、CuSO4 C、CuSO4·H2O D、CuSO4·5H2O9. 属于纯净物的是( )A、矿泉水 B、自来水 C、蒸馏水 D、石灰水10. 表示两个氢分子的是( )A、2H B、2H2 C、H D、H211. 自然界中存在氧循环和碳循环,其中能将二氧化碳转化为氧气的是( )A、燃料燃烧 B、光合作用 C、溶洞形成 D、动物呼吸12. 反应3C+4NH3 3CH4+2X可将树木纤维素转变为储能装置,其中X的化学式为( )A、N2 B、H2 C、C2H4 D、C2H213. 在反应H2+CuO Cu+H2O中,氧化剂是( )A、Cu B、H2O C、CuO D、H214. 将饱和硝酸钾溶液转化为不饱和溶液的方法是( )A、加水 B、降温 C、蒸发水 D、加溶质15. 物质在氧气中燃烧的现象,描述正确的是( )A、铁丝:火星四射 B、木炭:蓝色火焰 C、镁带:生成氧化镁 D、硫粉:黄色火焰16. 正确的化学方程式是( )A、4Fe+3O2 2Fe2O3 B、S+O2 SO2 C、H2+O2 H2O D、C+O2 CO2↑17. 物质的“性质——用途”对应关系错误的是( )A、一氧化碳有还原性——冶炼金属 B、石墨质地软且滑腻——制作电极 C、稀有气体通电发光——制霓虹灯 D、生石灰能与水反应——作干燥剂18. 天然气的主要成分是甲烷(CH4),有关描述正确的是( )A、甲烷的摩尔质量是20g/mol B、甲烷是由碳、氢原子构成的 C、1mol甲烷中含有4个氢原子 D、1 mol甲烷约含6.02×1023个甲烷分子19. 下图是某化学反应的微观示意图,“ ”、“
”、“  ”代表不同元素的原子。有关描述错误的是( )
”代表不同元素的原子。有关描述错误的是( ) A、反应物均为单质 B、化学变化的实质是原子重新组合 C、反应前后元素的存在形态发生改变 D、该示意图可以反映电解水的微观过程20. 用下图装置探究碳及其氧化物的性质,有关说法错误的是( )
A、反应物均为单质 B、化学变化的实质是原子重新组合 C、反应前后元素的存在形态发生改变 D、该示意图可以反映电解水的微观过程20. 用下图装置探究碳及其氧化物的性质,有关说法错误的是( )
A. 若通入气体一氧化碳,M处为氧化铜,加热前应先通一段时间纯净的一氧化碳
B. 若通入气体二氧化碳,M处为木炭,可观察到玻璃管中黑色粉末逐渐减少
C. 若M处为木炭和氧化铜(密封玻璃管左端),澄清石灰水的作用是检验二氧化碳
D. 在A、若通入气体一氧化碳,M处为氧化铜,加热前应先通一段时间纯净的一氧化碳 B、若通入气体二氧化碳,M处为木炭,可观察到玻璃管中黑色粉末逐渐减少 C、若M处为木炭和氧化铜(密封玻璃管左端),澄清石灰水的作用是检验二氧化碳 D、在A、B选项的实验中,a处点燃尾气的目的完全相同二、填空题
-
21. 人类生活离不开空气和水土资源。
① 在空气的成分中,能供给呼吸的是 , 约占空气体积78%的是 , 会引起温室效应的是;
② 浦东“8424”西瓜特别脆甜,这与土壤中某些矿物质含量适宜有关。如硅酸锌(Zn2SiO4),它是由种元素组成,其中锌、硅、氧元素的原子个数比为;
③ 家用净水器中常使用活性炭,主要利用了它的性。电解水实验揭示了水的组成,写出反应的化学方程式 , 在该实验中若正极产生3mL气体,负极产生气体体积约为 mL,检验氧气的操作及现象是。
22. 下表是NaCl、KClO3在不同温度下的溶解度(单位:g/100g水)。温度(℃)
0
20
40
60
80
100
S(NaCl)
35.7
36.0
36.6
37.3
38.4
39.8
S(KClO3)
3.3
7.3
13.9
23.8
37.5
56.3
① 20℃时,NaCl的溶解度为 g/100g水;
②40℃时,将10gKClO3放入100g水中充分溶解,所得溶液溶质质量分数为(最简分数);
③ “海水晒盐”利用的方法是(填“蒸发结晶”或“降温结晶”);
④ 工业上用氯化钠溶液制备氯酸钾,主要流程如下:

(第Ⅱ步中发生的反应:NaClO3+KCl→NaCl+KClO3)
上述流程中,氯化钠溶液中的水是否参与第Ⅰ步化学反应?(填“是”或“否”)。
溶液A中的溶质除NaCl外,还含有(填化学式)。
三、实验探究题
-
23. 以下改进实验能够更好地达成实验目的。

①图1实验说明了二氧化碳具有的性质是;
②按图2所示进行实验可以制取氧气,用启普发生器制取氧气的优点是(写一点),写出该反应的化学方程式;
③图3实验证明了可燃物燃烧的条件之一为 , 写出白磷燃烧的化学方程式;
④待图3实验结束后,将甲试管从烧杯中取出并按下图进行实验。若白磷足量,理论上进入试管中的水的体积约占试管容积的。 24. 根据题意回答。
24. 根据题意回答。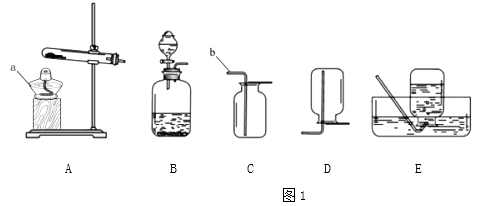
①写出仪器名称:a , b;
②实验室用氯酸钾和二氧化锰的混合物制取氧气,可选择的一组装置是(填编号)写出反应的化学方程式;
③下图是检查装置气密性的过程。最终在F处观察到的现象是(选填“甲~丁”);
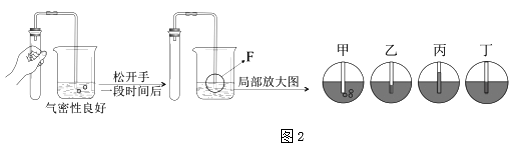
④ 资料表明:高铁酸钾(K2FeO4)固体也能用于制取氧气,原理如下:
方案一:4K2FeO4 2Fe2O3+4K2O+3O2↑
方案二:4K2FeO4+10H2O→4Fe(OH)3↓+8KOH+3O2↑
Ⅰ.关于以上方案说法错误的是
a.方案一是分解反应
b.方案二更节能简便
c.方案一、二均可在图1的装置B中进行实验
d.制取等质量的氧气,两种方案所需高铁酸钾的质量相等
Ⅱ.若用方案一(4K2FeO4 2Fe2O3+4K2O+3O2↑)制取0.3mol氧气,需要高铁酸钾的物质的量为 mol(根据化学方程式列式计算)。
25. “数字化实验”丰富了实验研究的方法,它可将实验过程中某些因素(酸碱性、气压等)的变化以数据、图像的形式呈现出来。请回答:探究二氧化碳与水的反应

Ⅰ.图1中可观察到甲试管中的紫色液体变为色,写出发生反应的化学方程式 , 乙试管的作用是;
Ⅱ.由图2坐标图中的曲线可知,烧杯内溶液的酸性逐渐变(填“强”或“弱”)。
探究蜡烛燃烧的产物

Ⅰ.如图3所示,用注射器在蜡烛外焰部位抽气并振荡,可观察到 , 证明反应生成了二氧化碳;若将干冷的烧杯罩在火焰上方,观察到 , 证明反应生成了水。
Ⅱ.如图4所示,蜡烛在密闭容器内燃烧,同时监测容器内氧气、二氧化碳和水蒸气含量的变化,形成三条曲线如坐标图所示,曲线(选填“a”、“b”、“c”)能够说明蜡烛燃烧生成了二氧化碳和水。
③ 比较块状碳酸钙、碳酸钙粉末与稀盐酸反应的速度

Ⅰ.写出碳酸钙与稀盐酸发生反应的化学方程式;
图5中,乙试管中稀盐酸的浓度C%应为;
较之块状碳酸钙,碳酸钙粉末与稀盐酸的反应更为剧烈,原因是。
Ⅱ.按图6所示进行实验,倾斜锥形瓶使小试管内的稀盐酸流入瓶中与固体接触发生反应,瓶内气压的变化如坐标图所示。对比分析坐标图中的点(选填a~d)可知:两个锥形瓶内达到相同的压强时,碳酸钙粉末与稀盐酸反应所需时间更短。