北京市东城区2015-2016学年高一上学期化学期末考试试卷
试卷更新日期:2018-01-06 类型:期末考试
一、单选题
-
1. 下列物质中,可用于治疗胃酸过多的是( )A、氢氧化铝 B、氯化钠 C、氢氧化钠 D、硫酸钠2. 当光束通过下列分散系时,能观察到丁达尔效应的是( )A、泥浆 B、CuSO4溶液 C、酒精溶液 D、Fe(OH)3胶体3. 氧气的摩尔质量是( )A、32 B、32 g C、32 mol D、32 g·mol-14. 下列金属在冷、浓的硝酸或硫酸中,能形成致密氧化膜的是( )A、Mg B、Fe C、Cu D、Na5. 下列物质不属于合金的是( )A、生铁 B、水银 C、青铜 D、硬铝6. 实验室中配制250 mL 0.10 mol·L-1NaOH溶液时,必须使用到的玻璃仪器是( )A、
 B、
B、 C、
C、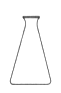 D、
D、 7. 下列物质常用作工业生产制冷剂的是( )A、液氨 B、液氧 C、液氯 D、液氢8. 下列物质不能使品红溶液褪色的是( )A、氯气 B、过氧化钠 C、次氯酸钠 D、氢氧化钠9. 下列物质属于电解质且能导电的是( )A、金属铜 B、碳酸钠晶体 C、硝酸钠溶液 D、熔融氯化钠10. 下列各组物质不能用焰色反应鉴别的是( )A、NaCl和Na2CO3 B、Na2CO3和BaCO3 C、CuCl2和CaCl2 D、Na2O2和K2O211. 下列有关萃取的说法不正确的是( )A、萃取在香料、药物的提取中应用广泛 B、用乙醇作萃取剂,萃取碘水中的碘单质 C、用四氯化碳萃取碘水时,下层溶液呈紫色 D、萃取后的混合物进行分离时,要使用分液漏斗12. 下列有关酸雨的说法不正确的是( )A、在酸雨形成过程中没有发生氧化还原反应 B、二氧化硫、二氧化氮是形成酸雨的主要因素 C、煤和石油的燃烧、汽车尾气等是酸雨污染物的主要来源 D、酸雨的危害有破坏农作物,使土壤、湖泊酸化以及加速建筑物、桥梁的腐蚀等13. 下图是喷泉实验装置图,下列说法正确的是( )
7. 下列物质常用作工业生产制冷剂的是( )A、液氨 B、液氧 C、液氯 D、液氢8. 下列物质不能使品红溶液褪色的是( )A、氯气 B、过氧化钠 C、次氯酸钠 D、氢氧化钠9. 下列物质属于电解质且能导电的是( )A、金属铜 B、碳酸钠晶体 C、硝酸钠溶液 D、熔融氯化钠10. 下列各组物质不能用焰色反应鉴别的是( )A、NaCl和Na2CO3 B、Na2CO3和BaCO3 C、CuCl2和CaCl2 D、Na2O2和K2O211. 下列有关萃取的说法不正确的是( )A、萃取在香料、药物的提取中应用广泛 B、用乙醇作萃取剂,萃取碘水中的碘单质 C、用四氯化碳萃取碘水时,下层溶液呈紫色 D、萃取后的混合物进行分离时,要使用分液漏斗12. 下列有关酸雨的说法不正确的是( )A、在酸雨形成过程中没有发生氧化还原反应 B、二氧化硫、二氧化氮是形成酸雨的主要因素 C、煤和石油的燃烧、汽车尾气等是酸雨污染物的主要来源 D、酸雨的危害有破坏农作物,使土壤、湖泊酸化以及加速建筑物、桥梁的腐蚀等13. 下图是喷泉实验装置图,下列说法正确的是( ) A、烧瓶中的溶液呈红色,则原气体一定是SO2 B、形成喷泉的原因是烧瓶内压强小于外界大气压 C、烧瓶中的溶液呈蓝色,则原气体一定属于碱类物质 D、若将石蕊改成氢氧化钠,则CO、CO2均能形成喷泉14. 下列存放物质的方法不正确的是( )A、用棕色细口试剂瓶存放氯水 B、漂白粉需在密闭容器中保存 C、HF溶液保存在玻璃试剂瓶中 D、NaOH溶液盛装在带橡皮塞的试剂瓶中15. 下列离子方程式书写正确的是( )A、铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+ B、氯化铝溶液与过量的氢氧化钠溶液反应:Al3++3OH-=Al(OH)3↓ C、氯气与氢氧化钠溶液反应:Cl2+2OH-=Cl-+ClO-+H2O D、碳酸氢钠溶液与稀盐酸反应:2H++CO32-=CO2↑+H2O16. 已知阿伏加德罗常数约为6.02×1023 , 下列叙述正确的是( )A、1.8g的NH4+ , 中含有的电子数为0.1×6.02×1023 B、常温常压下,11.2L氯气所含的原子数为6.02×1023 C、常温常压下,18g H2O含有的原子数为3×6.02×1023 D、5.6g金属铁变为离子时失去的电子数为0.2×6.02×102317. 用化学方法区别NaCl、MgCl2、AlCl3、CuCl2、FeCl3和NH4Cl六种溶液(必要时可加热),下列试剂中可选用的是( )A、KSCN溶液 B、AgNO3溶液 C、BaCl2溶液 D、NaOH溶液18. 下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
A、烧瓶中的溶液呈红色,则原气体一定是SO2 B、形成喷泉的原因是烧瓶内压强小于外界大气压 C、烧瓶中的溶液呈蓝色,则原气体一定属于碱类物质 D、若将石蕊改成氢氧化钠,则CO、CO2均能形成喷泉14. 下列存放物质的方法不正确的是( )A、用棕色细口试剂瓶存放氯水 B、漂白粉需在密闭容器中保存 C、HF溶液保存在玻璃试剂瓶中 D、NaOH溶液盛装在带橡皮塞的试剂瓶中15. 下列离子方程式书写正确的是( )A、铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+ B、氯化铝溶液与过量的氢氧化钠溶液反应:Al3++3OH-=Al(OH)3↓ C、氯气与氢氧化钠溶液反应:Cl2+2OH-=Cl-+ClO-+H2O D、碳酸氢钠溶液与稀盐酸反应:2H++CO32-=CO2↑+H2O16. 已知阿伏加德罗常数约为6.02×1023 , 下列叙述正确的是( )A、1.8g的NH4+ , 中含有的电子数为0.1×6.02×1023 B、常温常压下,11.2L氯气所含的原子数为6.02×1023 C、常温常压下,18g H2O含有的原子数为3×6.02×1023 D、5.6g金属铁变为离子时失去的电子数为0.2×6.02×102317. 用化学方法区别NaCl、MgCl2、AlCl3、CuCl2、FeCl3和NH4Cl六种溶液(必要时可加热),下列试剂中可选用的是( )A、KSCN溶液 B、AgNO3溶液 C、BaCl2溶液 D、NaOH溶液18. 下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是( )①Al ②Al2O3③Ca(OH)2④Al(OH)3⑤Na2CO3⑥NaHCO3 .
A、①②③⑤ B、①②④⑥ C、①②⑤⑥ D、②③④⑥19. 向A、B、C和D四支试管中的溶液分别进行表中的操作,通过观察到的实验现象得出的结论正确的是( )操作 现象 结论 A ①滴加稀HNO3
②滴加BaCl2溶液无明显现象
白色沉淀原溶液一定含SO42- B 滴加稀盐酸 有大量气泡产生 原溶液一定含CO32- C ①滴加稀HCl
②滴加AgNO3溶液无明显现象
白色沉淀原溶液一定含Cl- D ①滴加KCSN溶液
②滴加氯水无明显现象
溶液呈红色原溶液一定含Fe2+ A、A B、B C、C D、D20. 用以下三种途径来制取等质量的硝酸铜。( )①铜与稀硝酸反应;
②铜与浓硝酸反应;
③铜先与氧气反应生成氧化铜,氧化铜再跟硝酸反应。以下叙述不正确的是
A、三种途径所消耗铜的质量相等 B、三种途径所消耗硝酸的物质的量是①>②>③ C、途径③的制备方法最符合“绿色化学”理念 D、途径①中被氧化的铜与被还原的硝酸的物质的量之比是3:2二、填空题
-
21. 钠和铝是两种重要的金属。请回答:(1)、将一小块金属钠投入水中,发生反应的化学方程式是;
可观察到的实验现象是(填字母序号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动 d.有嘶嘶声
(2)、加热铝箔,其表面失去光泽,熔化后并不滴落,其原因是。(3)、将铝箔放入氢氧化钠溶液中,反应的离子方程式是 , 。(4)、用铝箔包裹0.1 mol金属钠,用针扎若干小孔后,放入水中,完全反应后,用排水法收集到标准状况下气体的体积(填字母序号)。a.等于1.12 L b.大于1.12 L c.小于1.12 L
22. 自然界中存在着很多的物质循环过程。(1)、下图是自然界中碳、氧循环的示意图。
①图一中,转化1是水吸收二氧化碳的过程,反应的化学反应方程式是。
②图二中,转化1是自然界中碳、氧循环的一个重要反应——绿色植物的光合作用,反应的化学方程式是。
③上述两个反应中的反应物相同,但得到的产物不同,原因是。
(2)、下图是氮循环示意图,请回答下列问题。
①自然界中的固氮和人工固氮的共同点是将氮元素由游离态转化为。
②雷电固氮反应的化学方程式是 , 其中氮元素被(填“氧化”或“还原”)。
③根据循环图判断下列说法不正确的是。
a.氮元素均被氧化
b.工业合成氨属于人工固氮
c.含氮无机物和含氮有机物可相互转化
d.碳、氢、氧三种元素也参与了氮循环
三、实验题
-
23. 下图是实验室制取SO2并验证SO2某些性质的装置图。若观察到装置④中有淡黄色沉淀生成,⑤中的溴水褪色(已知因含有Br2而溴水呈红棕色),请回答:
 (1)、①中发生反应的离子方程式是。(2)、②中的实验现象是。(3)、③的实验现象是 , 证明SO2有性。(4)、④中SO2做剂。(5)、⑤中反应生成两种强酸,该反应的离子方程式是 , 当1 molSO2参与反应时,转移电子的物质的量是。(6)、⑥的作用是。24. NH3经一系列反应可以得到HNO3和NH4NO3 , 如下图所示。
(1)、①中发生反应的离子方程式是。(2)、②中的实验现象是。(3)、③的实验现象是 , 证明SO2有性。(4)、④中SO2做剂。(5)、⑤中反应生成两种强酸,该反应的离子方程式是 , 当1 molSO2参与反应时,转移电子的物质的量是。(6)、⑥的作用是。24. NH3经一系列反应可以得到HNO3和NH4NO3 , 如下图所示。
【资料卡片】i.NH4NO3是一种白色晶体,易溶于水,微溶于乙醇。
ii.在230℃以上时,同时有弱光:2NH4NO3 2N2↑+O2↑+4H2O。
iii.在400℃以上时,剧烈分解发生爆炸:4NH4NO3 3N2↑+2NO2↑+8H2O
(1)、如图将水滴入盛有硝酸铵的试管中,观察到的A处液面上升,B处液面下降,产生该现象的原因是。一段时间后观察到的现象是。 (2)、实验室可以用氯化铵和熟石灰反应来制备氨气,该反应的化学方程式是 , 能否用硝酸铵代替氯化铵,(填“能”或“不能”),理由是。(3)、从反应类型角度分析在Ⅰ~Ⅳ的转化过程中的共同点是;完成反应Ⅳ的化学方程式:NO+H2O NH4++NO3-+H+。25. 分离混合物在工业生产中应用广泛。某含有金属钨(W)、WO2、WO3、W2O5的混合物,欲从该混合物中分离出WO3和W2O5 , 并冶炼金属钨,其流程示意图如下。
(2)、实验室可以用氯化铵和熟石灰反应来制备氨气,该反应的化学方程式是 , 能否用硝酸铵代替氯化铵,(填“能”或“不能”),理由是。(3)、从反应类型角度分析在Ⅰ~Ⅳ的转化过程中的共同点是;完成反应Ⅳ的化学方程式:NO+H2O NH4++NO3-+H+。25. 分离混合物在工业生产中应用广泛。某含有金属钨(W)、WO2、WO3、W2O5的混合物,欲从该混合物中分离出WO3和W2O5 , 并冶炼金属钨,其流程示意图如下。
请阅读资料卡片并回答下列问题。
【资料卡片】
i.WO3易溶于NaOH、Na2CO3和Na2C2O4(草酸钠)溶液并形成钨酸盐(Na2WO4);W2O5易被氧化,也能溶解在上述溶液中;金属钨和WO2不溶于上述溶液。
ii.WO3几乎不与无机酸反应。
iii.钨化合物在不同溶剂中的浸取率见下表(浸取是用溶剂溶解固体混合物,以分离可溶组分及残渣的过程。若浸取率为100%,则固体中的可溶组分全部溶解在溶剂中)。
溶剂
煮沸时间(min)
W2O5(%)
WO3(%)
WO2
金属钨
①100g/L NaOH
25
72.3
100
未检出
未检出
②300g/LNa2CO3
7
76.4
100
③50g/LNa2CO3
30
100
100
④饱和Na2C2O4
60
4.2
100
⑤饱和Na2C2O4
(在CO2气氛下浸取)
120
<0.5
100
(1)、步骤Ⅰ和Ⅳ均要进行的操作是。(2)、步骤Ⅱ、Ⅲ反应的化学方程式分别是、。(3)、WO3既属于金属氧化物,也属于氧化物,与NaOH溶液反应的离子方程式是。(4)、步骤Ⅰ是将WO3分离出来,选用的溶剂a是⑤,理由是。(5)、步骤Ⅳ可将W2O5分离出来,选用的溶剂b是(填序号),固体E中含有的物质是 , D中溶质是。