北京市海淀区2017-2018学年高三上学期化学期中考试试卷
试卷更新日期:2017-12-26 类型:期中考试
一、单选题
-
1. 下列我国古代的技术应用中,不涉及氧化还原反应的是( )A、
 煅烧贝壳
B、
煅烧贝壳
B、 粮食酿醋
C、
粮食酿醋
C、 古法炼铁
D、
古法炼铁
D、 火药爆炸
2. “一带一路”贸易使国外的特色产品走入百姓的日常生活。下列商品的主要成分所对应的材料类型不正确的是( )
火药爆炸
2. “一带一路”贸易使国外的特色产品走入百姓的日常生活。下列商品的主要成分所对应的材料类型不正确的是( ) A、A B、B C、C D、D3. 下列关于硅及其化合物的说法不正确的是( )A、高纯硅具有良好的半导体性能,可制成硅芯片、光电池、光导纤维等 B、二氧化硅能与氢氟酸反应,可用氢氟酸刻蚀玻璃 C、向硅酸钠溶液中滴加稀盐酸有不溶物生成,实验室可用该方法制备硅酸 D、“硅胶”由硅酸凝胶经干燥、脱水制得,常用作袋装食品的干燥剂4. 常温下,下列各组离子在指定溶液中一定能大量共存的是( )A、pH=1的溶液中:HCO3-、SO42-、K+、Cl- B、遇酚酞变红的溶液中:NO3-、Na+、AlO2-、K+ C、c(NO3-)=1 mol•L-1的溶液中:H+、Fe2+、Cl-、NH4+ D、无色透明溶液中:K+、SO42-、Na+、MnO4-5. 通常工业上监测SO2含量是否达到排放标准的化学反应原理是SO2+ H2O2+ BaCl2= BaSO4↓+ 2HCl ,用NA表示阿伏加德罗常数的值,下列说法不正确的是( )A、0.1 molBaCl2中所含离子总数约为0.3 NA B、25℃时,pH=l的HCl溶液中含有H+的数目约为0.1 NA C、标准状况下,17gH2O2中所含电子总数约为9 NA D、生成2.33gBaSO4沉淀时,吸收SO2的体积在标准状况下约为0.224L6. 下图表示自然界中的氮循环,相关说法正确的是( )
A、A B、B C、C D、D3. 下列关于硅及其化合物的说法不正确的是( )A、高纯硅具有良好的半导体性能,可制成硅芯片、光电池、光导纤维等 B、二氧化硅能与氢氟酸反应,可用氢氟酸刻蚀玻璃 C、向硅酸钠溶液中滴加稀盐酸有不溶物生成,实验室可用该方法制备硅酸 D、“硅胶”由硅酸凝胶经干燥、脱水制得,常用作袋装食品的干燥剂4. 常温下,下列各组离子在指定溶液中一定能大量共存的是( )A、pH=1的溶液中:HCO3-、SO42-、K+、Cl- B、遇酚酞变红的溶液中:NO3-、Na+、AlO2-、K+ C、c(NO3-)=1 mol•L-1的溶液中:H+、Fe2+、Cl-、NH4+ D、无色透明溶液中:K+、SO42-、Na+、MnO4-5. 通常工业上监测SO2含量是否达到排放标准的化学反应原理是SO2+ H2O2+ BaCl2= BaSO4↓+ 2HCl ,用NA表示阿伏加德罗常数的值,下列说法不正确的是( )A、0.1 molBaCl2中所含离子总数约为0.3 NA B、25℃时,pH=l的HCl溶液中含有H+的数目约为0.1 NA C、标准状况下,17gH2O2中所含电子总数约为9 NA D、生成2.33gBaSO4沉淀时,吸收SO2的体积在标准状况下约为0.224L6. 下图表示自然界中的氮循环,相关说法正确的是( ) A、“雷电作用”中发生的反应是:N2+ 2O2 2NO2 B、“人工固氮”过程中,氮元素一定被还原 C、①中涉及的反应可能有:2NO2-+O2 = 2NO3- D、②中涉及的反应可能有:2NO3-+12H+ = N2+ 6H2O7. 下列有关原子结构及元素周期表的叙述正确的是( )A、第IA族元素钫的两种核素:221Fr比223Fr少2个质子 B、第三周期金属元素的离子半径:r(Na+)< r(Mg2+)<r(Al3+) C、第ⅦA族元素从上到下,单质与氢气化合越来越容易 D、通常可在周期表的过渡元素中寻找化学反应的催化剂8. 下列解释事实的离子方程式正确的是( )A、铜丝溶于浓硝酸生成绿色溶液:3Cu+8H++2NO3-==3Cu2++2NO↑+4H2O B、稀硫酸与Ba(OH)2溶液混合出现浑浊:H++OH-+ Ba2++SO42- =BaSO4↓+H2O C、澄清石灰水中加入过量小苏打溶液出现浑浊:Ca2++ 2HCO3-+2OH-= CaCO3↓+CO32-+ 2H2O D、在AlCl3溶液中加入过量氨水出现浑浊:Al3++3OH-= Al(OH)3↓9. ①~⑥是周期表中第二、三周期的元素,它们的主要化合价和原子半径如下表所示:
A、“雷电作用”中发生的反应是:N2+ 2O2 2NO2 B、“人工固氮”过程中,氮元素一定被还原 C、①中涉及的反应可能有:2NO2-+O2 = 2NO3- D、②中涉及的反应可能有:2NO3-+12H+ = N2+ 6H2O7. 下列有关原子结构及元素周期表的叙述正确的是( )A、第IA族元素钫的两种核素:221Fr比223Fr少2个质子 B、第三周期金属元素的离子半径:r(Na+)< r(Mg2+)<r(Al3+) C、第ⅦA族元素从上到下,单质与氢气化合越来越容易 D、通常可在周期表的过渡元素中寻找化学反应的催化剂8. 下列解释事实的离子方程式正确的是( )A、铜丝溶于浓硝酸生成绿色溶液:3Cu+8H++2NO3-==3Cu2++2NO↑+4H2O B、稀硫酸与Ba(OH)2溶液混合出现浑浊:H++OH-+ Ba2++SO42- =BaSO4↓+H2O C、澄清石灰水中加入过量小苏打溶液出现浑浊:Ca2++ 2HCO3-+2OH-= CaCO3↓+CO32-+ 2H2O D、在AlCl3溶液中加入过量氨水出现浑浊:Al3++3OH-= Al(OH)3↓9. ①~⑥是周期表中第二、三周期的元素,它们的主要化合价和原子半径如下表所示:元素
①
②
③
④
⑤
⑥
主要化合价
+1
+1
+2
-2
-1
-1、+7
原子半径/nrn
0.152
0.186
0.160
0.074
0.071
0.099
下列说法不正确的是
A、①的单质加热时能与氧气化合 B、②的单质常温下可与水剧烈反应 C、③与⑥可以形成离子化合物 D、非金属性④>⑤10. 某实验小组通过下图所示实验探究Na2O2与水的反应: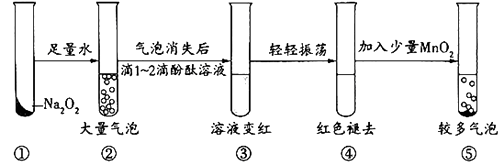
下列说法不正确的是( )
A、②中的大量气泡主要成分是氧气 B、③中溶液变红,说明有碱性物质生成 C、④中现象可能是由于溶液中含有强氧化性物质造成的 D、⑤中MnO2的主要作用是降低了水中氧气的溶解度11. 下列实验操作及现象能够达成相应实验目的的是( )实验目的
实验操作及现象
A
检验Na2SO3溶液是否变质
向Na2SO3溶液中加入Ba(NO3)2溶液,出现白色沉淀,再加入稀硝酸,沉淀不溶解
B
证明酸性条件下H2O2氧化性强于I2
向淀粉KI溶液中滴入3滴稀硫酸,未见溶液变蓝; 再加入10%的H2O2溶液,溶液立即变蓝色
C
证明碳的非金属性强于硅
将浓盐酸滴入Na2CO3固体中,生成的气体通入盛有Na2SiO3溶液的试管中,出现浑浊
D
证明SO2具有漂白性
将SO2通入酸性KMnO4溶液中,溶液紫色褪去
A、A B、B C、C D、D12. 碘循环工艺不仅能吸收SO2降低环境污染,同时还能制得氢气,具体流程如下:
下列说法正确的是( )
A、分离器中的物质分离操作为过滤 B、膜反应器中,增大压强有利于提高HI的分解速率和平衡转化率 C、该工艺中I2和HI的相互转化体现了“碘循环” D、碘循环工艺的总反应为2SO2+4H2O+I2 = H2+2H2SO4+ 2HI13. 一定温度下,向10 mL 0.40 mol·L-1 H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示。( )t / min
0
2
4
6
V(O2) / mL
0
9.9
17.2
22.4
资料显示,反应分两步进行:
①2Fe3++ H2O2 2Fe2++O2↑+2H+
② H2O2 + 2Fe2++2H+ 2H2O+2Fe3+
反应过程中能量变化如右图所示。下列说法不正确的是
 A、0~6 min的平均反应速率:v(H2O2) = 3.33×10-2 mol·L-1·min-1 B、Fe3+的作用是加快过氧化氢的分解速率 C、反应①是吸热反应、反应②是放热反应 D、反应2H2O2(aq) 2H2O(l) + O2(g)的△H =E1-E2 < 014. 羰基硫(COS)可用于合成除草剂、杀草丹等农药。H2S与CO2在高温下反应可制得COS: H2S(g)+CO2(g) COS(g) +H2O(g) △H > 0。在 2 L 容器中充入一定量的H2S和CO2发生上述反应,数据如下:
A、0~6 min的平均反应速率:v(H2O2) = 3.33×10-2 mol·L-1·min-1 B、Fe3+的作用是加快过氧化氢的分解速率 C、反应①是吸热反应、反应②是放热反应 D、反应2H2O2(aq) 2H2O(l) + O2(g)的△H =E1-E2 < 014. 羰基硫(COS)可用于合成除草剂、杀草丹等农药。H2S与CO2在高温下反应可制得COS: H2S(g)+CO2(g) COS(g) +H2O(g) △H > 0。在 2 L 容器中充入一定量的H2S和CO2发生上述反应,数据如下: 下列判断不正确的是( )A、K1= B、K2=K3 且n3=2n2 C、初始反应速率:实验3 >实验2 >实验1 D、实验2中平衡时的c(COS)约为0.0286 mol·L-115. 硫酸铜是一种重要的化工产品。某工厂用刻蚀印刷电路板产生的碱性废液[含较多[Cu(NH3)4]2+及少量Cu2+、NH4+、NH3和Cl-]制备硫酸铜晶体,流程如下:
下列判断不正确的是( )A、K1= B、K2=K3 且n3=2n2 C、初始反应速率:实验3 >实验2 >实验1 D、实验2中平衡时的c(COS)约为0.0286 mol·L-115. 硫酸铜是一种重要的化工产品。某工厂用刻蚀印刷电路板产生的碱性废液[含较多[Cu(NH3)4]2+及少量Cu2+、NH4+、NH3和Cl-]制备硫酸铜晶体,流程如下: (1)、通过“中和、沉淀和过滤”可得碱式氯化铜[Cu(OH)Cl]固体,请将生成该固体的反应的离子方程式补充完整:[Cu(NH3)4]2+ +。(2)、制备Cu(OH)Cl沉淀时,溶液的pH对铜元素含量的影响如下图所示:
(1)、通过“中和、沉淀和过滤”可得碱式氯化铜[Cu(OH)Cl]固体,请将生成该固体的反应的离子方程式补充完整:[Cu(NH3)4]2+ +。(2)、制备Cu(OH)Cl沉淀时,溶液的pH对铜元素含量的影响如下图所示:
①若要提高Cu(OH)Cl沉淀的量,应将溶液的pH控制在(填字母序号)。
A. <5.2 B. 5.2~5.8 C. >5.8
②pH< 5.2 时,随pH减小,溶液中铜元素含量增大,其原因用反应的离子方程式可表示为。
(3)、“化浆、酸化"过程可得到硫酸铜粗品,发生的反应为Cu(OH)Cl+ 4H2O+ H2SO4= CuSO4·5H2O+ HCl。则硫酸铜粗品中,含铜元素的杂质为 , 检验样品中含有该杂质的方法是:取少量硫酸铜粗品,加入适量水使其充分溶解,。(4)、硫酸铜粗品还需要通过重结晶法进行提纯,具体操作是:将粗晶体溶解于热水中形成饱和溶液,然后加入适量乙醇,搅拌,冷却,过滤并洗涤,得到高纯度的硫酸铜晶体。加入乙醇能够提高硫酸铜的产率,从溶解性角度解释其可能的原因是。二、填空题
-
16. A、D、E、W是中学常见的四种元素,原子序数依次增大。A的原子最外层电子数是次外层的2倍,D的氧化物属于两性氧化物,D、E位于同周期,A、D、E的原子最外层电子数之和为14,W是人体必需的微量元素,缺乏W会导致贫血症状。(1)、A在元素周期表中的位置是。(2)、下列事实能用元素周期律解释的是(填字母序号)。
a . D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b. E的气态氢化物的稳定性小于HF
c. WE3的溶液可用于刻蚀铜制的印刷电路板
(3)、E的单质可以从NaBr溶液中置换出Br2单质,从原子结构的角度解释其原因是。(4)、①工业上用电解法制备D的单质,反应的化学方程式为。②家用“管道通”的有效成分是烧碱和D的单质,使用时需加入一定量的水,此时发生反应的化学方程式为。
(5)、W的单质可用于处理酸性废水中的NO3- , 使其转换为NH4+ , 同时生成有磁性的W的氧化物X,再进行后续处理。① 上述反应的离子方程式为。
② D的单质与X在高温下反应的化学方程式为。
三、综合题
-
17. 氯气可用于制取漂白剂和自来水消毒。(1)、将氯气通入水中制得氯水,氯水可用于漂白,其中起漂白作用的物质是 (填写化学式)。(2)、“84”消毒液也可用于漂白,其工业制法是控制在常温条件下,将氯气通入NaOH溶液中,反应的离子方程式为。(3)、同学们探究“84”消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售“84”消毒液稀释100倍,测得稀释后溶液的pH=12;
步骤2:取稀释后溶液各20 mL分别加入3个洁净的小烧杯中;
步骤3:用硫酸将3个烧杯内溶液的pH分别调至10、7和4。(溶液体积变化忽略不计)
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
烧杯
溶液的pH
现象
a
10
10 min后,红纸基本不褪色;4h后红纸褪色
b
7
10 min后,红纸颜色变浅;4 h后红纸褪色
c
4
10 min后,红纸颜色变得更浅;4h后红纸褪色
已知,溶液中Cl2、HClO和ClO-物质的量分数(α) 随pH变化的关系如下图所示:

①由实验现象可获得以下结论:溶液的pH在4 ~10范围内,pH越大,红纸褪色。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是。
(4)、由于氯气会与自来水中的有机物发生反应,生成对人体有害的物质,人们尝试研究并使用新的自来水消毒剂,如ClO2气体就是一种新型高效含氯消毒剂。①一种制备ClO2的方法是将SO2通入硫酸酸化的NaClO3溶液中,反应的离子方程式为。
②另一种制备ClO2的方法是用NaClO3与盐酸反应,同时有Cl2生成,产物中Cl2体积约占1/3。则每生成0.5 mol ClO2 , 转移mole-。
18. 丙烯是重要的有机化工原料,主要用于生产聚丙烯、丙烯腈、环氧丙烷等。(1)、以丁烯和乙烯为原料制备丙烯的方法被称为“烯烃歧化法",主要反应为C4H8(g)+C2H4(g) 2C3H6(g)
2C3H6(g)已知相关燃烧热数据:
C2H4(g)+3O2(g)=2CO2(g)+2H2O(l) △H1=-1411kJ·mol-1
C3H6(g)+ O2(g)=3CO2(g)+3H2O(l) △H2=-2049kJ·mol-1
C4H8(g)+6O2(g)=4CO2(g)+4H2O(l) △H3=-2539kJ·mol-1
①乙烯的电子式为。
②相同质量的C2H4(g)、C3H6(g)和C4H8(g)充分燃烧,放出的热量由多到少的顺序依次为(填写化学式)。
③ 上述“烯烃歧化法”的反应的热化学方程式为。
(2)、“丁烯裂解法”是另一种重要的丙烯生产法,生产过程中会有生成乙烯的副反应发生。反应如下:主反应:3C4H8 4C3H6;副反应:C4H8 2C2H4
测得上述两反应的平衡体系中,各组分的质量分数(w%)随温度(T)和压强(p)变化的趋势分别如图1和图2所示:

①平衡体系中的丙烯和乙烯的质量比[ ]是工业生产丙烯时选择反应条件的重要指标之一,从产物的纯度考虑,该数值越高越好,从图1和图2中表现的趋势来看,下列反应条件最适宜的是(填字母序号)
A. 300℃ 0.1MPa B. 700℃ 0.1MPa
C.300℃ 0.5MPa D.700℃ 0.5MPa
②有研究者结合图1数据并综合考虑各种因素,认为450℃的反应温度比300℃或700℃更合适,从反应原理角度分析其理由可能是。
③图2中,随压强增大,平衡体系中丙烯的质量分数呈上升趋势,从平衡角度解释其原因是。
四、实验题
-
19. 某同学在做浓硫酸与铜反应的实验过程中,观察到铜片表面变黑,于是对黑色物质的组成进行实验探究。(1)、用如右图所示装置进行实验1。(加热和夹持仪器已略去)

实验1:铜片与浓硫酸反应
操作
现象
加热到120℃~250℃
铜片表面变黑,有大量气体产生,形成墨绿色浊液
继续加热至338℃
铜片上黑色消失,瓶中出现“白雾”,溶液略带蓝色,瓶底部有较多灰白色沉淀
①装置B的作用是;装置C中盛放的试剂是。
②为证明A装置中灰白色沉淀的主要成分为硫酸铜,实验操作及现象是。
(2)、探究实验1中120℃~250℃时所得黑色固体的成分。【提出猜想】黑色固体中可能含有CuO、CuS、Cu2S中的一种或几种。
【查阅资料】
资料1:亚铁氰化钾[K4Fe(CN)6]是Cu2+的灵敏检测剂,向含有Cu2+的溶液中滴加亚铁氰化钾溶液,生成红棕色沉淀。
资料2:
CuS
Cu2S
黑色结晶或粉末
灰黑色结晶或粉末
难溶于稀硫酸;可溶于硝酸;微溶于浓氨水或热的浓盐酸
难溶于稀硫酸和浓盐酸;可溶于硝酸;微溶于浓氨水
【设计并实施实验】
实验2.探究黑色固体中是否含CuO
操作
现象
i.取表面附着黑色固体的铜片5片,用清水洗干净,放入盛有10mL试剂A的小烧杯中,搅拌
黑色表层脱落,露出光亮的铜片
ii.取出铜片,待黑色沉淀沉降
上层溶液澄清、无色
①试剂A是。
②甲认为ii中溶液无色有可能是Cu2+浓度太小,于是补充实验确认了溶液中不含Cu2+ , 补充的实验操作及现象是。
实验3.探究黑色固体中是否含CuS、Cu2S
操作
现象
i.取实验2中黑色固体少许,加入适量浓氨水,振荡后静置
有固体剩余,固液分界线附近的溶液呈浅蓝色
ii.另取实验2中黑色固体少许,加入适量浓盐酸,微热后静置
有固体剩余,溶液变成浅绿色
【获得结论】由实验2和实验3可得到的结论是:实验1中,120℃~250℃时所得黑色固体中。
【实验反思】
分析实验1中338℃时产生现象的原因,同学们认为是较低温度时产生的黑色固体与热的浓硫酸进一步反应造成。已知反应的含硫产物除无水硫酸铜外还有二氧化硫,则黑色固体消失时可能发生的所有反应的化学方程式为。
-