江西省高安市2017-2018学年九年级上学期化学期中考试试卷
试卷更新日期:2017-12-22 类型:期中考试
一、单选题
-
1. 下列变化属于化学变化的是( )A、死灰复燃 B、杯弓蛇影 C、冰消雪融 D、铁柞磨针2. 下列实验操作中,正确的是( )A、
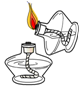 点燃酒精灯
B、
点燃酒精灯
B、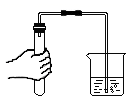 检查装置气密性
C、
检查装置气密性
C、 倾倒液体
D、
倾倒液体
D、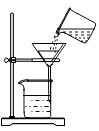 过滤
3. 下列关于氧气的说法正确的是( )A、空气中氧气含量最多 B、物质跟氧气反应都会发光发热 C、标准状况下氧气的密度比空气的密度小 D、鱼能在水中生存,说明水中溶解有氧气4. Cr2O3可以作为某些反应的催化剂,其中Cr元素的化合价是( )A、-3 B、+2 C、+3 D、+65. 下列关于化学方程式H2SO3+2H2=S↓+3H2O的理解,错误的是( )A、生成物有沉淀 B、反应物是H2SO3和H2 , 生成物是S和H2O C、该反应中,反应前后原子的种类和数目都不变 D、每1份质量的H2SO3和2份质量的H2完全反应,生成1份质量的S和3份质量的H2O6. 现有反应:2Cu(NO3)2 2CuO+O2↑+4X↑,则X 的化学式为( )A、NO B、NO2 C、NH3 D、N2O37. 下列粒子不直接构成物质的是( )A、原子 B、分子 C、电子 D、离子8. a克木炭在b克氧气中燃烧,生成二氧化碳的质量( )A、大于(a+b)克 B、小于(a+b)克 C、等于(a+b)克 D、小于或等于(a+b)克9. 在管道煤气中常添加微量具有刺激性气味的乙硫醇(化学式为C2H6S),目的是及时发现煤气泄漏。下列有关乙硫醇的说法不正确的是( )A、乙硫醇是由碳、氢、硫三种元素组成 B、乙硫醇中C,H,S三种元素的质量比为12:3:16 C、乙硫醇中碳元素的质量分数最大 D、1个乙硫醇分子中含有2个碳原子、6个氢原子、1个硫原子10. 已知固体氯酸钾在加热条件下可以分解,生成氧气.如果用二氧化锰作催化剂则可以加快其分解速度.已知a为固体氯酸钾,b为混有少量二氧化锰的固体氯酸钾,且a和b的质量相等,当分别同时加热a和b至完全反应时,能正确表示生成氧气的质量随反应时间而变化的图象是( )A、
过滤
3. 下列关于氧气的说法正确的是( )A、空气中氧气含量最多 B、物质跟氧气反应都会发光发热 C、标准状况下氧气的密度比空气的密度小 D、鱼能在水中生存,说明水中溶解有氧气4. Cr2O3可以作为某些反应的催化剂,其中Cr元素的化合价是( )A、-3 B、+2 C、+3 D、+65. 下列关于化学方程式H2SO3+2H2=S↓+3H2O的理解,错误的是( )A、生成物有沉淀 B、反应物是H2SO3和H2 , 生成物是S和H2O C、该反应中,反应前后原子的种类和数目都不变 D、每1份质量的H2SO3和2份质量的H2完全反应,生成1份质量的S和3份质量的H2O6. 现有反应:2Cu(NO3)2 2CuO+O2↑+4X↑,则X 的化学式为( )A、NO B、NO2 C、NH3 D、N2O37. 下列粒子不直接构成物质的是( )A、原子 B、分子 C、电子 D、离子8. a克木炭在b克氧气中燃烧,生成二氧化碳的质量( )A、大于(a+b)克 B、小于(a+b)克 C、等于(a+b)克 D、小于或等于(a+b)克9. 在管道煤气中常添加微量具有刺激性气味的乙硫醇(化学式为C2H6S),目的是及时发现煤气泄漏。下列有关乙硫醇的说法不正确的是( )A、乙硫醇是由碳、氢、硫三种元素组成 B、乙硫醇中C,H,S三种元素的质量比为12:3:16 C、乙硫醇中碳元素的质量分数最大 D、1个乙硫醇分子中含有2个碳原子、6个氢原子、1个硫原子10. 已知固体氯酸钾在加热条件下可以分解,生成氧气.如果用二氧化锰作催化剂则可以加快其分解速度.已知a为固体氯酸钾,b为混有少量二氧化锰的固体氯酸钾,且a和b的质量相等,当分别同时加热a和b至完全反应时,能正确表示生成氧气的质量随反应时间而变化的图象是( )A、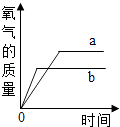 B、
B、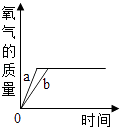 C、
C、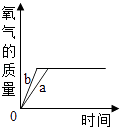 D、
D、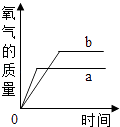
二、填空题
-
11. 如图所示,甲是某元素在周期表中的相关信息,乙是该元素原子的结构示意图。以下说法正确的是()

A.该元素属于金属元素
B.该元素的相对原子质量为35.45
C.该元素的原子在化学反应中易失去电子
D.该元素位于第周期
12. 下列实验现象描述正确的是()A.硫在空气中燃烧产生蓝紫色火焰 B.红磷燃烧产生大量白烟
C.木炭燃烧后生成黑色固体 D.
13. 雷阵雨过后,空气特别清新,原因之一是空气中少量氧气(O2 )转化为臭氧(O3),表示为:3O2 2O3 。下列说法中正确的是()A.等质量的 O2与O3所含原子数相等 B.O2 转化为O3属于物理变化
C.O2与O3的相对分子质量相等 D.
14. 活性炭可处理大气污染物NO。在一定条件下的密闭容器中,NO气体与活性炭中的C反应生成甲、乙两种气体,其中甲是空气中含量最多的气体。测得各物质的质量如下表所示:物质质量 /g
反应时间/min
活性炭
NO
甲
乙
0
28.72
5.00
0
0
4
28.00
1.40
x
2.64
下列说法正确的是()
A.生成甲、乙的分子数之比为1:1
B.反应消耗的C与NO的质量之比为2:5
C. x的值为26.76
D.
15. 以下是某化学反应的微观示意图。有关该反应的说法正确的是()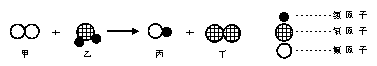
A.该反应中丙与丁的分子个数比为4:1 B.该反应属于化合反应
C.该反应前后原子的数目发生改变 D.
16. 用化学用语填空。
(1)、汞元素 ,(2)、2个氧分子 ,(3)、3个铵根离子17. 水是生命之源,也是人类最宝贵的资源。请回答下列有关问题: (1)、活性炭常用于净水,是利用其。(2)、建设新农村后,村民已经用上自来水,加入可检验自来水是否为硬水。(3)、实验室通常用右图装置来电解水,当B试管中产生的气体体积为10mL时, A试管中产生的气体体积为mL。(4)、下列做法有利于节水的是 (填字母序号)。A、农业上改漫灌为滴灌 B、用大量水冲洗汽车 C、用淘米水浇花 D、用洗衣服水冲厕所18. 我国自主研发的“硅衬底高光效氮化镓(GaN)发光二极管(简称LED)技术”已广泛应用于照明、显像等多个领域。请回答下列问题:(1)、有以下微粒的结构示意图:
(1)、活性炭常用于净水,是利用其。(2)、建设新农村后,村民已经用上自来水,加入可检验自来水是否为硬水。(3)、实验室通常用右图装置来电解水,当B试管中产生的气体体积为10mL时, A试管中产生的气体体积为mL。(4)、下列做法有利于节水的是 (填字母序号)。A、农业上改漫灌为滴灌 B、用大量水冲洗汽车 C、用淘米水浇花 D、用洗衣服水冲厕所18. 我国自主研发的“硅衬底高光效氮化镓(GaN)发光二极管(简称LED)技术”已广泛应用于照明、显像等多个领域。请回答下列问题:(1)、有以下微粒的结构示意图:
上述微粒中,属于阳离子的是 (填序号),化学性质相似的是 (填序号),D粒子的化学符号为。
(2)、镓(Ga)的原子结构示意图为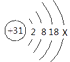 ,x=。磷化镓也是制造LED的一种材料,其化学式为。 19. 一种新型火箭推进剂在火箭发射过程中,发生反应的微观过程如下图所示。
,x=。磷化镓也是制造LED的一种材料,其化学式为。 19. 一种新型火箭推进剂在火箭发射过程中,发生反应的微观过程如下图所示。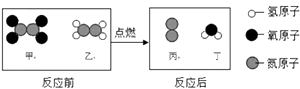 (1)、四种物质中属于氧化物的有(2)、丁中各元素的质量比为(3)、参加反应甲、乙质量比为
(1)、四种物质中属于氧化物的有(2)、丁中各元素的质量比为(3)、参加反应甲、乙质量比为
20. 甲、乙、丙三种物质均含地壳中含量最多的元素。甲、乙是组成元素相同的化合物,丙是单质;甲、乙在常温下均为液体,在一定条件下均可分解成丙;它们之间有如右图所示的转化关系(部分物质和反应条件已经略去)。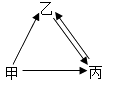 (1)、甲的化学式为;(2)、乙转化成丙的化学方程式为;(3)、甲转化成丙的反应基本类型为(4)、甲、乙、丙三种物质中属于单质的是。21. 下图是初中化学的几种常用仪器,根据要求回答问题:
(1)、甲的化学式为;(2)、乙转化成丙的化学方程式为;(3)、甲转化成丙的反应基本类型为(4)、甲、乙、丙三种物质中属于单质的是。21. 下图是初中化学的几种常用仪器,根据要求回答问题: (1)、写出仪器C的名称。(2)、实验室用过氧化氢溶液制取氧气,应选用的仪器是 (填字母序号),反应的化学方程式为;检验氧气已集满的方法是。(3)、小明为了用右图装置收集一定量的氧气,装置接口连接的顺序为 , 量筒的作用是。
(1)、写出仪器C的名称。(2)、实验室用过氧化氢溶液制取氧气,应选用的仪器是 (填字母序号),反应的化学方程式为;检验氧气已集满的方法是。(3)、小明为了用右图装置收集一定量的氧气,装置接口连接的顺序为 , 量筒的作用是。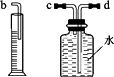 22. 某化学小组同学,用如图所示实验探究质量守恒定律.
22. 某化学小组同学,用如图所示实验探究质量守恒定律. (1)、充分反应冷却后,天平仍然平衡的是(填写字母序号),该反应的化学方程式为 .(2)、由上述实验可知,在化学反应前后,一定不变的(填数字序号).
(1)、充分反应冷却后,天平仍然平衡的是(填写字母序号),该反应的化学方程式为 .(2)、由上述实验可知,在化学反应前后,一定不变的(填数字序号).①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质总质量
(3)、红热的铁能与水蒸气反应,放出气体X,同时生成固体Y.X气体靠近火焰点火时,能燃烧或发出爆鸣声.其反应的化学方程式为:3Fe+4H2O 4X+Y.则X的化学式为 , Y的化学式为 .23. 在实验室加热32.5g二氧化锰和氯酸钾的固体混合物制取氧气时,剩余固体物质的质量变化如下图所示。请计算: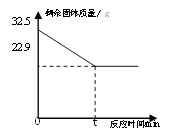 (1)、完全反应时,生成氧气的质量为。(2)、完全反应后,剩余固体物质属 (填纯净物、混合物)。(3)、原固体混合物中氯酸钾的质量为 (列式计算)。
(1)、完全反应时,生成氧气的质量为。(2)、完全反应后,剩余固体物质属 (填纯净物、混合物)。(3)、原固体混合物中氯酸钾的质量为 (列式计算)。三、实验探究题
-
24. 课本第二单元课后作业中有“寻找新的催化剂” 的探究内容,实验中学探究小组据此设计了如下探究方案。
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
(1)、【实验探究】实验步骤
实验现象
实验结论及解释
Ⅰ.
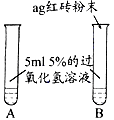
A中无明显现象, B中产生大量能使带火星木条复燃的气体
产生的气体是
② 红砖粉末能改变过氧化氢分解速率
Ⅱ. 向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣
① 又产生大量能使带火星木条复燃的气体
滤渣质量等于ag
红砖粉末的和在反应前后均没有发生变化,能作过氧化氢分解的催化剂
Ⅲ.
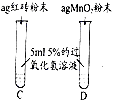
两试管中均产生气泡
且
红砖粉末的催化效果没有二氧化锰粉末好
(2)、【拓展应用】已知CuSO4也可作为过氧化氢分解的催化剂。向101.2g一定溶质质量分数的过氧化氢溶液中加入2g CuSO4粉末,充分反应后得到溶质质量分数为2%的溶液,则生成氧气 g。