江苏省无锡市和桥学区、张渚学区2017-2018学年九年级上学期化学期中考试试卷
试卷更新日期:2017-12-20 类型:期中考试
一、单选题
-
1. 绿色化学的核心是要利用化学原理从源头上减少和消除工业生产对环境的污染,下列措施属于“绿色化学”范畴的是( )A、杜绝污染源 B、治理污染点 C、深埋有毒物 D、处理废弃物2. 含氟牙膏能增强牙齿的坚固性.这里所说的氟指的是( )A、原子 B、分子 C、元素 D、单质3. 下列物质的用途是由其物理性质决定的是( )A、乙醇可作燃料 B、氧气用于急救病人 C、氢气填充气球 D、氮气做保护气4. 下列有关实验现象描述正确的是( )A、木炭点燃后生成黑色固体 B、蜡烛燃烧时生成水和二氧化碳 C、铁丝在纯氧中燃烧时发出白光 D、硫燃烧时产生无色、有刺激性气味的气体5. 下列基本操作正确的是( )A、
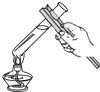 给液体加热
B、
给液体加热
B、 滴加液体
C、
滴加液体
C、 熄灭酒精灯
D、
熄灭酒精灯
D、 检查装置气密性
6. 下表是元素周期表的部分,其中碳元素部分信息缺失,有关该元素认识错误的是( )
检查装置气密性
6. 下表是元素周期表的部分,其中碳元素部分信息缺失,有关该元素认识错误的是( )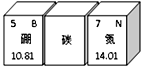 A、该元素对应原子的质子数为6 B、该元素属于金属元素 C、该元素的原子核外有6个电子 D、该元素化学性质与最外层电子数密切相关7. 下列说法正确的是( )A、过氧化氢和水的化学性质不同是因为组成元素不同 B、氧原子与碳原子属于不同种元素是因为最外层电子数不同 C、电解水实验证明水是由氢分子和氧分子构成的 D、纯净物的组成是固定不变的,所以表示每种物质组成的化学式只有一个8. 学习要善于归纳和总结。以下认识完全正确的是( )
A、该元素对应原子的质子数为6 B、该元素属于金属元素 C、该元素的原子核外有6个电子 D、该元素化学性质与最外层电子数密切相关7. 下列说法正确的是( )A、过氧化氢和水的化学性质不同是因为组成元素不同 B、氧原子与碳原子属于不同种元素是因为最外层电子数不同 C、电解水实验证明水是由氢分子和氧分子构成的 D、纯净物的组成是固定不变的,所以表示每种物质组成的化学式只有一个8. 学习要善于归纳和总结。以下认识完全正确的是( )A.对微粒的认识
B.对环境保护的认识
①分子可分,原子不可分
②质子数相同的粒子一定属于同种元素
①二氧化碳排放过多不会影响环境
②生活污水排放对水质影响比较大
C.对物质鉴别的认识
D.对化学史的认识
①用品尝的方法鉴别实验室的氯化钠和蔗糖
②用燃着的木条鉴别氮气和氧气
①门捷列夫发现了元素周期律
②张青莲主持测定了多个相对原子质量
A、A B、B C、C D、D9. 下列关于水的说法中正确的是( )A、我国水资源非常丰富,所以我国不是缺水国家 B、水的净化操作里,过滤所用的玻璃棒是起搅拌作用的 C、电解水时向水中加入少量氢氧化钠的目的是增强水的导电性 D、经过活性炭吸附后的水无色无味,是纯净物10. 花青素(C15H11O6)广泛存在于深红色、紫色或蓝色的蔬菜水果中,能够保护人体免受某些有害物质的损伤。关于花青素的说法正确的是( )A、花青素中氢元素和氧元素的质量比为11:96 B、花青素分子由碳元素、氢元素和氧元素构成 C、花青素中氧元素质量分数最高 D、花青素中有15个碳原子、11个氢原子和6个氧原子11. 某化学反应的微观示意图如下。下列说法错误的是( ) A、该反应共涉及三种元素 B、反应前后原子的种类发生了改变 C、生成物都是氧化物 D、反应前后分子的种类发生了改变12. 下列实验操作先后顺序错误的是( )A、点燃氢气前,先检验纯度后点燃,以免爆炸 B、高锰酸钾制取氧气结束时,先熄灭酒精灯,后将导气管移出水槽 C、排水法收集氧气时,待气泡连续均匀冒出后,再进行收集 D、检查装置的气密性时,先将导管插入水中,后用双手紧握试管外壁13. 某同学归纳了以下知识点①所有原子的原子核都是由质子和中子构成;②湖水中
A、该反应共涉及三种元素 B、反应前后原子的种类发生了改变 C、生成物都是氧化物 D、反应前后分子的种类发生了改变12. 下列实验操作先后顺序错误的是( )A、点燃氢气前,先检验纯度后点燃,以免爆炸 B、高锰酸钾制取氧气结束时,先熄灭酒精灯,后将导气管移出水槽 C、排水法收集氧气时,待气泡连续均匀冒出后,再进行收集 D、检查装置的气密性时,先将导管插入水中,后用双手紧握试管外壁13. 某同学归纳了以下知识点①所有原子的原子核都是由质子和中子构成;②湖水中
含有氧分子;③催化剂只能加快化学反应的速率;④同种元素组成的物质叫做单质;⑤
氧化反应不一定是化合反应;⑥最外层电子数为8的粒子不一定是稀有气体元素的原子。
以上说法中正确的是( )A、①②④ B、③④⑤ C、①③⑥ D、②⑤⑥14.如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若整个大圆圈代表纯净物,则在下列选项中,能正确指出①、②、③、④所属物质类别的是( )
 A、②化合物、④氧化物 B、①单质、③氧化物 C、①单质、③化合物 D、②含氧化合物、④氧化物
A、②化合物、④氧化物 B、①单质、③氧化物 C、①单质、③化合物 D、②含氧化合物、④氧化物二、填空题
-
15. 二氧化硅可用于制造分离膜,利用“膜分离”技术二氧化碳可被浓氨水吸收(如下图)转化为可做氮肥的碳酸氢铵(NH4HCO3)。
 (1)、浓氨水属于 (填“纯净物”或“混合物”)。(2)、NH4HCO3由种元素组成,其中碳元素和氢元素的质量比为。(3)、二氧化硅的化学式为。(4)、保持二氧化碳化学性质的最小粒子是 (填具体粒子名称),标出二氧化碳中碳元素的化合价。(5)、氧离子的结构示意图为
(1)、浓氨水属于 (填“纯净物”或“混合物”)。(2)、NH4HCO3由种元素组成,其中碳元素和氢元素的质量比为。(3)、二氧化硅的化学式为。(4)、保持二氧化碳化学性质的最小粒子是 (填具体粒子名称),标出二氧化碳中碳元素的化合价。(5)、氧离子的结构示意图为 ,则X= , 氧离子的离子符号是。 16. 根据下列实验装置图,回答有关问题。
,则X= , 氧离子的离子符号是。 16. 根据下列实验装置图,回答有关问题。 (1)、写出图中标号仪器的名称:a。(2)、实验室用氯酸钾制取氧气,其反应的符号表达式为 , 可选用的收集装置为 (从装置A~E中选择字母填写,下题同),若改用高锰酸钾来制取氧气,需要对装置进行的改进是。(3)、实验室里可用氢氧化钙与氯化铵的固体混合物加热制取氨气,则制取氨气所需的发生装置为 , 氨气极易溶于水、密度小于空气,一般可用装置收集氨气。(4)、利用F装置收集氧气,验满时应将带火星木条放在 (填“①”或“②”)处。(5)、在2017年江苏省中学化学创新实验调演中,李彬老师设计了“氢氧焰”的实验装置如下:
(1)、写出图中标号仪器的名称:a。(2)、实验室用氯酸钾制取氧气,其反应的符号表达式为 , 可选用的收集装置为 (从装置A~E中选择字母填写,下题同),若改用高锰酸钾来制取氧气,需要对装置进行的改进是。(3)、实验室里可用氢氧化钙与氯化铵的固体混合物加热制取氨气,则制取氨气所需的发生装置为 , 氨气极易溶于水、密度小于空气,一般可用装置收集氨气。(4)、利用F装置收集氧气,验满时应将带火星木条放在 (填“①”或“②”)处。(5)、在2017年江苏省中学化学创新实验调演中,李彬老师设计了“氢氧焰”的实验装置如下:
利用氢气与氧气的发生装置制取并储存纯净的气体于气球中。A瓶中硫酸铜溶液的作用是。通过玻璃活塞K1、K2分别有序控制氧气和氢气的流量,先后进行如下操作:
①闭K2 , 打开K1 , 通入氧气,将带火星的木条置于三通管口处,观察到 , 说明氧气具有助燃性。将术条移开,管口处无火焰。
②关闭K1 , 打开K2 , 通入氢气,将燃着的木条置于三通管口处,管口处有火焰。移去燃着的木条,氢气安静地燃烧,说明氢气具有可燃性,该反应的符号表达式为 。把铁片放在火焰上一段时间,铁片呈红热状。打开K1 , 通入氧气,铁片迅速熔断被切割,由此得出的结论是。
17. 如图是以空气中的氮气为原料制取氮肥(NH4NO3)的工业流程。 (1)、步骤①中发生的是变化(填“物理”或“化学”)。(2)、拉瓦锡是最早用定量的方法测定空气成分的化学家,他通过实验得出的结论是空气中氮气和氧气的体积比为。(3)、步骤③中发生的化学反应的符号表达式为。(4)、上述化学反应中属于化合反应的有个。
(1)、步骤①中发生的是变化(填“物理”或“化学”)。(2)、拉瓦锡是最早用定量的方法测定空气成分的化学家,他通过实验得出的结论是空气中氮气和氧气的体积比为。(3)、步骤③中发生的化学反应的符号表达式为。(4)、上述化学反应中属于化合反应的有个。三、实验探究题
-
18. 空气中氧气含量测定的再认识.
 (1)、【经典赏析】拉瓦锡用定量的方法研究空气的成分(实验装置如图1).
(1)、【经典赏析】拉瓦锡用定量的方法研究空气的成分(实验装置如图1).该实验中选择使用汞的优点有
A.实验过程中没有污染
B.能将密闭装置内空气中的氧气几乎耗尽
C.在汞槽中起到液封的作用
D.生成的化合物加热分解又能得到汞和氧气
(2)、【实验回顾】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如图2),写出红磷燃烧的符号表达式。图2中集气瓶底部的水的作用为。(填字母)A.吸收有害物质 B.降温,快速冷却 C.保护瓶底
但是用该方法测出的氧气含量常常低于21%。
(3)、【提出问题】用该方法测出的氧气含量为什么低于21%?【进行猜想】①;② , 装置内氧气有剩余;
(4)、【实验与交流】为了帮助同学们更好地理解空气中氧气含量测定的实验原理,老师利用传感器技术定时测定了实验装置(如图5)内的压强、温度和氧气浓度,三条曲线变化趋势如图6所示。其中X曲线表示的是 (填“温度”或“氧气的浓度”);【反思拓展】结合X、Y两条曲线,解释如图6中BC段气压变化的原因是;
(5)、【实验探究1】已知,铁丝在纯氧中才能燃烧,反应的符号表达式为 , 一般不能在空气中燃烧,因此无法用铁丝代替红磷进行该实验。小明根据铁生锈的原理(铁在常温下可以和氧气、水生成铁锈)来测定空气中氧气的含量,于是进行了实验(装置如图3)。通过7天测得的数据计算出空气中氧气的含量为19.13%。【交流与反思】与用红磷燃烧的方法相比,用铁丝生锈的方法的主要优点 (填字母)。
A.装置内残留的氧气更少
B.反应更彻底,实验结果更准确
C.铁丝生锈比红磷燃烧反应更快
(6)、【实验探究2】小明利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4)。8分钟后测得的数据如下表:请计算出空气中氧气含量 (计算结果保留一位小数)。相对于实验探究1,实验探究2改进的目的是。实验前的体积
实验后的体积
集气瓶内空气
烧杯内蒸馏水
烧杯内剩余蒸馏水
131mL
90.0mL
63.6mL
(7)、【拓展延伸】铜能与空气中氧气、水、二氧化碳反应生成铜绿[其主要成分为:Cu2(OH)2CO3]。若将图3中的铁丝换成足量的铜丝,能否比较准确地测定空气中氧气的含量 , 理由 (填字母)
A.空气中CO2含量只有约0.03%,铜不能将装置内的氧气几乎耗尽
B.铜丝反应比铁丝快
C.反应更彻底