人教版(五四学制)化学九年级上册单元测试-第三单元 酸和碱(基础卷)
试卷更新日期:2025-08-30 类型:单元试卷
一、选择题
-
1. 碱溶液中都含有OH- , 因此不同的碱表现出一些共同的性质.下列关于Ba(OH)2 性质的描述中不属于碱的共同性质的是( ).A、能使紫色石蕊溶液变蓝色 B、能与盐酸反应生成H2O C、能与 Na2SO4溶液反应生成BaSO4沉淀 D、能与CO2反应生成H2O2. 要使如图所示装置中的小气球鼓起来,则使用的固体和液体可以是( ).

①硝酸铵和水;②铁和稀硫酸;③固体氢氧化钠和水;④生石灰和水;⑤石灰石和稀盐酸.
A、①②③④⑤ B、②③④⑤ C、②③⑤ D、②④⑤3. 下列劳动实践与化学知识没有直接关联的是选项
劳动实践
化学知识
A
用食醋去除热水壶中的水垢
食醋的pH<7
B
铁锅用完后洗净擦干
防止铁与氧气、水接触而生锈
C
用小苏打片治疗胃酸过多
利用中和反应的原理
D
用厨余垃圾自制花肥
物质发生缓慢氧化
A、A B、B C、C D、D4. 小红学习酸碱指示剂与常见酸、碱溶液作用后,归纳总结出如图所示的关系.图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,其中颜色不正确的是( ). A、紫色 B、蓝色 C、红色 D、无色5. 下列实验操作正确的是A、测量溶液的pH
A、紫色 B、蓝色 C、红色 D、无色5. 下列实验操作正确的是A、测量溶液的pH B、检查气密性
B、检查气密性 C、稀释浓硫酸
C、稀释浓硫酸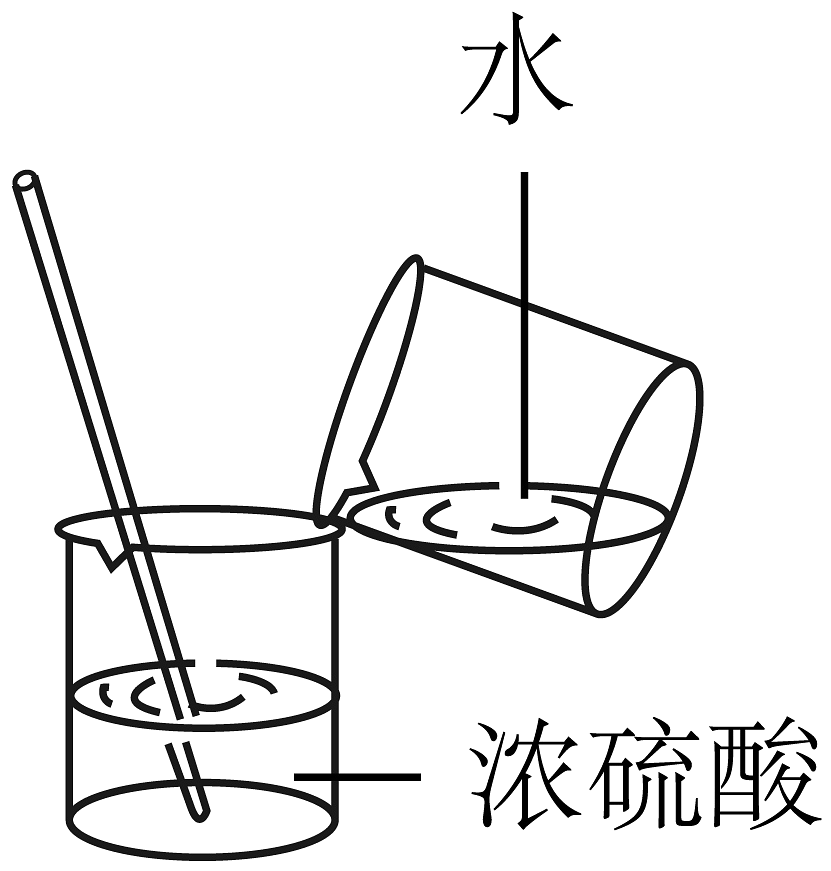 D、称量氢氧化钠
D、称量氢氧化钠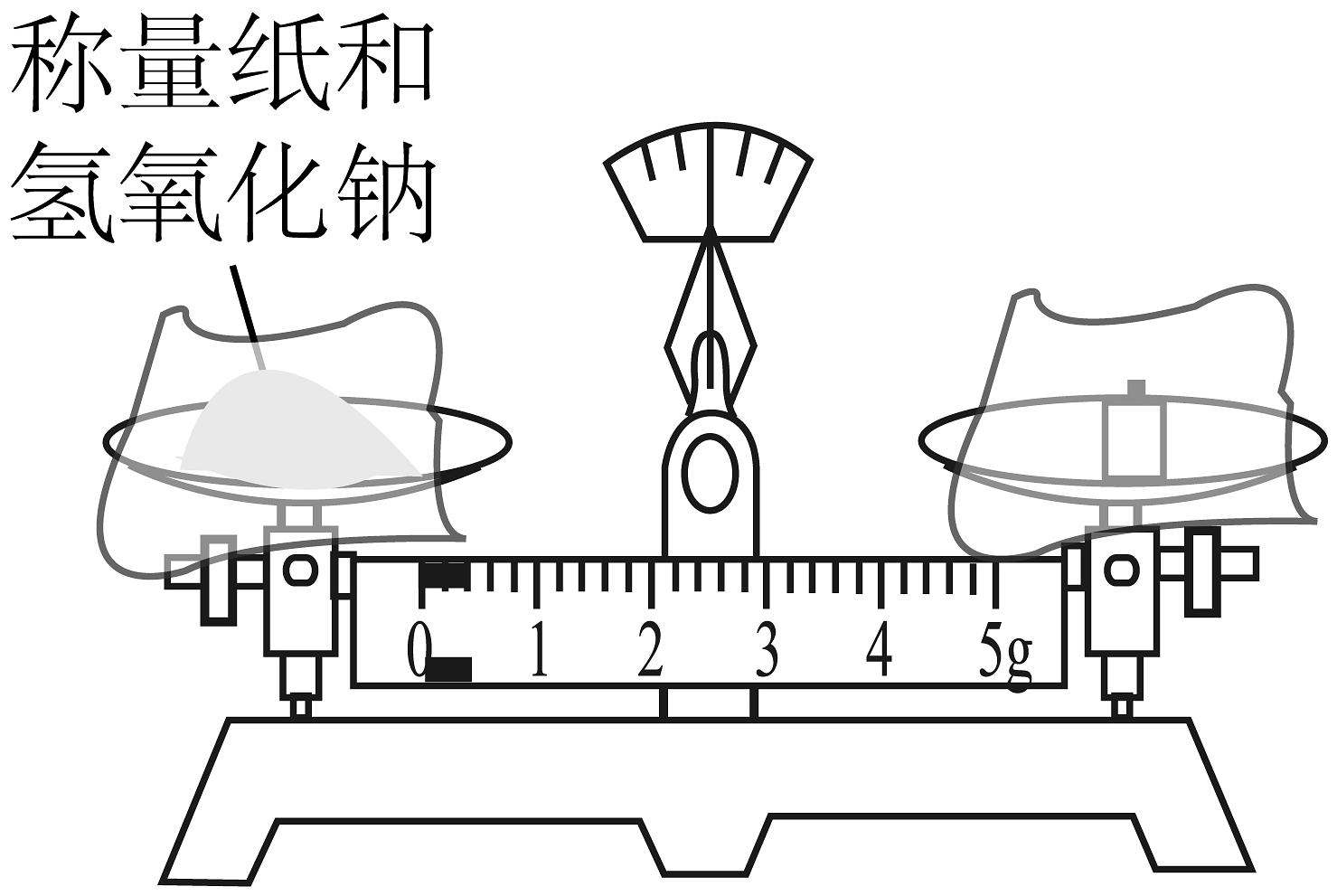 6. 生活中一些常见物质和近似pH如下,胃酸过多的人空腹最适宜喝的食物是( )A、柠檬汁pH(2~3) B、酸奶pH(5~6) C、玉米粥pH(7~8) D、可乐pH(2~4)7. 土壤酸碱性是土壤重要的化学性质,影响植物对营养物质的吸收。土壤的pH对部分营养元素吸收的影响如图1(条带越宽,吸收率越高)所示。农作物秸秆制成的有机物料具有一定修复酸性土壤的能力。科研人员研究添加等量(添加量为10g/kg)不同植物物料后,利用数字化实验仪器,对土壤pH进行测定,得到如图2所示的土壤pH与时间的关系图。下列说法错误的是
6. 生活中一些常见物质和近似pH如下,胃酸过多的人空腹最适宜喝的食物是( )A、柠檬汁pH(2~3) B、酸奶pH(5~6) C、玉米粥pH(7~8) D、可乐pH(2~4)7. 土壤酸碱性是土壤重要的化学性质,影响植物对营养物质的吸收。土壤的pH对部分营养元素吸收的影响如图1(条带越宽,吸收率越高)所示。农作物秸秆制成的有机物料具有一定修复酸性土壤的能力。科研人员研究添加等量(添加量为10g/kg)不同植物物料后,利用数字化实验仪器,对土壤pH进行测定,得到如图2所示的土壤pH与时间的关系图。下列说法错误的是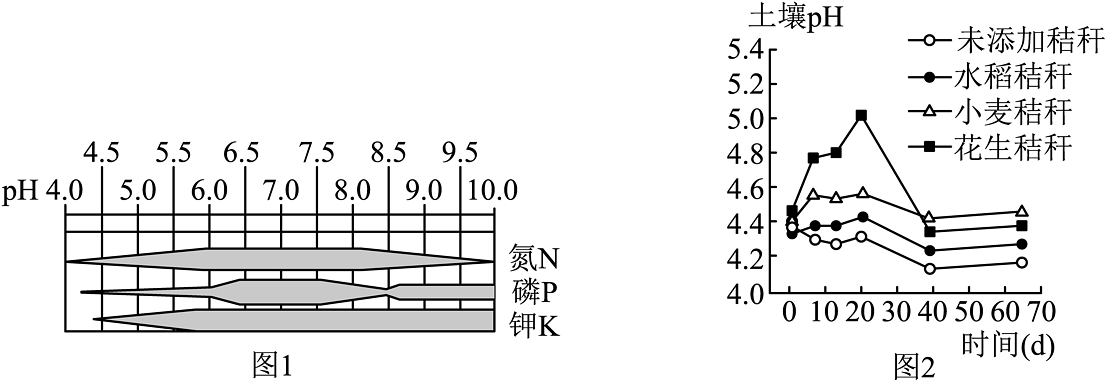 A、由图1可知,为提高营养元素吸收率,应将土壤pH控制在6.5~7.5 B、由图2可知,小麦秸秆比水稻秸秆对酸性土壤的改良效果更好 C、由图2可知,添加花生秸秆制作的物料后,土壤pH随天数增加而升高 D、某地土壤酸化是因为其中含有少量硫酸,通过喷洒熟石灰粉末的方法改良该土壤发生反应的化学方程式为H2SO4+Ca(OH)2=CaSO4+2H2O8. 实验小组用pH传感器研究溶液与稀硫酸的反应,实验装置及测定结果如下图已知: , 难溶于水。
A、由图1可知,为提高营养元素吸收率,应将土壤pH控制在6.5~7.5 B、由图2可知,小麦秸秆比水稻秸秆对酸性土壤的改良效果更好 C、由图2可知,添加花生秸秆制作的物料后,土壤pH随天数增加而升高 D、某地土壤酸化是因为其中含有少量硫酸,通过喷洒熟石灰粉末的方法改良该土壤发生反应的化学方程式为H2SO4+Ca(OH)2=CaSO4+2H2O8. 实验小组用pH传感器研究溶液与稀硫酸的反应,实验装置及测定结果如下图已知: , 难溶于水。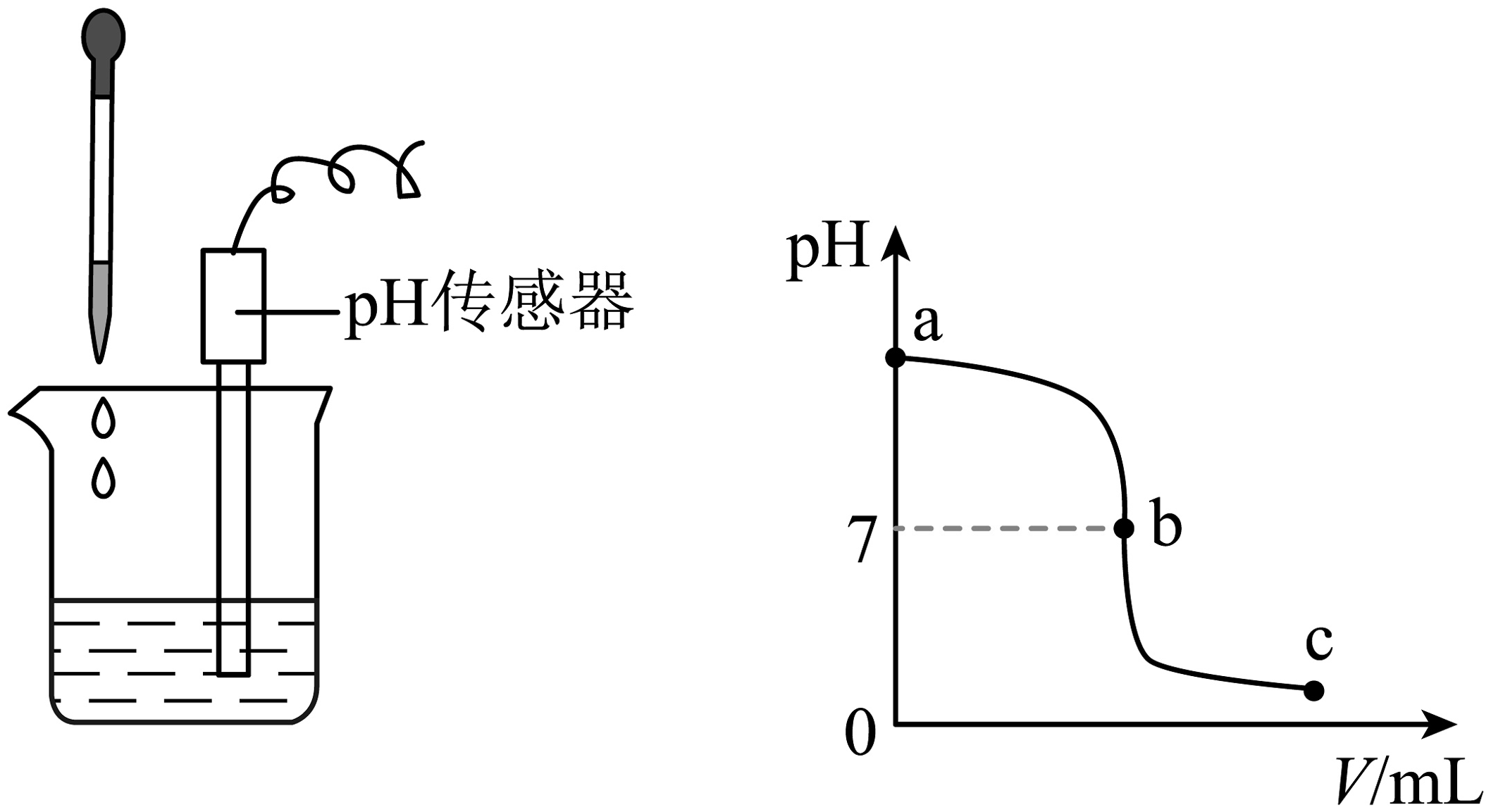
下列说法不正确的是
A、实验中可观察到溶液变浑浊 B、a处 , 说明烧杯中事先盛放的是溶液 C、b处 , 说明二者恰好完全反应 D、c处溶液能使酚酞溶液变红9. 健康人的体液必须维持在一定的酸碱度范围内,如果出现异常,则可能导致疾病。下表是人体内的一些体液和排泄物的正常范围:物质
血浆
胃液
胆汁
尿液
7.35~7.45
0.9~1.5
7.1~7.3
4.7~8.4
下列有关说法正确的是
A、当胆汁或时,人体可能导致疾病 B、胃液一定显酸性,尿液一定显碱性 C、可使用试纸测定血浆的是否在正常范围内 D、胆汁、血浆都呈碱性且胆汁的碱性比血浆强10. 小深用碳酸钠、水和紫罗兰花(变色规律与紫色石蕊溶液类似)进行了如图 1 所示的实验,并连续观察几天。碳酸钠的溶解度曲线如图 2 所示,下列说法错误的是( ) A、Ⅰ中 21.8g 碳酸钠能全部溶解 B、碳酸钠的溶解度随着温度的上升不断增大 C、Ⅲ中有碳酸钠晶体析出 D、紫罗兰花放在Ⅲ中,一段时间后变为蓝色11. 某兴趣小组同学将pH传感器分别插入三只盛有相同体积蒸馏水的烧杯中,打开磁力搅拌器,同时采集数据,再向三只烧杯中同时分别加入适量的柠檬酸、氯化钠、氢氧化钠三种固体。实验数据如图所示,下列说法不正确的是
A、Ⅰ中 21.8g 碳酸钠能全部溶解 B、碳酸钠的溶解度随着温度的上升不断增大 C、Ⅲ中有碳酸钠晶体析出 D、紫罗兰花放在Ⅲ中,一段时间后变为蓝色11. 某兴趣小组同学将pH传感器分别插入三只盛有相同体积蒸馏水的烧杯中,打开磁力搅拌器,同时采集数据,再向三只烧杯中同时分别加入适量的柠檬酸、氯化钠、氢氧化钠三种固体。实验数据如图所示,下列说法不正确的是 A、①表示氢氧化钠溶于水,说明OH-浓度越大pH越大 B、②表示氯化钠溶于水,pH=7说明溶液中无自由移动离子 C、③表示柠檬酸溶于水,说明H+浓度越大pH越小 D、柠檬酸溶液和氢氧化钠能发生中和反应12. 充分燃烧1kg天然气和煤所产生CO2和SO2的质量如下图所示.下列说法不正确的是( ).
A、①表示氢氧化钠溶于水,说明OH-浓度越大pH越大 B、②表示氯化钠溶于水,pH=7说明溶液中无自由移动离子 C、③表示柠檬酸溶于水,说明H+浓度越大pH越小 D、柠檬酸溶液和氢氧化钠能发生中和反应12. 充分燃烧1kg天然气和煤所产生CO2和SO2的质量如下图所示.下列说法不正确的是( ). A、等质量的煤和天然气充分燃烧,产生CO2的量接近,但产生SO2的量却相差较大 B、煤、天然气充分燃烧产生的CO2和SO2是导致酸雨的主要气体 C、煤、天然气及石油等是重要的化石燃料,属于不可再生能源 D、由图示可知,提倡将煤改为天然气作燃料,有利于改善空气质量13. 已知:( 2H2O.为探究铜和浓硫酸的反应及生成的二氧化硫气体的部分性质,某同学设计如图所示实验(图中脱脂棉团蘸有紫色石蕊溶液).关于该实验的说法错误的是( ).
A、等质量的煤和天然气充分燃烧,产生CO2的量接近,但产生SO2的量却相差较大 B、煤、天然气充分燃烧产生的CO2和SO2是导致酸雨的主要气体 C、煤、天然气及石油等是重要的化石燃料,属于不可再生能源 D、由图示可知,提倡将煤改为天然气作燃料,有利于改善空气质量13. 已知:( 2H2O.为探究铜和浓硫酸的反应及生成的二氧化硫气体的部分性质,某同学设计如图所示实验(图中脱脂棉团蘸有紫色石蕊溶液).关于该实验的说法错误的是( ). A、与鼓气球相连接的导管需插入浓硫酸中 B、该装置便于控制铜和浓硫酸反应的发生和停止 C、铜丝绕成螺旋状是为了加快铜和浓硫酸的反应 D、实验中可观察到脱脂棉团变红14. 利用数字化手持技术探究金属铝和稀盐酸反应,其容器内的压强和温度随时间变化的关系如下图所示,下列说法不正确的是( )
A、与鼓气球相连接的导管需插入浓硫酸中 B、该装置便于控制铜和浓硫酸反应的发生和停止 C、铜丝绕成螺旋状是为了加快铜和浓硫酸的反应 D、实验中可观察到脱脂棉团变红14. 利用数字化手持技术探究金属铝和稀盐酸反应,其容器内的压强和温度随时间变化的关系如下图所示,下列说法不正确的是( ) A、0~50s 内 AB 段压强变化不明显,原因可能是铝表面的金属氧化物与酸发生反应 B、由温度变化曲线可知,该反应属于放热反应 C、BC 段压强上升只是因为反应生成气体 D、CD 段压强下降是因为反应结束,温度下降
A、0~50s 内 AB 段压强变化不明显,原因可能是铝表面的金属氧化物与酸发生反应 B、由温度变化曲线可知,该反应属于放热反应 C、BC 段压强上升只是因为反应生成气体 D、CD 段压强下降是因为反应结束,温度下降二、非选择题
-
15. 生活中处处有化学。比如农业上通常用(写化学式)改良酸性土壤;医疗上通常用小苏打治疗胃酸过多,请写出该反应的化学方程式:。16. 我国使用的燃料主要是煤炭和石油,含有硫的煤炭燃烧时排放出污染空气的有毒气体,主要是 SO2 , 它遇到雨水成为酸雨降落到地面会带来很大的危害.请回答下列问题.(1)、请举出三个方面的危害实例:①;②;③.(2)、许多植物有抗御污染空气的有毒气体的能力,在常见植物中对这些气体有较强吸附能力的是(填植物名称).(3)、当SO2污染较严重时,可用直升机喷洒碳酸钙粉末,脱硫效果可达85%,其化学方程式为: 实验证明石灰浆[Ca(OH)2]在空气中也可吸收SO2生成硫酸钙和其他物质,该反应的化学方程式为:.17. 根据碱的部分化学性质回答下列问题。
 (1)、补上图中碱类物质的第④点化学性质:。(2)、小明同学为了验证碱溶液与指示剂的作用,向石灰水中滴入几滴无色酚酞,发现溶液。我们常用澄清石灰水来检验二氧化碳气体,其反应原理是(用方程式表示)。18. 坚持“人与自然和谐共生”是新时代中国特色社会主义的基本方略之一,让“山更绿,水更清,空气更清新”是我们共同的追求.(1)、“山更绿”离不开绿色植物.
(1)、补上图中碱类物质的第④点化学性质:。(2)、小明同学为了验证碱溶液与指示剂的作用,向石灰水中滴入几滴无色酚酞,发现溶液。我们常用澄清石灰水来检验二氧化碳气体,其反应原理是(用方程式表示)。18. 坚持“人与自然和谐共生”是新时代中国特色社会主义的基本方略之一,让“山更绿,水更清,空气更清新”是我们共同的追求.(1)、“山更绿”离不开绿色植物.①植物的光合作用需要吸收空气中的水和 , 可有效减缓温室效应.
②酸雨不利于植物生长.煤燃烧产生的进入大气后可形成“硫酸型”酸雨.
(2)、“水更清”就得保护好水资源.①下列关于水的说法正确的是(填字母).
a.工业废水需经处理达标后才可排放
b.为保护好水资源,禁止使用化肥和农药
c.天然水只要通过处理后变清即可饮用
d.为了改善水质,可向其中加入大量的净水剂和消毒剂
②“赤潮”或“水华”主要是由于水中某些营养元素含量过高,导致藻类大量繁殖,消耗氧气,使鱼类等死亡.这里的营养元素主要指(写出一种即可).
(3)、“空气更清新”需要监测防治大气污染.①目前未计入空气污染指数监测项目的有(填字母).
a.一氧化碳 b.二氧化氮 c.可吸入颗粒物 d.稀有气体
②硝酸工厂排放的尾气中常含有 NO、NO2等有害气体,可用氢氧化钠溶液来吸收: 的化学式为.
19. 《天工开物》记载:“凡取煤经历久者,从土面能辨有无之色,然后掘挖。深至五丈许,方始得煤,初见煤端时,毒气灼人。有将巨竹凿去中节,尖锐其末,插入炭中,其毒烟从竹中透上。人从其下施攫拾取者(如图)。”回答下列问题: (1)、煤属于(填“可再生”或“不可再生”)能源。“毒气灼人”,煤矿中的“毒气”的主要成分是甲烷,遇火会发生爆炸,主要反应的化学方程式为。(2)、“巨竹凿去中节”使竹子整体贯通,此竹筒相当于实验室中的(填仪器名称)。煤堆中心温度比地表高,利用竹筒可将“毒气”导出,原因是。(3)、煤燃烧产生的导致的环境问题是。(4)、为了防止煤矿的矿井发生瓦斯爆炸事故,下列做法可行的是 (填序号)。A、进矿井前先做灯火实验 B、矿井内要加强通风 C、安装瓦斯探头传感器监测瓦斯浓度20.
(1)、煤属于(填“可再生”或“不可再生”)能源。“毒气灼人”,煤矿中的“毒气”的主要成分是甲烷,遇火会发生爆炸,主要反应的化学方程式为。(2)、“巨竹凿去中节”使竹子整体贯通,此竹筒相当于实验室中的(填仪器名称)。煤堆中心温度比地表高,利用竹筒可将“毒气”导出,原因是。(3)、煤燃烧产生的导致的环境问题是。(4)、为了防止煤矿的矿井发生瓦斯爆炸事故,下列做法可行的是 (填序号)。A、进矿井前先做灯火实验 B、矿井内要加强通风 C、安装瓦斯探头传感器监测瓦斯浓度20.结合下图回答问题。
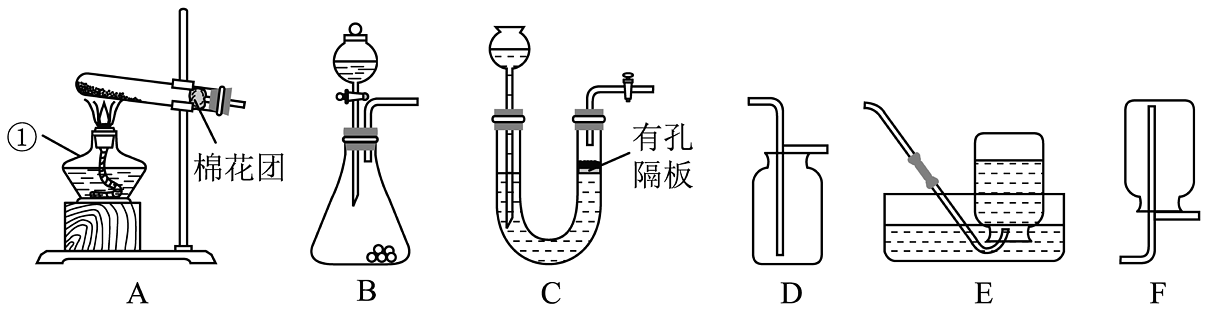
(1)仪器名称:①。
(2)实验室用高锰酸钾制氧气,选用的发生装置是(选填序号),反应的化学方程式为。
(3)实验室用锌粒与稀硫酸反应制氢气,选用发生装置C相对于装置B的优点是。
通常状况下,SO2气体密度比空气大,有毒,易溶于水。实验室常用亚硫酸钠(Na2SO3)固体与浓硫酸在常温下反应制取SO2 , 实验室选择下图装置收集SO2(图1)并验证其性质(图2)。

(4)图1“防倒吸装置”应选择(选填“甲”或“乙”)。
(5)图1NaOH溶液的作用是。
(6)已知SO2也能与水反应,生成亚硫酸(H2SO3),亚硫酸溶液呈酸性。如图2所示,把充满SO2的试管倒立在滴有紫色石蕊的水中,可看到的现象是。
21. 金属钴(Co)在国防工业中有重要应用.某矿石中含钴的氧化物(CoO、Co2O3).研究人员在实验室用硫酸酸浸的方法提取钴元素,并探究最佳提取条件。(1)、写出下列化合物中 Co元素的化合价:CoO , Co2O3.(2)、酸浸时钴的氧化物发生如下反应:反应Ⅰ
反应Ⅱ
反应Ⅲ Co
①反应后溶液中含钴元素的微粒是(填化学符号).
②已知反应前矿石中CoO的质量为 ag,Co2O3的质量为 bg,则理论上可以生成CoSO4g(用含 a、b的式子表示).
(3)、为探究最佳提取条件,将矿石在一定条件下酸浸4 小时,测量钴元素的浸出率,部分数据如下:编号
矿石用量(g)
硫酸用量(g)
Na2SO3 用量(g)
温度(℃)
钴元素浸出率(%)
1
85.71
12.62
0
85
56.39
2
85.71
6.31
0
85
49.98
3
85.71
6.31
0
65
43.33
4
85.71
6.31
0.43
65
73.95
5
85.71
6.31
0.86
65
74.77
①本实验研究了哪些因素对钴元素浸出率的影响?;
②根据上表数据,其他条件不变,温度升高,钴元素的浸出率;
③工业生产中采用实验(填编号)的提取条件更合理.
22. 小王发现厨房所用炉具清洁剂的有效成分是氢氧化钠,为测定该炉具清洁剂中氢氧化钠的质量分数,他进行了如下实验:取100g该炉具清洁剂于烧杯中,加入50g溶质质量分数为9.8%的稀硫酸恰好完全反应。(炉具清洁剂中的其他成分不与稀硫酸反应)(1)、计算该炉具清洁剂中氢氧化钠的质量分数(请写出计算过程)。(2)、炉具清洁剂在不用时需密封保存的原因是________。23. 酸碱度与人体健康我们知道许多物质具有酸性或碱性。其实,人体的体液也有一定的酸碱性,且其酸碱度保持在一个相对稳定的范围内,这样才能维持人体正常的生命活动。人体血液的量较多,分布广,正常人体血浆pH为7.35﹣7.45。氧气充足时,人体摄取的糖类、脂肪、蛋白质会被彻底氧化分解,最终生成CO2和H2O,在组织细胞与血液之间进行气体交换时,CO2扩散到血液中,会引起血浆的pH略有改变。
人体胃液担负着食物的消化,pH为0.9﹣1.5。20世纪初科学家在人体胃内发现了幽门螺杆菌,幽门螺旋杆菌能引起慢性胃炎,它主要是通过其产生的脲酶分解尿素产生氨而中和人体胃酸,导致人体胃内酸碱失衡,胃液分泌异常。

如图是一组胃病患者在空腹状态下24小时胃液pH的变化曲线。科学家发现人体胃液的pH影响人体对药物的吸收,胃液pH低时,胃液分泌多,胃对弱酸性类药物的吸收相对多;胃液pH高时,胃液分泌少,有利于弱碱性类药物的吸收。
依据文章内容回答下列问题:
(1)、正常人体血浆呈(填“弱酸性”或“弱碱性”)。(2)、CO2扩散到血液,血浆的pH会(填“增大”或“减小”),原因是(用化学方程式表示)。(3)、脲酶分解尿素反应的化学方程式为CO(NH2)2+H2OX+2NH3↑,则X的化学式。(4)、分析上图,患者服用含氢氧化铝的胃药时,最适宜的用药时间为。(5)、下列说法正确的是(填写序号)。A.胃酸能帮助消化食物,胃酸分泌越多越有利于人体健康
B.患者的用药时间也会影响到药效
C.患者在上午九点左右服用弱酸性类药物时吸收最好