人教版(五四学制)化学九年级上册单元测试-第二单元 溶液(基础卷)
试卷更新日期:2025-08-30 类型:单元试卷
一、选择题
-
1. 下列关于溶液的说法正确的是A、溶液都是无色透明的液体 B、气体、液体、固体都可以作为溶液的溶质 C、溶液由溶质和溶剂组成,所以溶液的质量和体积等于溶质和溶剂的质量和体积 D、溶液具有均一性、稳定性,所以具有均一性、稳定性的液体都是溶液2. 要使如图装置中的小气球鼓起来,则使用的固体和液体可以是

①石灰石和稀盐酸;②镁和稀盐酸;③氢氧化钠和水;④硝酸铵和水
A、①②③④ B、①②③ C、①②④ D、②③④3. 溶液用途广泛,与人们的生活息息相关。下列说法正确的是A、碘酒中的溶剂是酒精 B、只有固体和液体可以作为溶质 C、降低饱和溶液的温度后,溶液中溶质的质量分数一定减小 D、饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液4. 农业上常用质量分数为16%的NaCl溶液选种。实验室配制100 g该浓度溶液的过程如下图所示。下列说法不正确的是 A、实验操作顺序为④②①⑤③ B、①中有部分固体洒落所得溶液的浓度偏大 C、选用100 mL量筒量取所需水的体积 D、⑤中量取水时,仰视读数,导致溶浓度变小5. 甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( ).
A、实验操作顺序为④②①⑤③ B、①中有部分固体洒落所得溶液的浓度偏大 C、选用100 mL量筒量取所需水的体积 D、⑤中量取水时,仰视读数,导致溶浓度变小5. 甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示,下列说法中正确的是( ). A、甲的溶解度比乙大 B、t2℃时,甲、乙的溶液中溶质的质量分数相等 C、t1℃时,将50g水加入15g甲物质中,可得到65g溶液 D、要使接近饱和的乙溶液转化为饱和溶液,可采用蒸发溶剂的方法6. 生活中处处有化学,下列情境的解释,错误的是A、空气中的氖气可制作霓虹灯 B、二氧化硫是计入空气质量评价的主要污染物之一 C、家用煤气泄漏时扩散出来的CO是有刺激性气味的有毒气体 D、汽水等碳酸型饮料的生产过程中,用增大压强的方法使更多的CO2溶解到水中7. 农业上常用溶质质量分数为16%的NaCl溶液选种。实验室配制100g该溶液的过程如下图所示。下列说法错误的是( )
A、甲的溶解度比乙大 B、t2℃时,甲、乙的溶液中溶质的质量分数相等 C、t1℃时,将50g水加入15g甲物质中,可得到65g溶液 D、要使接近饱和的乙溶液转化为饱和溶液,可采用蒸发溶剂的方法6. 生活中处处有化学,下列情境的解释,错误的是A、空气中的氖气可制作霓虹灯 B、二氧化硫是计入空气质量评价的主要污染物之一 C、家用煤气泄漏时扩散出来的CO是有刺激性气味的有毒气体 D、汽水等碳酸型饮料的生产过程中,用增大压强的方法使更多的CO2溶解到水中7. 农业上常用溶质质量分数为16%的NaCl溶液选种。实验室配制100g该溶液的过程如下图所示。下列说法错误的是( ) A、实验操作顺序为④②①⑤③ B、选用100mL量筒量取所需水的体积 C、需称量NaCl的质量为16.0g D、②中游码在6g处,则食盐实际质量为16g8. 将某碳酸饮料拧开,倒入装有冰块的杯中,如图。下列分析合理的是
A、实验操作顺序为④②①⑤③ B、选用100mL量筒量取所需水的体积 C、需称量NaCl的质量为16.0g D、②中游码在6g处,则食盐实际质量为16g8. 将某碳酸饮料拧开,倒入装有冰块的杯中,如图。下列分析合理的是 A、拧开瓶盖后,二氧化碳溶解度变大 B、产生气泡的原因是饮料与冰发生化学反应 C、冒泡刚结束时,饮料仍然是二氧化碳的饱和溶液 D、图中现象能说明二氧化碳溶解度与压强、温度的关系9. 下列实验设计能达到实验目的的是
A、拧开瓶盖后,二氧化碳溶解度变大 B、产生气泡的原因是饮料与冰发生化学反应 C、冒泡刚结束时,饮料仍然是二氧化碳的饱和溶液 D、图中现象能说明二氧化碳溶解度与压强、温度的关系9. 下列实验设计能达到实验目的的是实验目的
A.探究NH3和CO2在水中溶解能力的大小
B.验证质量守恒定律
C.探究铁锈蚀的条件
D.证明MnO2能作为H2O2分解的催化剂
实验设计



 A、A B、B C、C D、D10. 在家务劳动中感悟化学原理。下列家务劳动涉及的化学知识正确的是
A、A B、B C、C D、D10. 在家务劳动中感悟化学原理。下列家务劳动涉及的化学知识正确的是选项
家务劳动
化学知识
A
用天然气作燃料生火做饭
天然气的成分是CO和H2
B
用洗洁精清洗餐具
洗洁精与油污发生中和反应
C
用食盐调节汤的咸淡
食盐和水的比例影响NaCl的浓度
D
用扇子扇煤炉火
提高煤的着火点
A、A B、B C、C D、D11. 如图为Na2SO4与NaCl的溶解度曲线,下列说法正确的是 A、30℃时,Na2SO4的溶解度为41 B、P点表示该温度下,两饱和溶液中溶质质量相等 C、20℃时,Na2SO4饱和溶液的溶质质馓分数为19.5% D、若氯化钠中含有少量硫酸钠,则提纯氯化钠的方式为蒸发结晶,趁热过滤,洗涤,干燥12. 打开啤酒瓶盖时,你会发现啤酒会自动喷出,喝了啤酒后又常常会打嗝,这说明气体的溶解性与外界的压强和温度有关。下列关于气体溶解度的说法不正确的是A、压强增大,气体的溶解度增大 B、温度升高,气体的溶解度增大 C、压强减小,气体的溶解度减小 D、温度升高,气体的溶解度减小13. 某小组借助传感器研究稀氢氧化钠溶液与稀盐酸发生的中和反应,三颈烧瓶中盛放X溶液,用恒压滴液漏斗(漏斗内压强不变)匀速滴加另一种溶液,如图 1所示。用pH传感器测定三颈烧瓶内溶液的pH,pH随时间的变化如图2所示。下列说法中正确的是( )
A、30℃时,Na2SO4的溶解度为41 B、P点表示该温度下,两饱和溶液中溶质质量相等 C、20℃时,Na2SO4饱和溶液的溶质质馓分数为19.5% D、若氯化钠中含有少量硫酸钠,则提纯氯化钠的方式为蒸发结晶,趁热过滤,洗涤,干燥12. 打开啤酒瓶盖时,你会发现啤酒会自动喷出,喝了啤酒后又常常会打嗝,这说明气体的溶解性与外界的压强和温度有关。下列关于气体溶解度的说法不正确的是A、压强增大,气体的溶解度增大 B、温度升高,气体的溶解度增大 C、压强减小,气体的溶解度减小 D、温度升高,气体的溶解度减小13. 某小组借助传感器研究稀氢氧化钠溶液与稀盐酸发生的中和反应,三颈烧瓶中盛放X溶液,用恒压滴液漏斗(漏斗内压强不变)匀速滴加另一种溶液,如图 1所示。用pH传感器测定三颈烧瓶内溶液的pH,pH随时间的变化如图2所示。下列说法中正确的是( )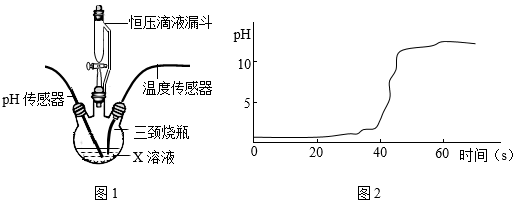 A、若将恒压滴液漏斗换成长颈漏斗,实验结果一样 B、X溶液是氢氧化钠溶液 C、实验进行到20 s时,溶液中的溶质为稀盐酸、氯化钠 D、实验中溶液的温度随时间变化的曲线与pH曲线相同14. 为探究物质溶解过程中的能量变化,某同学设计图Ⅰ所示装置.在盛有水的烧杯中放入一装有饱和硝酸钾溶液的试管,向水中加入足量物质X,搅拌.结合图Ⅱ硝酸钾溶解度曲线,对硝酸钾溶液变化的推断,合理的是( ).
A、若将恒压滴液漏斗换成长颈漏斗,实验结果一样 B、X溶液是氢氧化钠溶液 C、实验进行到20 s时,溶液中的溶质为稀盐酸、氯化钠 D、实验中溶液的温度随时间变化的曲线与pH曲线相同14. 为探究物质溶解过程中的能量变化,某同学设计图Ⅰ所示装置.在盛有水的烧杯中放入一装有饱和硝酸钾溶液的试管,向水中加入足量物质X,搅拌.结合图Ⅱ硝酸钾溶解度曲线,对硝酸钾溶液变化的推断,合理的是( ).
①X 为 NaCl 固体,试管中无晶体析出,硝酸钾溶液仍是饱和溶液
②X为 NaOH 固体,试管中无晶体析出,硝酸钾溶液仍是饱和溶液
③X为 NH4NO3晶体,试管中有晶体析出,硝酸钾溶液仍是饱和溶液
④X 为浓 H2SO4 , 试管中无晶体析出,硝酸钾溶液为不饱和溶液
A、①②③ B、①③④ C、①②④ D、②③④15. 水是常见的溶剂。“果蔬洗盐”是一种果蔬清洁剂,某“果蔬洗盐”的部分标签如图1所示,配料中物质的溶解度曲线如图2所示。下列说法正确的是 A、取15g“果蔬洗盐”放入1kg20℃的水中,形成的溶液是NaCl的饱和溶液 B、任取“果蔬洗盐”溶液中的各部分,清洗果蔬的效果不一样 C、提纯含有少量Na2CO3的NaCl样品,可用溶解→蒸发→过滤的方法,其中过滤要在40℃左右进行 D、20℃时,NaHCO3的饱和溶液溶质质量分数为10%
A、取15g“果蔬洗盐”放入1kg20℃的水中,形成的溶液是NaCl的饱和溶液 B、任取“果蔬洗盐”溶液中的各部分,清洗果蔬的效果不一样 C、提纯含有少量Na2CO3的NaCl样品,可用溶解→蒸发→过滤的方法,其中过滤要在40℃左右进行 D、20℃时,NaHCO3的饱和溶液溶质质量分数为10%二、非选择题
-
16. 生活与化学密切相关。(1)、打开汽水瓶盖时,汽水会自动喷出来,这些说明气体在水中的溶解度随的减小而减小。(2)、焊锡的熔点 , 可用于焊接金属。(3)、木炭由于具有很强的性,可以清除冰箱内的异味。(4)、加碘食盐中的碘是指(填序号)______。A、分子 B、原子 C、元素 D、电子(5)、生活中,常用的方法降低水硬度。(6)、餐具上的油污可以用加入水的洗涤剂洗掉,这是由于洗涤剂有功能。17. KCl和KNO3在不同温度下的溶解度数据如下表:
温度/℃
0
10
20
30
40
50
60
溶解度/g
KNO3
13.3
20.9
31.6
45.8
63.9
85.5
110
KCl
27.6
31.0
34.0
37.0
40.0
42.6
45.5
(1)、30℃时,KCl的溶解度是g。(2)、如图是KCl和KNO3的溶解度曲线,则KNO3的溶解度曲线是(选填“甲”或“乙”)。 (3)、t1的取值范围是。(4)、t1℃时,将等质量的甲、乙饱和溶液升温至t2℃,溶质质量分数:甲(选填“>”、“=”或“<”)乙。18. 根据所学知识回答:(1)、如图是某同学配制溶质质量分数为18%的NaCl溶液的实验操作示意图,据图回答下列问题:
(3)、t1的取值范围是。(4)、t1℃时,将等质量的甲、乙饱和溶液升温至t2℃,溶质质量分数:甲(选填“>”、“=”或“<”)乙。18. 根据所学知识回答:(1)、如图是某同学配制溶质质量分数为18%的NaCl溶液的实验操作示意图,据图回答下列问题:
①配制溶液的步骤是计算、、 、装瓶贴标签;
②在配制过程中,导致溶液中氯化钠质量分数小于18%的可能原因是下列叙述中的(填序号)。
a.用量筒量取水时俯视读数 b.配制溶液的烧杯用少量蒸馏水润洗
c.固体转移到烧杯时,氯化钠洒出 d.用量筒量取水时仰视读数
(2)、根据下图回答问题:
①仪器①名称:。
②实验室制取CO2可选择的发生装置和收集装置是(填字母,写一组即可),D装置的优点是。
③在常温下,用浓氨水与固体烧碱混合也可以制取氨气,但需要控制好反应的速率,你选择上图中发生装置(填字母)制取氨气。
19. R 是硝酸钾或氯化铵中的一种。硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组的同学进行了如图2所示的实验。 (1)、t1℃时,将 30g 氯化铵固体溶解在 50g 水中,形成溶液的质量是 g。(2)、在图2中,②的溶液中溶质质量分数为 。(3)、根据以上信息可推出 R 是 (填“硝酸钾”或“氯化铵”)。(4)、关于图 2 中烧杯内的物质,以下几种说法正确的有 (填序号)。
(1)、t1℃时,将 30g 氯化铵固体溶解在 50g 水中,形成溶液的质量是 g。(2)、在图2中,②的溶液中溶质质量分数为 。(3)、根据以上信息可推出 R 是 (填“硝酸钾”或“氯化铵”)。(4)、关于图 2 中烧杯内的物质,以下几种说法正确的有 (填序号)。A①、②、③中,只有③中上层清液是饱和溶液
B若使③中的固体溶解,可采用加水或升温的方法
C①和②的溶液中,溶质质量相等
D①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数小
20. 某化工有限公司生产的硫酸铜溶液的标签示意图如下图,根据标签计算:200mL
品名:硫酸铜溶液
溶质质量分数:20%
密度:1.2g/mL
XX化工有限公司
(1)、这瓶硫酸铜溶液中溶剂的质量是;(直接填结果)(2)、现需要配制2400g溶质质量分数为12%的硫酸铜溶液,需要溶质质量分数为20%的硫酸铜溶液多少毫升?(写出计算过程)