黑龙江省尚志市2017-2018学年九年级上学期化学期中考试试卷
试卷更新日期:2017-12-11 类型:期中考试
一、单选题
-
1. 下列关于化学的看法错误的是( )A、化学的发展必然导致生态环境的恶化 B、化学可以为人类研制新能源 C、化学会在环境保护中发挥重要作用 D、化学可以为人类研制新材料2. 下列图示中的实验操作,正确的是( )A、
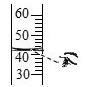
B、
B、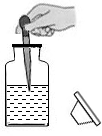
C、
C、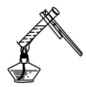
D、
D、
3. 同学们进行了下列实验,主要发生化学变化的是( )A、
3. 同学们进行了下列实验,主要发生化学变化的是( )A、 水的沸腾
B、
水的沸腾
B、 用简易净水器净水
C、
用简易净水器净水
C、 水的电解
D、
水的电解
D、 实验室制取蒸馏水
4. 春天是禽流感多发期,为了防止禽流感的大面积发生,常使用浓度为2%的过氧乙酸溶液喷雾消毒,过氧乙酸的结构式如图所示,下列有关过氧乙酸的说法中不正确的( )
实验室制取蒸馏水
4. 春天是禽流感多发期,为了防止禽流感的大面积发生,常使用浓度为2%的过氧乙酸溶液喷雾消毒,过氧乙酸的结构式如图所示,下列有关过氧乙酸的说法中不正确的( ) A、过氧乙酸的化学式是C2H4O3 B、过氧乙酸中质子数大于中子数 C、过氧乙酸中碳、氢原子的个数比为1:2 D、过氧乙酸是由碳、氢、氧三种原子构成的化合物5. 出去下列物质中的杂质,所选用的试剂和操作均正确的是( )
A、过氧乙酸的化学式是C2H4O3 B、过氧乙酸中质子数大于中子数 C、过氧乙酸中碳、氢原子的个数比为1:2 D、过氧乙酸是由碳、氢、氧三种原子构成的化合物5. 出去下列物质中的杂质,所选用的试剂和操作均正确的是( )选项
物质
杂质(少量)
所选试剂
操作方法
A
H2O
臭味物质
活性炭
吸附
B
N2
O2
足量木炭粉
点燃
C
KCl
KClO3
少量的MnO2
加热后冷却
D
CuO
C
足量氧气
灼烧
A、A B、B C、C D、D6. 某农场需要购置NH4NO3和CO(NH2)2两种化肥总质量为100kg,经测得其中含氢元素的质量分数为6%,则两种化肥中含氮元素的总质量为( )
A、36kg B、40kg C、42kg D、50kg二、简答题
-
7. 请根据图中信息回答下列问题:

⑴投入几小块烘烤过的木炭,红棕色会消失的原因
是:

⑵防毒面具中滤毒罐填充的物质是(填名称)

⑶氧化铜和氢气在加热的条件下反应的方程式:

⑷铁钉和硫酸铜溶液反应前后质量测定整个实验中观察的现象是:
8. 在实验室中,硝酸(HNO3)必须保存在如右图的棕色细口瓶中,原因是硝酸见光分解,生成一种能污染大气的红棕色气体,一种能供给呼吸的气体和另外一种常见的氧化物。打开瓶盖用手煽动时,会闻到刺激性气味。
请回答:
(1)、硝酸的性质有;(2)、请写出硝酸在光照的条件下分解的化学方程式 , 反应前氮元素化合价为。9. 用“○”和“●”分别表示氢原子和氧原子,下图是氢气和氧气在点燃条件下发生反应的微观模拟图。请回答下列问题: (1)、在B图中将相关粒子图形补充完整:补充的依据是;(2)、此变化中发生变化的粒子是;(3)、从微观角度写出此反应由B到C过程的反应实质;10. 分类学习对研究化学知识有帮助,现有下列物质:
(1)、在B图中将相关粒子图形补充完整:补充的依据是;(2)、此变化中发生变化的粒子是;(3)、从微观角度写出此反应由B到C过程的反应实质;10. 分类学习对研究化学知识有帮助,现有下列物质:过氧化氢、金刚石、氯化钠、铜、氧化汞、硫酸铜。
(1)、请根据构成物质的粒子种类,选出部分物质归为一类(填化学式)。分类标准 , 包括物质。
(2)、许多物质的命名与元素的化合价高低有关,如氧化铁、氧化亚铁、其中铁元素的化合价分别为+3价、+2价,硫元素常见的化合价有+6价、+4价、-2价。由此推测价化合物FeS的名称为 , 其中硫元素的化合价为。11. 实验室现有氯酸钾、稀盐酸、大理石、火柴、药匙、镊子、升降台及以下仪器,按要求填写下列空白或回答问题。 (1)、若用上述仪器和药品制取二氧化碳,所需要的仪器编号是① , 写出仪器b的名称是② , 在此实验中的用途是③;(2)、制取气体前需要检查装置的气密性,方法如下,先① , 在将导气管一段浸没水中,最后用手紧握锥形瓶外壁,若观察到②的现象,说明气密性良好。(3)、下图是某学习小组设计的制备并检验二氧化碳的装置,请将其补充完整;
(1)、若用上述仪器和药品制取二氧化碳,所需要的仪器编号是① , 写出仪器b的名称是② , 在此实验中的用途是③;(2)、制取气体前需要检查装置的气密性,方法如下,先① , 在将导气管一段浸没水中,最后用手紧握锥形瓶外壁,若观察到②的现象,说明气密性良好。(3)、下图是某学习小组设计的制备并检验二氧化碳的装置,请将其补充完整; (4)、若补充一种药品① , 还可以制取氧气,则反应的化学方程式为②。12. A、B、C、D、E分别是铁、氧气、二氧化碳、澄清石灰水和木炭粉中的一种物质,用五个圆表示这五种物质,用两圆相交表示两种物质可以发生反应,且D的相对分子质量比B大,请回答下列问题:
(4)、若补充一种药品① , 还可以制取氧气,则反应的化学方程式为②。12. A、B、C、D、E分别是铁、氧气、二氧化碳、澄清石灰水和木炭粉中的一种物质,用五个圆表示这五种物质,用两圆相交表示两种物质可以发生反应,且D的相对分子质量比B大,请回答下列问题: (1)、写出C和D反应的化学方程式为;(2)、A与B反应实验现象为;(3)、物质B和D物质的名称分别为和。13. 化学实验小组收集了“碳还原氧化铜”实验后的固体残渣,发现剩余固体中有黑色固体,于是对黑色固体成分产生了好奇心,准备探究一下黑色固体成分是什么。(1)、【提出猜想】根据反应物和生成物性质猜想黑色固体成分
(1)、写出C和D反应的化学方程式为;(2)、A与B反应实验现象为;(3)、物质B和D物质的名称分别为和。13. 化学实验小组收集了“碳还原氧化铜”实验后的固体残渣,发现剩余固体中有黑色固体,于是对黑色固体成分产生了好奇心,准备探究一下黑色固体成分是什么。(1)、【提出猜想】根据反应物和生成物性质猜想黑色固体成分甲同学猜想:氧化铜;乙同学猜想:碳;丙同学猜想:。
(2)、甲同学猜想的理由是:。(3)、【查阅资料】氧化铜在空气中不燃烧【设计实验】乙同学为了验证自己的猜想,设计实验如图所示,取黑色固体放入试管中加强热,若观察到澄清石灰水变白色浑浊,即可以得出自己猜想的正确的结论。请你对乙同学的结论做出评价。
(4)、【进行实验】丙同学按照乙同学的实验设计进行了实验,观察到的现象是。证明自己的猜想正确,写出黑色固体发生反应的化学方程式。(5)、【反思与总结】根据上述实验探究内容,我们可以总结出在根据实验产生的现象验证物质成分时,需要注意 , 才能准确得出结论。14. 工业上通常用高温加热碳酸钙制取生石灰。甲取碳酸钙200g高温加热一段时间后测得剩余固体质量为156g,乙将剩余固体继续高温加热至完全反应。请你回答下列问题:(1)、写出制取生石灰的化学方程式;(2)、甲实验时产生的气体质量为g;(3)、根据甲产生的气体质量列出解参加反应的碳酸钙的质量(x)的比例式;(4)、乙加热完全反应后得到固体的质量为;(5)、甲、乙两同学实验时消耗碳酸钙的质量比为。