北京市海淀区2017-2018学年九年级上学期化学期中考试试卷
试卷更新日期:2017-12-11 类型:期中考试
一、单选题
-
1. 下列做法中,不符合“爱护资源,保护环境”主张的是( )
A、公交出行 B、焚烧垃圾、秸秆 C、监督举报排污 D、使用节水器具2. 空气成分中,体积分数最大的是( )A、氮气 B、二氧化碳 C、氧气 D、稀有气体3. 地壳中含量最多的元素是( )
A、Si B、Fe C、O D、Al4. 下列物质在空气中燃烧,产生大量白烟的是( )
A、铁丝 B、硫粉 C、木炭 D、红磷5. 生活中“低钠盐”“高钙奶”中的“钠”和“钙”是指( )
A、元素 B、单质 C、原子 D、分子6. 运送酒精的车辆上,应该张贴的图标是( )
A、 B、
B、 C、
C、 D、
D、 7. 钠原子的原子核内有11个质子和12个中子,该原子的核外电子数为( )
7. 钠原子的原子核内有11个质子和12个中子,该原子的核外电子数为( )
A、1 B、23 C、11 D、128. 下列做法符合实验室药品取用规则的是( )
A、用手直接取用药品 B、若未说明用量,按最少量取用 C、将未用完的药品丢弃或带出实验室 D、实验后将剩余药品放回原瓶中9. 王安石用“遥知不是雪,为有暗香来”描写梅花,能从远处闻到花香的原因是( )
A、分子质量很小 B、分子在不断运动 C、分子间有间隔 D、分子由原子构成10. 下列物质中,属于化合物的是( )
A、空气 B、氧气 C、矿泉水 D、四氧化三铁11. 下列符号能表示2个氧分子的是( )
A、2O2 B、O2 C、2O D、2O2-12. 下列物质的用途中,主要利用其物理性质的是( )
A、氢气用于填充气球 B、红磷燃烧测空气中氧气含量 C、氮气用于食品防腐 D、氧气供给呼吸13. 下列元素符号书写正确的是( )
A、锰Mn B、钠NA C、钙Cu D、铝AL14. 下列物质的化学式书写不正确的是( )
A、氧气O2 B、二氧化硫SO2 C、氧化铁FeO D、氯化钠NaCl15. 下列操作或措施符合实验安全的是( )
A、加热时试管口对着他人 B、用嘴吹灭酒精灯 C、酒精洒在桌上燃烧时,立即用湿抹布扑盖 D、用水冷却加热后的试管16. 观察蜡烛燃烧过程中的变化,下列说法不正确的是( )
A、蜡烛燃烧的过程中,既有物理变化也有化学变化 B、蜡烛燃烧的过程中,既有物质变化也有能量变化 C、燃烧后的气体使澄清石灰水变浑浊,发生的是化学变化 D、燃烧后的气体在干燥烧杯壁上冷凝成液滴时,发生的是化学变化17. 下列关于实验操作和目的的说法中,不正确的是( )
A、用小刀切割蜡烛,以研究石蜡的硬度 B、将石蜡放入水中,研究石蜡的密度,以及能否溶于水 C、用火柴去点蜡烛刚熄灭时产生的白烟,以研究白烟能否燃烧 D、将火柴梗迅速平放入火焰中(如下图所示)约1秒后取出,以研究火柴梗能否燃烧18. 通过下列操作和现象,得出的结论可靠的是( )
A、测量蜡烛燃烧后的长度,发现明显短于燃烧前,说明蜡烛发生了化学变化 B、用湿润的烧杯罩在火焰上方,观察到烧杯壁上有液滴,说明蜡烛燃烧时有水产生 C、用涂有澄清石灰水的烧杯罩住蜡烛熄灭时产生的白烟,发现石灰水变浑浊,说明白烟是二氧化碳 D、点燃两支相同的蜡烛,用烧杯将其中一支罩在桌面上,一段时间后烧杯中的蜡烛熄灭,另一支继续燃烧,说明空气中有物质参与了燃烧19. 进一步对蜡烛燃烧进行探究,下列推断中不合理的是( )
A、单独点燃制作烛芯用的棉线,棉线很快燃尽,说明蜡烛燃烧时不仅是棉线在燃烧 B、固态石蜡很难被点燃,说明燃烧可能需要一定的条件 C、由于空气几乎不含碳元素,澄清石灰水变浑浊说明碳元素来自石蜡 D、石蜡燃烧生成水和二氧化碳,说明石蜡中一定含有碳、氢、氧三种元素20. 下图为载人航天器工作仓中气体成分的微观示意图,已知在同温同压下,气体的体积之比等于分子个数之比,下列说法不合理的是( ) A、1个氧分子是由2个氧原子构成的 B、氧分子和氮分子能均匀混合,是因为航天器处于失重状态 C、航天器工作仓内氮气与氧气的体积比与地表空气接近 D、航天器工作仓中充氮气可避免发生火灾后燃烧过于剧烈21. 下列现象能说明我们身边存在空气的是( )(填字母序号)
A、1个氧分子是由2个氧原子构成的 B、氧分子和氮分子能均匀混合,是因为航天器处于失重状态 C、航天器工作仓内氮气与氧气的体积比与地表空气接近 D、航天器工作仓中充氮气可避免发生火灾后燃烧过于剧烈21. 下列现象能说明我们身边存在空气的是( )(填字母序号)
A、快速奔跑时感受到有风吹来 B、把塑料袋抖开后扎紧,感到不易压缩 C、将玻璃杯倒扣在水槽中,水不能充满玻璃杯二、填空题
-
22. 2找一个大小合适的瓶子,将燃着的纸条扔进瓶中,待燃烧结束后迅速将一剥过皮的鸡蛋放在瓶口处,发现鸡蛋慢慢挤入瓶口。瓶内气压(填“大于”“小于”或“等于”)大气压。
23. 在保鲜袋中加入少量酒精,排出袋内空气后封闭,放在热水中,发现保鲜袋迅速鼓起。请从微观角度解释产生上述现象的原因。 24. 空气质量是城市的名片,如何改善空气质量是很多大城市需要解决的问题之一
24. 空气质量是城市的名片,如何改善空气质量是很多大城市需要解决的问题之一
(1)、下列属于空气污染物的是 (填字母序号)A、CO2 B、SO2 C、N2 D、PM2.5(2)、拥堵公路上的空气使人感到呼吸不畅,而在茂密森林中的空气却使人感到清新舒畅,你认为可能的原因是。25. “液氮冰淇淋”是一种用液氮作制冷剂,使奶油等原料快速冻结而制成的冰淇淋。冻结时原料中的水迅速凝结成微小冰晶,来不及聚集,所以吃起来柔滑,无冰渣感。
(1)、氮气的化学式是。(2)、制作“液氮冰淇淋”时利用的氮气的性质包括、。26. “智能加热器”是液体蚊香的好搭档,可以定时加热,自动停止,减少蚊香液的浪费。从微观角度看,蚊香液逐渐减少的原因是 , 据此推测可能影响微粒运动的快慢的因素是。
27. 乒乓球是中国的国球。参加国际比赛用的乒乓球曾经由易燃材料“赛璐珞”制成,需要装在低温集装箱里通过海运或公路运输。2014年,乒乓球开始使用“聚酯纤维”这种不易燃的新材料制作,从此乒乓球也可以“乘”飞机出行了。
(1)、硝化纤维是生产赛璐珞的原料之一,其化学式为C12H16O6(NO2)4 , 其中含有种元素。
(2)、最早的聚酯纤维是用对苯二甲酸(化学式为C8H6O4)和乙二醇(化学式为C2H6O2)为原料制成的。乙二醇中碳、氢元素的质量比为。28. 中国航天科技一直以来备受世界瞩目。2017年9月2日,我国成功提纯了“超级金属”铼。铼及其合金被广泛应用到航空航天领域。金属铼硬度大,熔点很高,在高温下能与硫化合形成二硫化铼。 (1)、铼的相对原子质量是。(2)、上述信息中,属于金属铼的物理性质的是。(3)、七氧化二铼(Re2O7)是铼最常见的氧化物,其中铼元素的化合价为。29. 水对航天员的生存非常重要,目前航天器中水的来源包括:
(1)、铼的相对原子质量是。(2)、上述信息中,属于金属铼的物理性质的是。(3)、七氧化二铼(Re2O7)是铼最常见的氧化物,其中铼元素的化合价为。29. 水对航天员的生存非常重要,目前航天器中水的来源包括:①从地面携带水。
②由氢氧燃料电池提供水,氢气和氧气在一定条件下发生反应,为飞船提供能量,同时生成水。请写出相关文字表达式:。
③通过蒸发和冷凝,把尿液中的水和呼吸产生的水蒸气收集起来,处理再生。蒸发与冷凝过程中,分子的种类(填“改变”或“不变”)。
30. 铝镓合金是铝和镓混合,用氩气做保护气,加热熔合成的具有金属性质的物质。
(1)、铝元素属于元素(填“金属”或“非金属”)。(2)、氩气可以做保护气,是因为。31. 美国普度大学研发出一种利用铝镓合金制备氢气的新工艺,流程如下图所示: (1)、氧化铝(Al2O3)制得铝的反应中,铝元素的化合价(填“升高”“降低”或“不变”)。(2)、氧化铝中的氧元素来自于。(3)、上述过程中,涉及到的氧化物有。(4)、氧化铝可以借助太阳能电池重新变成氧气与金属铝,该反应的反应类型是(填“化合反应”或“分解反应”)。
(1)、氧化铝(Al2O3)制得铝的反应中,铝元素的化合价(填“升高”“降低”或“不变”)。(2)、氧化铝中的氧元素来自于。(3)、上述过程中,涉及到的氧化物有。(4)、氧化铝可以借助太阳能电池重新变成氧气与金属铝,该反应的反应类型是(填“化合反应”或“分解反应”)。
32. 下图中的物质都是初中化学常见的纯净物。 (1)、“花瓣”上的物质从物质类别上看,都属于。(2)、每一片“花瓣”上的物质都能与“花心”中的物质甲发生化学反应,其中C与甲反应的文字表达式为 , 该反应属于(填“化合反应”或“分解反应”)。反应的现象是 , 同时放出大量的热。(3)、若物质甲与H2反应后生成物质的微观示意图为
(1)、“花瓣”上的物质从物质类别上看,都属于。(2)、每一片“花瓣”上的物质都能与“花心”中的物质甲发生化学反应,其中C与甲反应的文字表达式为 , 该反应属于(填“化合反应”或“分解反应”)。反应的现象是 , 同时放出大量的热。(3)、若物质甲与H2反应后生成物质的微观示意图为 ,则构成物质甲的微观粒子示意图可表示为。 33. 请从35-A或35-B两题中任选一个作答,若两题均作答,按35-A计分。
,则构成物质甲的微观粒子示意图可表示为。 33. 请从35-A或35-B两题中任选一个作答,若两题均作答,按35-A计分。35-A液体药品的取用
35-B液体药品的加热
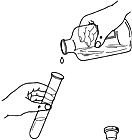
以上操作的错误之处有①、②

以上操作的错误之处有①、②
34. 用如下图所示的装置进行实验。 (1)、实验前,另取少量酚酞溶液,向其中滴加浓氨水,观察到酚酞溶液变红。这一操作的目的是。
(1)、实验前,另取少量酚酞溶液,向其中滴加浓氨水,观察到酚酞溶液变红。这一操作的目的是。
(2)、实验中观察到酚酞溶液变红,这一现象说明分子具有的性质是。
三、实验探究题
-
35. 阅读下面的科普短文。
水是地球上最常见的物质之一,生命的孕育和维系都需要水,关于它的传闻有很多。
传闻1:自来水中有余氯,不能饮用。
自来水从自来水厂到用户家可能需要经过几十公里的管道,为了保证水质,必须在水里加入一些消毒剂以防止细菌滋生。最常用的消毒剂就是氯气,此外还有氯胺和二氧化氯等。根据世界卫生组织的余氯标准推算,如果氯全部来自于饮用水,则自来水中氯的允许含量为5 mg/L。而根据我国《生活饮用水卫生标准》,水厂出厂水中余氯不得高于4 mg/L。由于传输损失,管网末端用户处的自来水中余氯含量远低于允许上限。为维持消毒效果,国家规定管网末端自来水中余氯下限为0.05 mg/L。
传闻2:煮过很多次的“千滚水”有毒。
有研究对多次煮沸水中亚硝酸盐情况进行实验分析,实验的数据如表1所示。
表1 不同煮沸次数的水中亚硝酸盐含量(mg/L)
水样类型
亚硝酸盐含量
一次沸水
0.0008
二次沸水
0.0020
三次沸水
0.0028
人体长时间摄入超标的亚硝酸盐,会增加患癌症的可能性。但是在这个实验中可以看到,即使三次煮沸的水中,亚硝酸盐含量比我国天然矿泉水中亚硝酸盐标准(0.1 mg/L)还低不少。从饮用水健康的角度来看,相比对开水中亚硝酸盐的忧虑,我们更应该注意如果不将水煮开,或者密封、储存方法不当,饮用水中可能存在细菌污染的隐患。
传闻3:常喝“富氧水”能够抗衰老。
富氧水原是医学界为了研究生物细胞厌氧性和好氧性的研究用水,是通过人为地往纯净水里充入更多的氧气制成的。
对于富氧水对健康的影响,学术界存在争议。有研究认为若水中氧含量过高或常喝富氧水会加速氧化,使人体衰老。无论是吸氧还是喝氧, 对健康人都是弊多利少。人们在“ 喝氧” 的问题上应采取慎重态度, 勿作非明智的选择。
依据文章内容回答下列问题。
(1)、为保证水质,可用的自来水消毒剂包括。(2)、判断传闻1真假,并说明理由:。(3)、依据文中数据,煮沸的水中亚硝酸盐含量的变化规律是。(4)、传闻3的资料中,反映出的氧气性质有。(5)、下列关于水的说法不正确的是 (填字母序号)。A、如果自来水中含氯量过低,水中细菌就可能超标 B、因为“千滚水”含有亚硝酸盐,所以有毒而不能饮用 C、“富氧水”中富含氧气,适合多喝36. 实验室用高锰酸钾制取氧气,并验证氧气的化学性质。 (1)、图A装置用于高锰酸钾制取氧气,发生反应的文字表达式为 , 用排水法收集气体,利用的氧气性质是。
(1)、图A装置用于高锰酸钾制取氧气,发生反应的文字表达式为 , 用排水法收集气体,利用的氧气性质是。
(2)、如图B所示,可观察到铁丝在氧气中剧烈燃烧,放出大量热,。该反应的文字表达式为。37. 某同学用右图所示仪器和药品研究吸入空气和呼出气体的成分。
已知:二氧化碳可以使燃着的木条熄灭。
(1)、向盛有呼出气体的集气瓶中滴加澄清石灰水,石灰水变浑浊不能说明呼出气体中二氧化碳含量比空气中多。若要证明这一观点,还需要补充进行的实验是。
(2)、将燃着的木条伸入盛有呼出气体的集气瓶中,观察到木条熄灭,下列说法不合理的是( )A、木条在空气中能够燃烧,说明空气中有氧气 B、木条在空气中能够燃烧,说明空气中不含二氧化碳 C、因为木条熄灭,所以呼出的气体是二氧化碳38. 实验小组同学用右图所示装置进行空气中氧气含量的测定。集气瓶的容积为350mL,实验时先在集气瓶中加入50mL水。 (1)、装置连接好后,检验气密性的方法是。(2)、用弹簧夹夹紧胶皮管,点燃燃烧匙内足量的红磷后,立即伸入瓶中并把塞子塞紧。红磷燃烧的文字表达式为。(3)、待红磷熄灭并冷却后打开弹簧夹,最终集气瓶中水的体积约为 mL,说明实验成功。打开弹簧夹后集气瓶内压强的变化为。(4)、下列有关该实验的说法中,正确的是 (填字母序号)。A、实验过程中可以不使用弹簧夹 B、燃烧匙中的红磷可以换成木炭 C、该实验可以说明氮气难溶于水 D、该实验可以说明空气是混合物39. 小林同学在体育课上腿部擦伤,医务室的大夫在她伤口上涂了医用过氧化氢溶液,小林看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?
(1)、装置连接好后,检验气密性的方法是。(2)、用弹簧夹夹紧胶皮管,点燃燃烧匙内足量的红磷后,立即伸入瓶中并把塞子塞紧。红磷燃烧的文字表达式为。(3)、待红磷熄灭并冷却后打开弹簧夹,最终集气瓶中水的体积约为 mL,说明实验成功。打开弹簧夹后集气瓶内压强的变化为。(4)、下列有关该实验的说法中,正确的是 (填字母序号)。A、实验过程中可以不使用弹簧夹 B、燃烧匙中的红磷可以换成木炭 C、该实验可以说明氮气难溶于水 D、该实验可以说明空气是混合物39. 小林同学在体育课上腿部擦伤,医务室的大夫在她伤口上涂了医用过氧化氢溶液,小林看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?
I.小林准备用如下图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气。记录2分钟收集的气体体积。
 (1)、请写出过氧化氢分解的文字表达式:。(2)、若要检验生成的气体是否为氧气,可将导气管从水中取出,取带火星的木条放在 导气管口处,观察到 , 说明生成的气体是氧气。(3)、II.小林查阅了相关资料,并进行了探究实验
(1)、请写出过氧化氢分解的文字表达式:。(2)、若要检验生成的气体是否为氧气,可将导气管从水中取出,取带火星的木条放在 导气管口处,观察到 , 说明生成的气体是氧气。(3)、II.小林查阅了相关资料,并进行了探究实验【查阅资料】
①过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
②温度对化学反应的快慢有影响,人体正常体温是37℃。
【提出猜想】
猜想1: 过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2: 过氧化氢分解加快是因为伤口中有过氧化氢酶。
【进行实验】

实验①得出的结论是。
(4)、实验②中第一次收集到的氧气体积为 mL。(5)、实验②中横线部分应进行的操作是。(6)、【实验反思】小林反思了实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的结论可能存在不足。因此又补充进行了几组实验,数据记录如下表所示。
加入过氧化氢酶
不加过氧化氢酶
反应温度/ ℃
25
37
42
25
37
42
收集到气体体积/ mL
39
56
34
5
5
5
通过这些数据,你能得出的新结论是。