浙江省温州市十校联合体2015-2016学年高一上学期化学期中考试试卷
试卷更新日期:2017-12-06 类型:期中考试
一、选择题
-
1. 中国女药学家屠呦呦因发现青蒿素对疟疾的治疗作用而成为2015年诺贝尔生理医学奖获得者之一.下列说法不正确的是( )
 A、从青蒿中提取青蒿素的方法是以萃取原理为基础,萃取是一种化学变化 B、青蒿素的分子式为C15H22O5 , 它属于有机物 C、人工合成青蒿素经过了长期的实验研究,实验是化学研究的重要手段 D、现代化学分析测试中,可用元素分析仪确定青蒿素中的C,H,O元素2. 下列各组物质按酸、碱、盐分类顺次排列.正确的是( )A、硫酸、纯碱、碳酸钙 B、硝酸、烧碱、食盐 C、冰醋酸、纯碱、醋酸钠 D、盐酸、熟石灰、苛性钠3. 最先发现电子的科学家是( )A、道尔顿 B、玻尔 C、汤姆生 D、卢瑟福4. 如果你家里的食用花生油不小心混入了大量的水,利用你所学的知识,最简便的分离方法是( )A、
A、从青蒿中提取青蒿素的方法是以萃取原理为基础,萃取是一种化学变化 B、青蒿素的分子式为C15H22O5 , 它属于有机物 C、人工合成青蒿素经过了长期的实验研究,实验是化学研究的重要手段 D、现代化学分析测试中,可用元素分析仪确定青蒿素中的C,H,O元素2. 下列各组物质按酸、碱、盐分类顺次排列.正确的是( )A、硫酸、纯碱、碳酸钙 B、硝酸、烧碱、食盐 C、冰醋酸、纯碱、醋酸钠 D、盐酸、熟石灰、苛性钠3. 最先发现电子的科学家是( )A、道尔顿 B、玻尔 C、汤姆生 D、卢瑟福4. 如果你家里的食用花生油不小心混入了大量的水,利用你所学的知识,最简便的分离方法是( )A、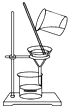 B、
B、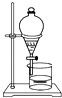 C、
C、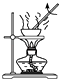 D、
D、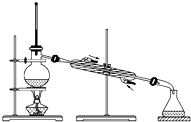 5. 下列化学用语中,不正确的是( )A、钠离子结构示意图为:
5. 下列化学用语中,不正确的是( )A、钠离子结构示意图为: B、质子数为6,中子数为8的原子为:14C
C、H,D,T互为同位素
D、液态的氯气称为氯水
6. 下列类型的反应,一定发生电子转移的是( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应7. 下列关于胶体的叙述不正确的是( )A、胶体区别于其他分散系的本质特征是分散质的微粒直径在10﹣9~10﹣7m之间 B、光线透过胶体时,胶体中可发生丁达尔效应 C、用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同 D、Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的8. 关于萃取的理解,下列说法正确的是( )A、可以用四氯化碳把溴水中的溴萃取出来,静置分层后,上层呈橙红色 B、可以用酒精萃取碘水中的碘 C、可以用水做萃取剂把碘从四氯化碳溶液中分离出来 D、萃取之后一般通过分液的方法将互不相溶的液体分离9. 下列关于氯气和氯水的说法中正确的是( )A、氯气是一种无色、密度比空气大的有毒气体 B、红热的铁丝在Cl2中剧烈燃烧生成FeCl2 C、新制氯水能杀菌消毒是因为Cl2有毒,能毒杀细菌 D、氯水放置数天后酸性增强10. 能把Na2SO4、NH4NO3、KCl,(NH4)2SO4四瓶无色溶液加以区别的一种试剂是(必要时可加热)( )A、BaCl2 B、NaOH C、Ba(OH)2 D、AgNO311. 下列电离方程式错误的是( )A、NaHCO3=Na++HCO3﹣ B、NaHSO4═Na++H++SO42﹣ C、H2SO4═2H++SO42﹣ D、KClO3═K++Cl﹣+3O2﹣12. 已知aAm+与bBn﹣具有相同的核外电子排布,则下列关系正确的是( )A、a=b+m+n B、a=b﹣m+n C、a=b+m﹣n D、a=b﹣m﹣n13. 设NA表示阿伏加德罗常数,下列叙述中正确的是( )A、常温常压下,11.2L氧气所含的原子数为NA B、1.8g的NH4+离子中含有的电子数为10NA C、常温常压下,48g O3含有的氧原子数为3NA D、2.4 g金属镁变为镁离子时失去的电子数为0.1NA14. 下列溶液中Cl﹣浓度最大的是( )A、200mL 2 mol•L﹣1 MgCl2溶液 B、1000mL 2.5 mol•L﹣1 NaCl溶液 C、300mL 5 mol•L﹣1 KCl溶液 D、250mL 1 mol•L﹣1 AlCl3溶液15. 实现下列变化,一定要加入其它物质作氧化剂的是( )A、Zn→ZnCl2 B、Cl2→HClO C、CaCO3→CO2 D、CuO→CuSO416. 实验室欲用Na2CO3﹒10H2O晶体配制1mol/L的Na2CO3溶液100mL,下列说法正确的是( )A、要完成实验需称取10.6gNa2CO3﹒10H2O晶体 B、本实验需用到的仪器是天平、药匙、玻璃棒、烧杯、100mL容量瓶 C、配制时若容量瓶不干燥,含有少量蒸馏水会导致浓度偏低 D、定容时俯视刻度线会导致浓度偏高17. 在反应3Cl2+8NH3=6NH4Cl+N2中,发生氧化与还原反应的分子个数比是( )A、2:3 B、3:2 C、3:8 D、8:318. 同温同压下,某容器充满O2时的质量为116g,充满CO2时的质量为122g,若充满某气体时的质量为114g,则该气体的相对分子质量为( )A、44 B、36 C、32 D、2819. 含MgCl2、KCl、Na2SO4三种溶质的混合液中,已知其中含Cl﹣1.5mol,K+和Na+共1.5mol,Mg2+为0.5mol,则SO42﹣的物质的量为( )A、1 mol B、0.5 mol C、0.25 mol D、0.15 mol20. 为了除去KCl中少量的MgSO4和CaCl2杂质,需要进行下列七项操作,其正确操作的先后顺序是( )
B、质子数为6,中子数为8的原子为:14C
C、H,D,T互为同位素
D、液态的氯气称为氯水
6. 下列类型的反应,一定发生电子转移的是( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应7. 下列关于胶体的叙述不正确的是( )A、胶体区别于其他分散系的本质特征是分散质的微粒直径在10﹣9~10﹣7m之间 B、光线透过胶体时,胶体中可发生丁达尔效应 C、用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同 D、Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的8. 关于萃取的理解,下列说法正确的是( )A、可以用四氯化碳把溴水中的溴萃取出来,静置分层后,上层呈橙红色 B、可以用酒精萃取碘水中的碘 C、可以用水做萃取剂把碘从四氯化碳溶液中分离出来 D、萃取之后一般通过分液的方法将互不相溶的液体分离9. 下列关于氯气和氯水的说法中正确的是( )A、氯气是一种无色、密度比空气大的有毒气体 B、红热的铁丝在Cl2中剧烈燃烧生成FeCl2 C、新制氯水能杀菌消毒是因为Cl2有毒,能毒杀细菌 D、氯水放置数天后酸性增强10. 能把Na2SO4、NH4NO3、KCl,(NH4)2SO4四瓶无色溶液加以区别的一种试剂是(必要时可加热)( )A、BaCl2 B、NaOH C、Ba(OH)2 D、AgNO311. 下列电离方程式错误的是( )A、NaHCO3=Na++HCO3﹣ B、NaHSO4═Na++H++SO42﹣ C、H2SO4═2H++SO42﹣ D、KClO3═K++Cl﹣+3O2﹣12. 已知aAm+与bBn﹣具有相同的核外电子排布,则下列关系正确的是( )A、a=b+m+n B、a=b﹣m+n C、a=b+m﹣n D、a=b﹣m﹣n13. 设NA表示阿伏加德罗常数,下列叙述中正确的是( )A、常温常压下,11.2L氧气所含的原子数为NA B、1.8g的NH4+离子中含有的电子数为10NA C、常温常压下,48g O3含有的氧原子数为3NA D、2.4 g金属镁变为镁离子时失去的电子数为0.1NA14. 下列溶液中Cl﹣浓度最大的是( )A、200mL 2 mol•L﹣1 MgCl2溶液 B、1000mL 2.5 mol•L﹣1 NaCl溶液 C、300mL 5 mol•L﹣1 KCl溶液 D、250mL 1 mol•L﹣1 AlCl3溶液15. 实现下列变化,一定要加入其它物质作氧化剂的是( )A、Zn→ZnCl2 B、Cl2→HClO C、CaCO3→CO2 D、CuO→CuSO416. 实验室欲用Na2CO3﹒10H2O晶体配制1mol/L的Na2CO3溶液100mL,下列说法正确的是( )A、要完成实验需称取10.6gNa2CO3﹒10H2O晶体 B、本实验需用到的仪器是天平、药匙、玻璃棒、烧杯、100mL容量瓶 C、配制时若容量瓶不干燥,含有少量蒸馏水会导致浓度偏低 D、定容时俯视刻度线会导致浓度偏高17. 在反应3Cl2+8NH3=6NH4Cl+N2中,发生氧化与还原反应的分子个数比是( )A、2:3 B、3:2 C、3:8 D、8:318. 同温同压下,某容器充满O2时的质量为116g,充满CO2时的质量为122g,若充满某气体时的质量为114g,则该气体的相对分子质量为( )A、44 B、36 C、32 D、2819. 含MgCl2、KCl、Na2SO4三种溶质的混合液中,已知其中含Cl﹣1.5mol,K+和Na+共1.5mol,Mg2+为0.5mol,则SO42﹣的物质的量为( )A、1 mol B、0.5 mol C、0.25 mol D、0.15 mol20. 为了除去KCl中少量的MgSO4和CaCl2杂质,需要进行下列七项操作,其正确操作的先后顺序是( )①加水溶解 ②加热蒸发得到晶体 ③加入过量的BaCl2
④加入过量的盐酸 ⑤加入过量的碳酸钾 ⑥过滤 ⑦加入过量的KOH溶液.
A、①③⑤⑦⑥④② B、①⑤③④⑦⑥② C、①③④⑥⑤②⑦ D、①④③⑤⑥⑦②二、填空题
-
21.(1)、下列物质中,能导电的是 ,(2)、属于电解质的是 ,(3)、属于非电解质的是 . (填序号)
①饱和食盐水 ②液态HCl ③液态汞 ④固体BaSO4 ⑤液态氨 ⑥熔融KNO3⑦干冰 ⑧蔗糖 ⑨干燥的空气.
22. 相等质量的CO和CH4相比较,请完成下列问题.(1)、它们所含的分子数目之比为(2)、同温同压时密度之比为(3)、同温同体积时的压强之比为(4)、同温同压时体积之比为 .23. 用双线桥表示下列反应的电子转移方向和数目,并回答下列问题:3I2+6NaOH=5NaI+NaIO3+3H2O(1)、是氧化剂,是还原剂,氧化产物是;(2)、氧化剂与还原剂的物质的量之比为 , 当反应消耗3mol NaOH时,转移的电子数目为 .24. 在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气.进行此实验,所用仪器如图: (1)、连接上述仪器的正确顺序是:E接 , 接 , 接 , 接F.(2)、气体发生装置中进行的反应化学方程式是;当0.5mol MnO2参与反应时,被氧化的HCl的质量为 , 生成的Cl2在标准状况下的体积约为 .(3)、在装置中:①饱和食盐水的作用是 , ②浓硫酸的作用是 .(4)、化学实验中检验是否有Cl2产生常用湿润的淀粉﹣KI试纸.如果有Cl2产生,可观察到的现象是 , 写出反应方程式 .(5)、写出尾气吸收装置中进行的反应的化学方程式 .
(1)、连接上述仪器的正确顺序是:E接 , 接 , 接 , 接F.(2)、气体发生装置中进行的反应化学方程式是;当0.5mol MnO2参与反应时,被氧化的HCl的质量为 , 生成的Cl2在标准状况下的体积约为 .(3)、在装置中:①饱和食盐水的作用是 , ②浓硫酸的作用是 .(4)、化学实验中检验是否有Cl2产生常用湿润的淀粉﹣KI试纸.如果有Cl2产生,可观察到的现象是 , 写出反应方程式 .(5)、写出尾气吸收装置中进行的反应的化学方程式 .三、计算题
-
25. 标准状况下,22.4LHCl气体溶于50mL水再配成250mL溶液,求:(1)、所得盐酸的物质的量浓度为;(2)、若将此溶液再稀释成1L溶液,则稀释后盐酸的物质的量浓度变为;(3)、将(2)的溶液取出250mL与足量Zn反应可以产生的H2在标准状况下的体积为 .