(浙教版)九年级科学上册专项知识点:金属的化学性质
试卷更新日期:2024-09-27 类型:同步测试
一、选择题
-
1. 电脑芯片的制作需要硅,硅可用石英砂制取,其中涉及的反应有 , 该反应属于( )A、化合反应 B、分解反应 C、置换反应 D、复分解反应2. 下列金属不能与硫酸铜溶液反应,制备出铜单质的是( )A、铁 B、锌 C、镁 D、银3. 为探究Fe、Cu、Ag三种金属的活动性顺序,某兴趣小组设计了如图所示的四组实验方案,其中不能达到实验目的的是( )A、
 B、
B、 C、
C、 D、
D、 4. 在柠檬中插入两种不同的金属可以制得水果电池。相同条件下,水果电池的电压与两种金属的活动性差异大小有关。下列柠檬电池的两种金属,活动性差异最大的是( )A、
4. 在柠檬中插入两种不同的金属可以制得水果电池。相同条件下,水果电池的电压与两种金属的活动性差异大小有关。下列柠檬电池的两种金属,活动性差异最大的是( )A、 B、
B、 C、
C、 D、
D、 5. 光亮的铁钉在下列几种情况下,最不容易生锈的是( )A、
5. 光亮的铁钉在下列几种情况下,最不容易生锈的是( )A、 B、
B、 C、
C、 D、
D、 6. 将质量相等的Mg、Al、Zn三种金属分别放入质量和质量分数均相等的三份稀硫酸中,反应结束后,生成氢气的质量关系不可能的是( )A、
6. 将质量相等的Mg、Al、Zn三种金属分别放入质量和质量分数均相等的三份稀硫酸中,反应结束后,生成氢气的质量关系不可能的是( )A、 B、
B、 C、
C、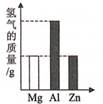 D、
D、 7. 为实现“碳达峰”,世界各国协约节能减排。我国大力推行清洁能源,减少二氧化碳排放,其燃烧的微观过程如图。该反应的基本反应类型属于( )
7. 为实现“碳达峰”,世界各国协约节能减排。我国大力推行清洁能源,减少二氧化碳排放,其燃烧的微观过程如图。该反应的基本反应类型属于( )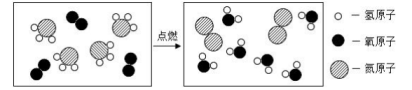 A、化合反应 B、分解反应 C、置换反应 D、复分解反应8. 小科为确定铝(Pd)、铜(Cu)、铂(Pt)三种金属的活动性进行了如图实验,发现铂的表面没有现象,铜的表面有固体覆盖,根据实验现象可知三种金属的活动性顺序是( )
A、化合反应 B、分解反应 C、置换反应 D、复分解反应8. 小科为确定铝(Pd)、铜(Cu)、铂(Pt)三种金属的活动性进行了如图实验,发现铂的表面没有现象,铜的表面有固体覆盖,根据实验现象可知三种金属的活动性顺序是( ) A、 B、 C、 D、9. 将一定量的金属M加入到ZnCl2和CuCl2的混合溶液中,充分反应后过滤,得固体滤渣,滤液为无色,向滤渣中滴加稀硫酸气泡产生,下列有关金属M、Zn、Cu的金属活动性判断一定正确的是( )A、M>Zn B、Zn>M C、M>Cu D、Cu>M10. 把一些锌粉放入Fe(NO3)2和AgNO3的混合溶液中,完全反应后过滤,向滤渣中加入稀盐酸有气体产生,根据以上现象,得出正确结论是( )A、滤渣中一定有Zn、Fe、Ag B、滤渣中一定有Fe、Ag,可能有Zn C、滤渣中一定有Zn、Fe,可能有Ag D、滤渣中一定有Ag,可能有Zn、Fe11. 小科用细线将两根大小相同的铁钉,分别固定在如图所示的液面高度相同的甲、乙密闭装置中,放置几天后观察两个装置中铁钉的锈蚀程度及液面变化,下列表述中正确的是( )
A、 B、 C、 D、9. 将一定量的金属M加入到ZnCl2和CuCl2的混合溶液中,充分反应后过滤,得固体滤渣,滤液为无色,向滤渣中滴加稀硫酸气泡产生,下列有关金属M、Zn、Cu的金属活动性判断一定正确的是( )A、M>Zn B、Zn>M C、M>Cu D、Cu>M10. 把一些锌粉放入Fe(NO3)2和AgNO3的混合溶液中,完全反应后过滤,向滤渣中加入稀盐酸有气体产生,根据以上现象,得出正确结论是( )A、滤渣中一定有Zn、Fe、Ag B、滤渣中一定有Fe、Ag,可能有Zn C、滤渣中一定有Zn、Fe,可能有Ag D、滤渣中一定有Ag,可能有Zn、Fe11. 小科用细线将两根大小相同的铁钉,分别固定在如图所示的液面高度相同的甲、乙密闭装置中,放置几天后观察两个装置中铁钉的锈蚀程度及液面变化,下列表述中正确的是( ) A、甲装置中铁钉的锈蚀程度更明显 B、乙装置中铁钉的锈蚀程度更明显 C、甲装置中铁钉这一侧的液面下降 D、乙装置中铁钉这一侧的液面下降12. 现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法正确的是( )
A、甲装置中铁钉的锈蚀程度更明显 B、乙装置中铁钉的锈蚀程度更明显 C、甲装置中铁钉这一侧的液面下降 D、乙装置中铁钉这一侧的液面下降12. 现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法正确的是( )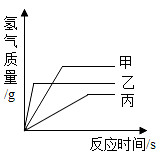 A、甲、乙、丙依次可能是Mg、Zn、Fe B、金属活动性:甲>乙>丙 C、相对原子质量:乙>丙>甲 D、消耗硫酸的质量:甲>乙>丙13. 将质量均为10克的Mg、Fe、Zn三种金属分别放入质量和溶质质量分数均相同的三份稀硫酸中,反应完成后有2种金属剩余,则它们生成氢气的质量关系是( )A、
A、甲、乙、丙依次可能是Mg、Zn、Fe B、金属活动性:甲>乙>丙 C、相对原子质量:乙>丙>甲 D、消耗硫酸的质量:甲>乙>丙13. 将质量均为10克的Mg、Fe、Zn三种金属分别放入质量和溶质质量分数均相同的三份稀硫酸中,反应完成后有2种金属剩余,则它们生成氢气的质量关系是( )A、 B、
B、 C、
C、 D、
D、 14. 某金属加工厂生产过程中的废液含有少量的硝酸银和硝酸铜,为回收利用资源和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤渣中加入少量的稀盐酸,无气泡产生,则下列有关说法中正确的是( )A、滤出的固体中一定含有银,滤液可能含有硝酸亚铁 B、滤出的固体中一定含有银和铜,一定不含有铁 C、滤液中一定含有硝酸亚铁,一定没有硝酸银 D、滤出的固体中一定含有银,滤液中一定含有硝酸亚铁15. 在密闭容器中,分别用压强和温度传感器测定未经打磨的铝片与稀盐酸反应过程的图像如下。下列结论不正确的是( )
14. 某金属加工厂生产过程中的废液含有少量的硝酸银和硝酸铜,为回收利用资源和防止污染,该厂向废液中加入一定量的铁粉,反应停止后过滤,向滤渣中加入少量的稀盐酸,无气泡产生,则下列有关说法中正确的是( )A、滤出的固体中一定含有银,滤液可能含有硝酸亚铁 B、滤出的固体中一定含有银和铜,一定不含有铁 C、滤液中一定含有硝酸亚铁,一定没有硝酸银 D、滤出的固体中一定含有银,滤液中一定含有硝酸亚铁15. 在密闭容器中,分别用压强和温度传感器测定未经打磨的铝片与稀盐酸反应过程的图像如下。下列结论不正确的是( ) A、反应过程中有热量放出 B、0~50s时,变化不明显,是因为铝表面有一层致密氧化铝薄膜 C、60~100s气体压强升高,是因为温度升高的原因 D、100s后温度降低是因为反应停止的原因16. 现有两个烧杯,分别装有质量分数均为10%的AgNO3溶液和Cu(NO3)2溶液各200克,现分别向两烧杯的溶液中缓慢加入足量的铁粉,则两个烧杯内所得金属固体的质量随加入铁粉质量的关系图中,正确的是( )A、
A、反应过程中有热量放出 B、0~50s时,变化不明显,是因为铝表面有一层致密氧化铝薄膜 C、60~100s气体压强升高,是因为温度升高的原因 D、100s后温度降低是因为反应停止的原因16. 现有两个烧杯,分别装有质量分数均为10%的AgNO3溶液和Cu(NO3)2溶液各200克,现分别向两烧杯的溶液中缓慢加入足量的铁粉,则两个烧杯内所得金属固体的质量随加入铁粉质量的关系图中,正确的是( )A、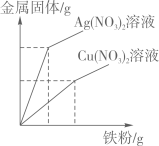 B、
B、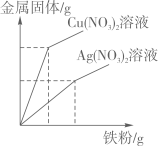 C、
C、 D、
D、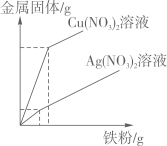 17. 为比较金属活动性顺序,用砂纸将大小相同的锌片、铜片和镁条表面的氧化物除掉,然后分别投入盛有相同质量分数的 5mL稀盐酸的三支试管中 (如图) 。下列有关说法正确的是( )
17. 为比较金属活动性顺序,用砂纸将大小相同的锌片、铜片和镁条表面的氧化物除掉,然后分别投入盛有相同质量分数的 5mL稀盐酸的三支试管中 (如图) 。下列有关说法正确的是( )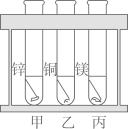 A、除去表面氧化膜后,三种金属均呈银白色 B、注入5mL同种稀盐酸,目的是产生一样多的气体 C、镁表面产生气泡最快,说明镁的金属活动性最强 D、反应结束后,甲、丙两试管中溶液的质量变小
A、除去表面氧化膜后,三种金属均呈银白色 B、注入5mL同种稀盐酸,目的是产生一样多的气体 C、镁表面产生气泡最快,说明镁的金属活动性最强 D、反应结束后,甲、丙两试管中溶液的质量变小二、填空题
-
18. 金属及金属材料在生产、生活中有广泛的应用。(1)、钢铁是制造船舶的主要材料,钢铁与纯铁相比,其硬度更(填“大"或"小”)。(2)、铝的金属活动性较强,但在空气中却耐锈蚀,原因是。(3)、铁制品若保管不善,很容易生锈,请说出一种铁制品的防锈措施:。(4)、在家庭电路中使用的是铜芯线,这是主要利用了铜的性。19. 小明用普通铁钉,纯铁钉同时进行如图的四组实验,一段时间后只有实验A中观察到了锈斑,其他均无明显变化。
 (1)、对比实验,说明铁制品锈蚀需要水;对比A和D实验,说明铁制品锈蚀与因素有关;(2)、根据上述实验结论,下列措施中能有效防止金属锈蚀的是
(1)、对比实验,说明铁制品锈蚀需要水;对比A和D实验,说明铁制品锈蚀与因素有关;(2)、根据上述实验结论,下列措施中能有效防止金属锈蚀的是①金属表面涂抹油漆 ②改变金属的内部结构 ③用湿布擦拭,保持金属表面清洁④在金属表面进行电镀⑤使金属表面形成致密的氧化物薄膜
20. 被誉为“中国天眼”的FAST,是目前世界上最大口径、最灵敏的射电望远镜。请回答下列问题。 (1)、角钢中含有锰(Mn)和硅,锰可以与稀盐酸发生置换反应,生成锰的化合物中锰元素显+2价。请写出其反应的化学方程式。(2)、为探究Fe、Cu、Mn三种金属的活动性,进行了如图2所示的实验:观察到试管③中有明显的现象,判断三种金属的活动性由强到弱的顺序为。21. 钻(Co)的化学性质与铁相似,但钻在常温下对水和空气都比较稳定。(1)、如图是含钴物质的化合价——物质类价图。其中物质a的化学式是。
(1)、角钢中含有锰(Mn)和硅,锰可以与稀盐酸发生置换反应,生成锰的化合物中锰元素显+2价。请写出其反应的化学方程式。(2)、为探究Fe、Cu、Mn三种金属的活动性,进行了如图2所示的实验:观察到试管③中有明显的现象,判断三种金属的活动性由强到弱的顺序为。21. 钻(Co)的化学性质与铁相似,但钻在常温下对水和空气都比较稳定。(1)、如图是含钴物质的化合价——物质类价图。其中物质a的化学式是。 (2)、下列预测钴的化学性质合理的是____。A、Co能在O2中燃烧 B、常温时钴易与H2O反应 C、Co能与稀H2SO4反应 D、CoCl3溶液中的杂质MgCl2可加入钻粉除去22. 金属及金属材料在生产、生活中有广泛的应用。(1)、下列金属制品中,利用金属导热性的是____(填字母)。A、金属硬币 B、铝制导线 C、铜制火锅(2)、近年来,我国高铁飞速发展,已成为世界上唯一高铁成网运行的国家。建造高铁使用了大量铁合金,构成金属铁的粒子是(填“分子”“原子”或“离子”)。(3)、铝合金中主要含铝、铜、镁三种金属,为验证这三种金属的活动性顺序,某同学设计了以下3个实验:甲实验能得出的结论是铝的金属活动性更强,小明同学认为乙、丙实验对验证这三种金属活动性没有作用,可以省去,你的看法是____(填字母)。
(2)、下列预测钴的化学性质合理的是____。A、Co能在O2中燃烧 B、常温时钴易与H2O反应 C、Co能与稀H2SO4反应 D、CoCl3溶液中的杂质MgCl2可加入钻粉除去22. 金属及金属材料在生产、生活中有广泛的应用。(1)、下列金属制品中,利用金属导热性的是____(填字母)。A、金属硬币 B、铝制导线 C、铜制火锅(2)、近年来,我国高铁飞速发展,已成为世界上唯一高铁成网运行的国家。建造高铁使用了大量铁合金,构成金属铁的粒子是(填“分子”“原子”或“离子”)。(3)、铝合金中主要含铝、铜、镁三种金属,为验证这三种金属的活动性顺序,某同学设计了以下3个实验:甲实验能得出的结论是铝的金属活动性更强,小明同学认为乙、丙实验对验证这三种金属活动性没有作用,可以省去,你的看法是____(填字母)。 A、乙、丙都可以省去 B、乙、丙都不能省去 C、丙可以省去,乙不能省 D、乙可以省去,丙不能省(4)、如图横坐标表示反应时间,纵坐标表示的质量:能代表等质量的Mg、Zn、Fe分别与足量的盐酸反应的图象是____。A、
A、乙、丙都可以省去 B、乙、丙都不能省去 C、丙可以省去,乙不能省 D、乙可以省去,丙不能省(4)、如图横坐标表示反应时间,纵坐标表示的质量:能代表等质量的Mg、Zn、Fe分别与足量的盐酸反应的图象是____。A、 B、
B、 C、
C、 D、
D、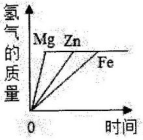 23. 某品牌电器的废旧电路板中含有Fe、Cu、Ag、Ni等金属,如图是某车间回收部分金属的工艺流程,已知: 2Cu+O2+2H2SO4=2CuSO4+2H2O.
23. 某品牌电器的废旧电路板中含有Fe、Cu、Ag、Ni等金属,如图是某车间回收部分金属的工艺流程,已知: 2Cu+O2+2H2SO4=2CuSO4+2H2O. (1)、操作A的名称是。(2)、根据以上工艺流程图,可以判断Ni和Fe比较,金属活动性较强的是 。(3)、固体M中主要含有铜,还含有一定量的铁,为了进一步提纯铜,可以向固体M中加入。
(1)、操作A的名称是。(2)、根据以上工艺流程图,可以判断Ni和Fe比较,金属活动性较强的是 。(3)、固体M中主要含有铜,还含有一定量的铁,为了进一步提纯铜,可以向固体M中加入。三、实验探究题
-
24. 小嘉发现学校草地周围都做上新的铁栅栏,师傅们在上面涂油漆。铁栅栏上为什么要涂油漆呢? 某兴趣小组为此进行研究:

【方案】取四支试管编号为①、②、③、④,分别作如图处理,两周后,观察铁钉表面的锈蚀情况。
【分析】
(1)、设置①③两支试管对照,基于的猜想是。(2)、若两周后观察到①中铁钉生锈而④中铁钉未生锈,据此可得出:导致铁钉生锈的因素为。(3)、若得出食盐会加速金属锈蚀,则实验中支持该结论的证据是。【解释】根据以上实验,请解释学校铁栅栏涂漆能防锈的原因是:。
25. 如图所示为探究铁生锈条件的装置图(图中铁丝绒的固定装置未画出)。 (1)、据图可知,探究的是铁生锈是否需要。(2)、实验开始一段时间后,可观察到U形管中两侧液面高低情况是。(3)、为进一步探究温度对铁生锈快慢的影响。将该装置(每组装置内铁丝绒质量均相等且足量)分别置于不同温度下进行实验,4小时后记录每组U形管两端液面高度差,具体数据如表:
(1)、据图可知,探究的是铁生锈是否需要。(2)、实验开始一段时间后,可观察到U形管中两侧液面高低情况是。(3)、为进一步探究温度对铁生锈快慢的影响。将该装置(每组装置内铁丝绒质量均相等且足量)分别置于不同温度下进行实验,4小时后记录每组U形管两端液面高度差,具体数据如表:温度/摄氏度
10℃
20℃
30℃
40℃
50℃
60℃
70℃
U形管两端液面高度差/厘米
2
4
6
7
8
8
8
分析数据发现,在10-50℃范围内,温度越高,铁生锈越快。但50℃以后U形管两端液面高度差不变,请分析出现该现象的原因是。
四、解答题
-
26. 人类的生产生活离不开金属。某兴趣小组为了测定铜钱(铜锌合金)中铜的质量分数,取多枚铜钱放入烧杯中,另取80克稀硫酸,分四次等质量加入,每次均充分反应,实验数据记录如下表。
实验次数
1
2
3
4
稀硫酸的用量/克
20
20
20
20
剩余固体的质量/克
20.0
17.4
14.8
13.8
分析上述数据,请回答下列问题:
(1)、第4次实验结束后溶液的pH7(填“>”、“=”或“<”)。(2)、计算铜钱中铜的质量分数(计算结果精确到0.1%)。(3)、计算稀硫酸的溶质质量分数。27. 现有铜与金属镁、锌中的一种组成的混合物,现欲测定其组成。取该混合物粉末8.0g放入烧杯中,将140.0g溶质的质量分数为14.0%的稀硫酸平均分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如图:通过计算,
求:
(1)、该混合物粉末中铜的质量分数是(2)、计算确定混合物中另一种金属成分(写出计算过程)(3)、加入稀硫酸充分反应后,所得溶液中溶质的质量分数是多少?(写出计算过程)28. 黄铜是由铜和锌组成的合金,常被用于制造阀门、水管、空调内外机连接管和散热器等。当黄铜的含锌量不同时,其性能不同,见下表。小实同学用足量的稀硫酸对10克某铜锌合金样品进行科学探究,有关数据见下图。含锌量
性能及用途
≤35%
塑性好,适于冷热加压加工
36%~46%
塑性减小而抗拉强度上升,只适于热压力加工
>46%
抗拉强度下降,无使用价值

请回答以下问题:
(1)、图中M的值为克。(2)、AB和BC不在同一直线上的原因是。(3)、求这块合金样品中所含锌的质量分数。