(浙教版)九年级科学上册专项知识点:碱
试卷更新日期:2024-09-27 类型:同步测试
一、选择题
-
1. 下列选项中可以确定某物质属于碱的是( )A、能使酚酞试液变红色 B、能使紫色石蕊试液变蓝色 C、电离时生成的阴离子全部是氢氧根离子 D、能跟酸发生反应生成盐和水2. 下列四个实验中,不能体现碱的通性的是( )A、
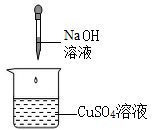
B、
B、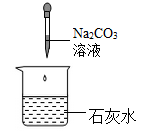
C、
C、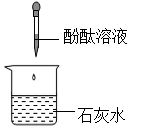
D、
D、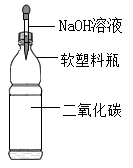
3. 下表为人体内部分体液的正常pH范围,其中碱性最强的是( )
3. 下表为人体内部分体液的正常pH范围,其中碱性最强的是( )液体
血浆
胰液
胃液
胆汁
pH
7.35~7.45
7.5~8.0
0.9~1.5
7.1~7.3
A、血浆 B、胰液 C、胃液 D、胆汁4. 小明发现放置在空气中的氢氧化钠颗粒会很快变成了如图的“浆糊”状态,其主要原因是氢氧化钠固体( ) A、吸热熔化 B、吸水潮解 C、与CO2反应 D、受热分解5. 在一定质量的NaOH溶液中逐滴加入蒸馏水,如图中能正确表示溶液pH变化的是(横坐 标表示加入蒸馏水的质量,纵坐标表示溶液的pH)( )A、
A、吸热熔化 B、吸水潮解 C、与CO2反应 D、受热分解5. 在一定质量的NaOH溶液中逐滴加入蒸馏水,如图中能正确表示溶液pH变化的是(横坐 标表示加入蒸馏水的质量,纵坐标表示溶液的pH)( )A、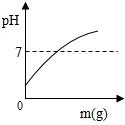 B、
B、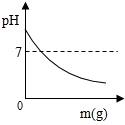 C、
C、 D、
D、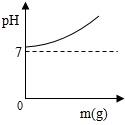 6. 为了维持人体的健康生命活动,人体不同器官内的体液保持不同的酸碱性:
6. 为了维持人体的健康生命活动,人体不同器官内的体液保持不同的酸碱性:体液
尿液
胃液
血液
pH
4.7~8.4
0.9~1.5
7.35~7.45
根据上表可知,在正常情况下( )
A、人体的尿液一定呈酸性 B、人体的血液一定呈碱性 C、人体的胃液能使紫色石蕊试液变蓝色 D、pH试纸可精确测得以上体液的pH7. 在①二氧化碳,②酚酞试液,③稀盐酸,④硫酸铜溶液这四种物质中,能和氢氧化钠作用且表现出了“碱的通性”的组合是( )A、①②③④ B、①②③ C、②③④ D、①③④8. 物质X和Ba(OH)2在溶液中反应的化学方程式为X+Ba(OH)2=BaSO4↓+2Y,下列说法正确的是( )A、X可能为氯化铁 B、X只能为硫酸 C、Y可以为氢氧化铜 D、Y不一定是水9. 有甲、乙、丙三支试管,所装无色溶夜如图所示,已知紫甘蓝菜汁的颜色变化与溶液酸碱性的关系如右表所示。将紫甘蓝菜汁分别滴入三支试管后,试管内溶液颜色将变成( )
溶液
紫甘蓝菜汁颜色
酸性
红色
中性
紫色
碱性
绿色
A、紫色、红色、绿色 B、紫色、绿色、红色 C、紫色、红色、紫色 D、红色、绿色、紫色10. 氢氧化铯是一种可溶性碱,其化学式为CsOH,则下列叙述中正确的是( )A、CsOH溶液能与Fe2O3反应 B、CsOH在水中能电离出Cs+、OH- C、CsOH溶液能使紫色石蕊试液变红 D、CsOH溶液与硫酸反应生成的盐的化学式为CsSO411. 实验探究是获取证据的重要途径。某学习小组阅读资料获知氢氧化钡(Ba(OH)2)与氢氧化钙的化学性质相似,为了验证氢氧化钡的某些化学性质,他们设计如图所示实验。其中不能达到实验目的的是( ) A、实验①验证氢氧化钡溶液显碱性 B、实验②验证氢氧化钡能与酸反应 C、实验③验证氢氧化钡能与某些盐反应 D、实验④验证氢氧化钡能与某些非金属氧化物反应12. 实验小组用传感器研究等量水或NaOH溶液分别吸收CO2的效果,实验装置及测定结果如图所示。下列说法不正确的是( )
A、实验①验证氢氧化钡溶液显碱性 B、实验②验证氢氧化钡能与酸反应 C、实验③验证氢氧化钡能与某些盐反应 D、实验④验证氢氧化钡能与某些非金属氧化物反应12. 实验小组用传感器研究等量水或NaOH溶液分别吸收CO2的效果,实验装置及测定结果如图所示。下列说法不正确的是( )
 A、曲线①是CO2溶解和CO2与水反应的综合结果 B、对比曲线①和②,可说明CO2能与NaOH反应 C、NaOH溶液吸收CO2的效果比水好 D、若选用等量饱和石灰水进行实验,其曲线在①上方13. 我们可以通过建立图像来表示化学反应过程中的量的相互关系。现一烧杯中含有HCl和CuCl2的混合液,将一定质量分数的氢氧化钠溶液加入到混合液中直至过量(CuCl2溶液看成中性),则反应中各个量的图像正确的是( )
A、曲线①是CO2溶解和CO2与水反应的综合结果 B、对比曲线①和②,可说明CO2能与NaOH反应 C、NaOH溶液吸收CO2的效果比水好 D、若选用等量饱和石灰水进行实验,其曲线在①上方13. 我们可以通过建立图像来表示化学反应过程中的量的相互关系。现一烧杯中含有HCl和CuCl2的混合液,将一定质量分数的氢氧化钠溶液加入到混合液中直至过量(CuCl2溶液看成中性),则反应中各个量的图像正确的是( ) A、甲、乙、丙 B、甲、乙 C、乙、丙 D、甲、丙14. 稀HCl和NaOH溶液混合后无明显现象,要证明两者已发生化学反应,下列操作及实验现象(或结果),不能证明反应发生的是( )
A、甲、乙、丙 B、甲、乙 C、乙、丙 D、甲、丙14. 稀HCl和NaOH溶液混合后无明显现象,要证明两者已发生化学反应,下列操作及实验现象(或结果),不能证明反应发生的是( ) A、在混合液中加金属Zn,无气泡产生 B、在混合液中加无色酚酞,溶液呈无色 C、在混合液中加AgNO3溶液,有白色沉淀 D、用pH试纸测混合液的pH,测得pH等于715. 一定温度下,向agFeCl3溶液中加入NaOH固体,溶液的质量与加入NaOH固体的质量变化关系如图所示。下列叙述正确的是( )
A、在混合液中加金属Zn,无气泡产生 B、在混合液中加无色酚酞,溶液呈无色 C、在混合液中加AgNO3溶液,有白色沉淀 D、用pH试纸测混合液的pH,测得pH等于715. 一定温度下,向agFeCl3溶液中加入NaOH固体,溶液的质量与加入NaOH固体的质量变化关系如图所示。下列叙述正确的是( ) A、m-n=c-b B、MP段发生的反应为:FeCl3+3NaOH=3NaCl+Fe(OH)3↓ C、P点对应的溶液中溶质的种类有三种 D、生成Fe(OH)3的质量为(n-c+a)g
A、m-n=c-b B、MP段发生的反应为:FeCl3+3NaOH=3NaCl+Fe(OH)3↓ C、P点对应的溶液中溶质的种类有三种 D、生成Fe(OH)3的质量为(n-c+a)g二、填空题
-
16. 小明在学习Ca(OH)2化学性质时,归纳出了Ca(OH)2与其他物质间相互反应的关系如图(图中“一”表示相连的两种物质能发生反应)。
 (1)、若X是与其他三种不同类别的化合物,则X可能是。(2)、根据图示物质间的关系,写出2的化学方程式:。17. 如图为酸、碱化学性质的知识网络,A、B、C、D是四种常见的不同类别的无机化合物,图中短线表示两种物质在一定条件下可以发生化学反应。请据图回答:
(1)、若X是与其他三种不同类别的化合物,则X可能是。(2)、根据图示物质间的关系,写出2的化学方程式:。17. 如图为酸、碱化学性质的知识网络,A、B、C、D是四种常见的不同类别的无机化合物,图中短线表示两种物质在一定条件下可以发生化学反应。请据图回答: (1)、A、B、C三种物质中,能用来鉴别稀硫酸与氢氧化钙溶液的物质有(填字母编号)。(2)、能同时实现反应①和②的物质D的类别是。18. 归纳总结是学习科学的重要方法,小明同学用图甲总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学变化)。
(1)、A、B、C三种物质中,能用来鉴别稀硫酸与氢氧化钙溶液的物质有(填字母编号)。(2)、能同时实现反应①和②的物质D的类别是。18. 归纳总结是学习科学的重要方法,小明同学用图甲总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学变化)。 (1)、为了验证反应①,小明将无色酚酞试液滴入NaOH溶液中,溶液变成色。(2)、依据反应②说明NaOH必须密封保存,否则在空气中会变质,其化学方程式为。(3)、为了验证反应④能够发生,你选择的物质是____(填序号)。A、Na2CO3 B、HCl C、CuSO4 D、NaCl19. 图甲是关于氢氧化钠化学性质的思维导图,请据图回答问题。
(1)、为了验证反应①,小明将无色酚酞试液滴入NaOH溶液中,溶液变成色。(2)、依据反应②说明NaOH必须密封保存,否则在空气中会变质,其化学方程式为。(3)、为了验证反应④能够发生,你选择的物质是____(填序号)。A、Na2CO3 B、HCl C、CuSO4 D、NaCl19. 图甲是关于氢氧化钠化学性质的思维导图,请据图回答问题。 (1)、性质①,将无色酚酞溶液滴入氢氧化钠溶液中,溶液呈色。(2)、性质②,将氢氧化钠溶液滴入稀盐酸中、图2表示该反应过程中溶液pH的变化曲线,n点溶液中的溶质是(填化学式)。(3)、依据性质③,除去硫酸厂在生产过程中产生的二氧化硫气体,化学方程式为。20. 小明研究氢氧化钙化学性质,进行了如下两个实验。
(1)、性质①,将无色酚酞溶液滴入氢氧化钠溶液中,溶液呈色。(2)、性质②,将氢氧化钠溶液滴入稀盐酸中、图2表示该反应过程中溶液pH的变化曲线,n点溶液中的溶质是(填化学式)。(3)、依据性质③,除去硫酸厂在生产过程中产生的二氧化硫气体,化学方程式为。20. 小明研究氢氧化钙化学性质,进行了如下两个实验。
 (1)、实验过程中能观察到有白色沉淀生成的是实验。(填写图中的序号)(2)、图乙表示实验③过程中溶液中离子种类在反应前后的变化,★表示的离子是。(3)、实验结束后,将实验②和③试管中的废液倒入同一个烧杯中,发现沉淀消失,其原因是。
(1)、实验过程中能观察到有白色沉淀生成的是实验。(填写图中的序号)(2)、图乙表示实验③过程中溶液中离子种类在反应前后的变化,★表示的离子是。(3)、实验结束后,将实验②和③试管中的废液倒入同一个烧杯中,发现沉淀消失,其原因是。三、实验探究题
-
21. 小科对已经变质的氢氧化钠固体是否还含有氢氧化钠进行了以下探究。
[作出猜想]猜想一:有氢氧化钠 猜想二:没有氢氧化钠
(查阅资料) BaCl2溶液、NaNO3溶液、Ba(NO3)2溶液均呈中性。
[进行实验]取少量固体置于试管中,加水充分溶解,滴入几滴无色酚酞,观察到溶液变红,小科认为猜想一成立。
[交流与评价]小玲同学认为小科的结论不一定正确, 原因是 。
于是,小玲同学继续进行探究。
[进行实验]
实验操作
实验现象
实验结论
小玲同学在小科所做实验后的溶液中,滴入过量的Ba(NO3)2溶液
猜想一成立
[反思与拓展]
另取少量烧杯中的溶液进行以下实验,也能证明猜想一成立的是。
A、先加足量稀盐酸,再滴加紫色石蕊溶液 B、先加足量BaCl2溶液,静置,取上层清液,再滴加CuCl2溶液 C、先加足量Ca(OH)2溶液,静置,取上层清液,再滴加酚酞溶液 D、先加足量Ba(NO3)2溶液,静置,取上层清液,再滴加酚酞溶液22. 学习了酸雨及酸的性质后,同学们知道了煤(含有C、H、O、S等元素)燃烧产生的二氧化硫是形成酸雨的主要原因之一。同学们在老师指导下制作了“酸雨形成及危害的模型”来研究酸雨形成的原因及危害,并设计了评价表。图1是小科制作的模型。
评价表:
评价指标
优秀
合格
待改进
指标一
密封性好,能除去大部分污染气体
密封性好,能除去小部分污染气体
密封性不好,不能除去污染气体
指标二
能通过实验现象说明煤燃烧产生的气体是SO2
有实验现象,但不能说明煤燃烧产生SO2
没有明显实验现象
指标三
能通过多个实验现象显示酸雨的危害
能通过一个实验现象显示酸雨的危害
不能通过实验现象显示酸雨的危害
(1)、根据评价表,该模型的指标一可被评为优秀。因为该装置可以除去大部分污染气体,原因是氢氧化钠溶液具有 的性质。(2)、该模型的指标二被评为合格的原因是,煤燃烧还能产生 气体,也能使浸有紫色石蕊试液的棉花变红。(3)、该模型的指标三被评为待改进,于是小科设计了图2、图3两种模型。这两种改进模型中,图 的模型能被评为合格。23. 为探究一瓶久置的氢氧化钠固体样品是否全部变质,小柯取少量样品配制成溶液,再取少量溶液分别装入两支试管中,进行了如甲、乙两图所示实验。(注:BaCl2溶液呈中性)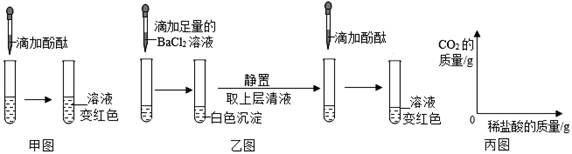 (1)、小柯认为“甲图实验说明了氢氧化钠固体部分变质”。你认为小柯的观点是否正确,并说明理由。(2)、分析乙图实验的现象,可以确定样品的变质情况为。(3)、进一步探究:另取少量样品溶液,加入一定质量分数的稀盐酸,直至过量。请在丙图中画出“生成CO2的质量随加入稀盐酸质量变化”的大致图像。
(1)、小柯认为“甲图实验说明了氢氧化钠固体部分变质”。你认为小柯的观点是否正确,并说明理由。(2)、分析乙图实验的现象,可以确定样品的变质情况为。(3)、进一步探究:另取少量样品溶液,加入一定质量分数的稀盐酸,直至过量。请在丙图中画出“生成CO2的质量随加入稀盐酸质量变化”的大致图像。四、解答题
-
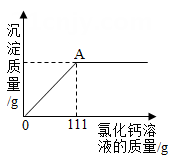
24. 有一份久置于空气中的氢氧化钠固体,通 过以下操作,分析并计算。(1)、取少量该溶液于试管中,向溶液中滴加无色 酚酞试液,试液变红,由此(选填 “能”或“不能”)得出氢氧化钠溶液变质,判断的理由是;(2)、取16g样品完全溶于水中,逐滴加入10% 氯化钙溶液,产生沉淀的质量随氯化钙溶液的质量关系如图。请列式计算A时溶液中氯化钠的溶质质量分数。
 25. 某科学兴趣小组在参加科学拓展课时,进行了以下实验:取硫酸和硫酸铜的混合溶液100克,将200克10%的NaOH溶液分5次加入混合溶液中,得到如下记录表:
25. 某科学兴趣小组在参加科学拓展课时,进行了以下实验:取硫酸和硫酸铜的混合溶液100克,将200克10%的NaOH溶液分5次加入混合溶液中,得到如下记录表:加入NaOH溶液的质量/g
40
80
120
160
200
生产沉淀的总质量/g
0.0
2.45
7.35
9.8
9.8
 (1)、第一次加入NaOH溶液没有产生沉淀的原因是。(2)、第四次加入NaOH溶液后,经充分反应,烧杯中混合溶液的溶质是。(3)、求原混合溶液中硫酸铜的质量分数。(4)、请在坐标图中画出生成沉淀的质量和加入NaOH溶液质量的关系图。
(1)、第一次加入NaOH溶液没有产生沉淀的原因是。(2)、第四次加入NaOH溶液后,经充分反应,烧杯中混合溶液的溶质是。(3)、求原混合溶液中硫酸铜的质量分数。(4)、请在坐标图中画出生成沉淀的质量和加入NaOH溶液质量的关系图。