(浙教版)九年级科学上册专项知识点:酸
试卷更新日期:2024-09-27 类型:同步测试
一、选择题
-
1. 如图所示装置中观察到紫色石蕊变红。物质甲是( )。
 A、浓氨水 B、浓硫酸 C、浓盐酸 D、食盐水2. 盐酸在生产和生活中的用途很广,能与多种物质发生反应。下列物质与盐酸反应时,能观察到白色沉淀的是( )A、
A、浓氨水 B、浓硫酸 C、浓盐酸 D、食盐水2. 盐酸在生产和生活中的用途很广,能与多种物质发生反应。下列物质与盐酸反应时,能观察到白色沉淀的是( )A、 B、
B、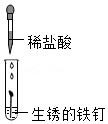 C、
C、 D、
D、 3. 小艺利用酒精提取了几种花的色素,并分别检测它们在不同溶液中的显色情况,记录如表。则其中能用来区分稀硫酸和氯化钠溶液(呈中性)的是( )
3. 小艺利用酒精提取了几种花的色素,并分别检测它们在不同溶液中的显色情况,记录如表。则其中能用来区分稀硫酸和氯化钠溶液(呈中性)的是( )花的种类
不同溶液中的颜色
酸性溶液
中性溶液
碱性溶液
月季花
红色
红色
黄色
菊花
红色
紫色
黄色
丝瓜花
黄色
黄色
黄色
一串红
红色
红色
黄绿色
A、月季花 B、菊花 C、丝瓜花 D、一串红4. 在①氧化铁 ②金属锌 ③氢氧化铜 ④氯化钡溶液四种物质中,跟稀硫酸、稀盐酸都能发生反应且反应中表现了“酸的通性”的组合是( )A、①②③④ B、①②③ C、①③④ D、②③④5. 打开浓盐酸试剂瓶,发现瓶口会有“白雾”出现。已知盐酸中含有水分子、氢离子和氯离子。下列实验能证明“白雾”中含有氢离子的是( ) A、①③ B、②④ C、①②④ D、①③④6. 查阅资料可以知道柠檬酸(C6H8O7)是一种较强的有机酸,在水溶液中可以解离出H+,从而呈现酸性,主要用于制造香料或作为饮料的酸化剂。下列物质不能与柠檬酸反应的是( )A、Mg B、Fe2O3 C、CO2 D、Fe7. 氯气(Cl2)能与水发生如下反应:Cl2+H2O=HCl+HCIO,其中HCIO是一种酸。将Cl2通入过量氢氧化钠溶液中,反应后的生成物有( )A、NaCl、H2O B、NaClO、H2O C、NaCl、NaCIO D、NaCl、NaCIO、H2O8. 取稀盐酸与氢氧化钠反应后的溶液进行实验,下列能说明两者恰好完全反应的是( )A、加氢氧化铜固体生成蓝色溶液 B、加入镁粉,没有气体生成 C、测得该溶液的pH=7 D、滴入酚酞试液,溶液显红色9. 如图是稀硫酸与甲、乙、丙、丁、戊五种常见物质反应出现的不同现象。下列有关说法正确的是( )
A、①③ B、②④ C、①②④ D、①③④6. 查阅资料可以知道柠檬酸(C6H8O7)是一种较强的有机酸,在水溶液中可以解离出H+,从而呈现酸性,主要用于制造香料或作为饮料的酸化剂。下列物质不能与柠檬酸反应的是( )A、Mg B、Fe2O3 C、CO2 D、Fe7. 氯气(Cl2)能与水发生如下反应:Cl2+H2O=HCl+HCIO,其中HCIO是一种酸。将Cl2通入过量氢氧化钠溶液中,反应后的生成物有( )A、NaCl、H2O B、NaClO、H2O C、NaCl、NaCIO D、NaCl、NaCIO、H2O8. 取稀盐酸与氢氧化钠反应后的溶液进行实验,下列能说明两者恰好完全反应的是( )A、加氢氧化铜固体生成蓝色溶液 B、加入镁粉,没有气体生成 C、测得该溶液的pH=7 D、滴入酚酞试液,溶液显红色9. 如图是稀硫酸与甲、乙、丙、丁、戊五种常见物质反应出现的不同现象。下列有关说法正确的是( ) A、甲可能是无色酚酞试液 B、乙、戊一定是金属单质 C、稀硫酸与丙生成的白色沉淀不可能属于盐 D、稀硫酸与丁的反应类型可能是置换反应10. 刘谦在春晚上表演了魔壶,小徐在实验课上也进行了“魔壶”的实验。将“魔壶”中盛有的液体依次倒入两个分别盛有不同溶液的的烧杯中,现象如表,有关说法正确的是( )
A、甲可能是无色酚酞试液 B、乙、戊一定是金属单质 C、稀硫酸与丙生成的白色沉淀不可能属于盐 D、稀硫酸与丁的反应类型可能是置换反应10. 刘谦在春晚上表演了魔壶,小徐在实验课上也进行了“魔壶”的实验。将“魔壶”中盛有的液体依次倒入两个分别盛有不同溶液的的烧杯中,现象如表,有关说法正确的是( )“魔壶”内盛有的液体
烧杯1中形成的“饮料
烧杯2中形成的“饮料
稀硫酸
“牛奶”
“雪碧”
A、此实验用的“魔壶”能用铁制的 B、烧杯1中盛有的溶液一定是 C、烧杯2中得到“雪碧”饮料可能的原因是生成 D、若将“魔壶”中的溶液改为稀硝酸溶液实验现象相同11. 为了研究稀硫酸的性质,教材中设计了如图所示实验。分别将过量的稀硫酸滴入盛有锌粒、氧化铁粉末、氧化铜粉末、氢氧化铜和氯化钡溶液的5支试管中。关于本实验下列说法正确的是( ) A、所有的反应均体现了酸的通性 B、把稀硫酸改成稀盐酸现象都相同 C、氧化铁与硫酸反应生成硫酸亚铁 D、反应后的溶液全部倒进废液缸不再有新的反应12. 如图是稀盐酸和NaOH溶液反应的pH变化曲线图,下列说法正确的是( )
A、所有的反应均体现了酸的通性 B、把稀硫酸改成稀盐酸现象都相同 C、氧化铁与硫酸反应生成硫酸亚铁 D、反应后的溶液全部倒进废液缸不再有新的反应12. 如图是稀盐酸和NaOH溶液反应的pH变化曲线图,下列说法正确的是( ) A、该反应是将NaOH溶液滴入稀盐酸中 B、用湿润的pH试纸测量出A点溶液的pH将偏大 C、该反应的微观实质是H+和OH-结合生成水分子 D、B点时加入溶液的质量和另一种溶液的质量一定相同13. 小科按图示操作进行酸的性质实验,下列有关分析正确的是( )
A、该反应是将NaOH溶液滴入稀盐酸中 B、用湿润的pH试纸测量出A点溶液的pH将偏大 C、该反应的微观实质是H+和OH-结合生成水分子 D、B点时加入溶液的质量和另一种溶液的质量一定相同13. 小科按图示操作进行酸的性质实验,下列有关分析正确的是( ) A、若X是稀硫酸,则a可能是紫色石蕊试液 B、若X是稀硫酸,则d一定是CuO固体 C、若X是稀盐酸,则c一定是单质 D、若b是Fe2O3 , 则黄色溶液一定是氯化铁14. 如图所示,小乐在实验室分别完成①②两个实验后,依次将①②反应后的废液缓慢倒入同一洁净的废液缸,当②的废液倒入时,观察到废液缸中先有气泡产生,然后又出现了白色沉淀。则下列分析错误的是( )
A、若X是稀硫酸,则a可能是紫色石蕊试液 B、若X是稀硫酸,则d一定是CuO固体 C、若X是稀盐酸,则c一定是单质 D、若b是Fe2O3 , 则黄色溶液一定是氯化铁14. 如图所示,小乐在实验室分别完成①②两个实验后,依次将①②反应后的废液缓慢倒入同一洁净的废液缸,当②的废液倒入时,观察到废液缸中先有气泡产生,然后又出现了白色沉淀。则下列分析错误的是( ) A、若向①反应后的废液中滴加紫色石蕊试液,石蕊试液会变红 B、若向②反应后的废液中滴加无色酚酞试液,酚酞试液会变红 C、废液缸中最终的废液里一定含氯离子,一定不含氢离子 D、废液缸中最终的废液里一定含钠离子,一定不含钙离子15. 4mL质量分数为7.3%稀HCl和4mL质量分数为7.3%NaOH溶液混合后无明显现象,要证明两者是否发生了化学反应,下列操作及实验现象(或结果),不能证明反应发生的是( )
A、若向①反应后的废液中滴加紫色石蕊试液,石蕊试液会变红 B、若向②反应后的废液中滴加无色酚酞试液,酚酞试液会变红 C、废液缸中最终的废液里一定含氯离子,一定不含氢离子 D、废液缸中最终的废液里一定含钠离子,一定不含钙离子15. 4mL质量分数为7.3%稀HCl和4mL质量分数为7.3%NaOH溶液混合后无明显现象,要证明两者是否发生了化学反应,下列操作及实验现象(或结果),不能证明反应发生的是( ) A、在混合液中加金属Fe,无气泡产生 B、在混合液中加紫色石蕊试液,溶液呈紫色 C、在混合液中加AgNO3溶液,有白色沉淀 D、用pH试纸测混合液的pH,测得pH等于7
A、在混合液中加金属Fe,无气泡产生 B、在混合液中加紫色石蕊试液,溶液呈紫色 C、在混合液中加AgNO3溶液,有白色沉淀 D、用pH试纸测混合液的pH,测得pH等于7二、填空题
-
16. 对知识的及时整理与归纳是学习科学的重要方法。某同学在学习了硫酸 的化学性质后,初步归纳出稀硫酸与其他物质相互反应的关系,如图所示(“一”表示相连的两种物质能发生反应,五个圈中的物质属于不同的类别)。
 (1)、已知X是金属单质,则X可以是(填一种即可)。(2)、请写出稀硫酸与Y反应的一个化学方程式:。17. 盐酸在实验室有较多的使用,也呈现出不同的性质。(1)、打开浓盐酸时,瓶口出现白雾,说明浓盐酸具有 性;(2)、实验室常用金属锌与稀盐酸来制取氢气,该反应的微观示意图如图甲、乙所示,其中“●”表示的离子是 。
(1)、已知X是金属单质,则X可以是(填一种即可)。(2)、请写出稀硫酸与Y反应的一个化学方程式:。17. 盐酸在实验室有较多的使用,也呈现出不同的性质。(1)、打开浓盐酸时,瓶口出现白雾,说明浓盐酸具有 性;(2)、实验室常用金属锌与稀盐酸来制取氢气,该反应的微观示意图如图甲、乙所示,其中“●”表示的离子是 。 (3)、实验室选用溶质质量分数为22%的盐酸与足量的大理石制取二氧化碳时,产生二氧化碳的快慢与时间关系如图丙所示,在实验过程中发现,发生装置中的锥形瓶外壁发烫。推测图中第5~10分钟时反应快速变慢的主要原因是 。
(3)、实验室选用溶质质量分数为22%的盐酸与足量的大理石制取二氧化碳时,产生二氧化碳的快慢与时间关系如图丙所示,在实验过程中发现,发生装置中的锥形瓶外壁发烫。推测图中第5~10分钟时反应快速变慢的主要原因是 。 18. 小科所在的实验小组进行了如下实验:
18. 小科所在的实验小组进行了如下实验: (1)、写出B中反应的化学方程式:。(2)、D中沉淀的化学式是:。(3)、B、D试管内的物质在E中混合后得到无色溶液,其中一定含有的溶质是: , 可能含有的溶质是:。19. 兴趣小组研究酸碱反应时利用稀硫酸、氢氧化钠溶液、紫色石蕊指示剂进行实验,实验操作和溶液颜色变化如下图所示。
(1)、写出B中反应的化学方程式:。(2)、D中沉淀的化学式是:。(3)、B、D试管内的物质在E中混合后得到无色溶液,其中一定含有的溶质是: , 可能含有的溶质是:。19. 兴趣小组研究酸碱反应时利用稀硫酸、氢氧化钠溶液、紫色石蕊指示剂进行实验,实验操作和溶液颜色变化如下图所示。
 (1)、从微观角度分析,该反应的实质是。(2)、根据乙图颜色的变化,判断图甲中B溶液是。(填写溶液名称)(3)、图乙中M点时,溶液中除紫色石蕊外还存在的溶质有。
(1)、从微观角度分析,该反应的实质是。(2)、根据乙图颜色的变化,判断图甲中B溶液是。(填写溶液名称)(3)、图乙中M点时,溶液中除紫色石蕊外还存在的溶质有。三、实验探究题
-
20. 甲酸是一种无色、有刺激性气味的液体,有较强的腐蚀性。小科想知道甲酸是否具有酸性,做了如下探究:
 (1)、他作出的猜想是“甲酸具有酸性”。你认为下列哪一项实验设计能够检验这一猜想?请用图中字母表示。(2)、若小科的猜想是正确的,则甲酸就会像盐酸那样,能与碳酸钠反应,产生气体。(3)、甲酸(HCOOH)是有机物,浓硫酸能将有机物中的氢元素和氧元素按照水分子中氢原子、氧原子个数比“脱出”生成水;这就是浓硫酸的脱水性。实验室里将甲酸和浓硫酸混合加热进行反应,该反应中甲酸脱水后会生成气体。21. 某化学活动小组以“酸的化学性质”为主题进行探究性实验学习,请根据下图实验回答下列问题:
(1)、他作出的猜想是“甲酸具有酸性”。你认为下列哪一项实验设计能够检验这一猜想?请用图中字母表示。(2)、若小科的猜想是正确的,则甲酸就会像盐酸那样,能与碳酸钠反应,产生气体。(3)、甲酸(HCOOH)是有机物,浓硫酸能将有机物中的氢元素和氧元素按照水分子中氢原子、氧原子个数比“脱出”生成水;这就是浓硫酸的脱水性。实验室里将甲酸和浓硫酸混合加热进行反应,该反应中甲酸脱水后会生成气体。21. 某化学活动小组以“酸的化学性质”为主题进行探究性实验学习,请根据下图实验回答下列问题: (1)、实验中观察到产生气泡是试管;(填“①”“②”、“③”或“④”);(2)、试管③中反应的化学方程式是。(3)、实验中观察到试管⑤中物质变蓝色溶液,X可能是。
(1)、实验中观察到产生气泡是试管;(填“①”“②”、“③”或“④”);(2)、试管③中反应的化学方程式是。(3)、实验中观察到试管⑤中物质变蓝色溶液,X可能是。四、解答题
-
22. 小明买了一瓶钙片,但说明书某些地方模糊不清,于是拿到实验室做了探究:取2片钙片样品研磨后放在烧杯里,加入50g盐酸溶液,两者恰好完全反应(假设钙片中其他成分不与盐酸溶液反应),测得烧杯中剩余物质的总质量(m)与反应时间(t)的关系如图所示。

 (1)、将钙片研磨的目的是。(2)、反应后产生气体的质量 g。(3)、试通过计算求每片钙片中碳酸钙的含量23. 高纯度的MnO2主要用于制造干电池。科学活动小组同学得到某MnO2样品(主要含有杂质MnCO3 , 其它杂质忽略不计)。为了测定此样品中MnO2的含量,把10g MnO2样品放入烧杯中,将40g稀硫酸分4次加入与之充分反应,测得的数据如下表。(已知烧杯中发生的反应为:MnCO3+H2SO4=MnSO4+H2O+CO2↑)
(1)、将钙片研磨的目的是。(2)、反应后产生气体的质量 g。(3)、试通过计算求每片钙片中碳酸钙的含量23. 高纯度的MnO2主要用于制造干电池。科学活动小组同学得到某MnO2样品(主要含有杂质MnCO3 , 其它杂质忽略不计)。为了测定此样品中MnO2的含量,把10g MnO2样品放入烧杯中,将40g稀硫酸分4次加入与之充分反应,测得的数据如下表。(已知烧杯中发生的反应为:MnCO3+H2SO4=MnSO4+H2O+CO2↑)次数
1
2
3
4
加入稀硫酸的质量(g)
10
10
10
10
剩余固体质量(g)
9.425
8.85
8.275
7.82
请根据图表数据回答下列问题:
(1)、样品中MnO2的质量为克。(2)、稀硫酸有剩余的是第次实验。(3)、第⒉次加入稀硫酸反应后,所得溶液中溶质的质量分数为多少?(计算结果精确到0.1%)