四川省达州市渠县六校联考2016年中考化学二模考试试卷
试卷更新日期:2017-12-06 类型:中考模拟
一、选择题
-
1. 用Mg、MgO、Mg(OH)2、MgCO3、HCl五种物质两两进行反应,能得到MgCl2的方法有( )A、3种 B、4种 C、2种 D、无法确定2. 下列关于化学反应“X2十3Y2=2Z”的叙述错误的是( )
A、Z的化学式为XY3 B、若mgX2和ngY2恰好完全反应,则生成(m+n)gZ C、若X2和Y2的相对分子质量分别为M和N,则Z的相对分子质量为(M+N) D、若agX2完全反应生成bgZ,则同时消耗(b﹣a)gY23. 中和一定质量的稀硫酸,需用a克NaOH若改用a克KOH来中和时,则反应后溶液的pH为( )A、等于7 B、大于7 C、小于7 D、无法确定4. 分析推理是学习化学常用的一种方法.下列推理正确的是( )
A、Zn置换H2是有元素化合价变化的置换反应,则所有置换反应都有元素化合价变化 B、酸碱中和反应有盐和H2O生成,则有盐和H2O生成的反应一定是酸碱中和反应 C、一定温度下的不饱和溶液还能溶解溶质,则一定温下的饱和溶液不能溶解任何物质 D、CH4充分燃烧生成的H2O和CO2 , 则充分燃烧生成H2O和CO2的物质只含C、H元素5. 酒精(C2H5OH)的某种水溶液,溶质和溶剂中氢原子个数相等,则该溶液中溶质的质量分数为( )A、23% B、46% C、55% D、72%6. 下列所示图象能正确反映对应的实验或化学反应事实的是( )
A、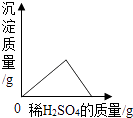 稀H2SO4滴入BaCl2溶液中
B、
稀H2SO4滴入BaCl2溶液中
B、 往部分变质的NaOH溶液中滴加稀盐酸
C、
往部分变质的NaOH溶液中滴加稀盐酸
C、 等质量的Mg、Zn、Fe与足量的等质量分数的稀盐酸反应
D、
等质量的Mg、Zn、Fe与足量的等质量分数的稀盐酸反应
D、 等质量,等质量分数的过氧化氢溶液制取O2
7. 将一定质量的铁粉加到Zn(NO3)2、Cu(NO3)2、AgNO3的混合溶液中,充分反应后过滤,将滤渣放入稀盐酸中,有气泡产生,则下列情况不可能存在的是( )
等质量,等质量分数的过氧化氢溶液制取O2
7. 将一定质量的铁粉加到Zn(NO3)2、Cu(NO3)2、AgNO3的混合溶液中,充分反应后过滤,将滤渣放入稀盐酸中,有气泡产生,则下列情况不可能存在的是( )
A、滤渣是Ag、Cu、Fe B、滤液中有Zn2+、Fe2+、NO3﹣ C、滤渣是Zn、Cu、Ag D、金属活动性顺序为Ag<Cu<Fe<Zn8. 将CaCO3和Cu的混合固体放在敞口容器中,高温下使其完全反应,测得反应前后固体质量不变,则CaCO3与Cu的质量之比为( )
A、14:11 B、14:20 C、25:44 D、25:16二、填空题
-
9. 用化学符号表示:
海水中最多的物质 , 三个铵根离子 , 氧化亚铁 , 氯化镁中镁元素化合价 , 氯化钠溶液中的微粒有 .
10.(1)、已知反应4P+5O2 2P2O5 , 如果有m个P2O5分子生成,则参加反应的氧分子个数为个
(2)、m克氧气与n克碳充分反应后生成CO2质量(m+n)克(填“<”或“=”或“≤”)11. 现有三个化学反应:①S+O2 SO2②2CO+O2 2CO2③4Al+3O2 2Al2O3(1)、比较发现,它们的相似之处有:我也能写出另外一个符合这三点的化学方程式:(2)、某同学课外学习Cu2(OH)2CO3 2CuO+H2O+CO2↑他发现这个反应和上述三个反应也有相似之处,其相似之处是 .12. 如表所示是相应各物质反应前后的质量关系,完成相应各题.物质
O2
CO2
H2O
M
反应前质量/g
100
1
1
46
反应后质量/g
4
89
55
X
则:
(1)、表中X的值为(2)、物质M中一定有的元素为(填元素符号)(3)、若M的相对分子质量为46,请写出M在氧气中燃烧的化学方程式: .13. 如图是A,B两物质的溶解度曲线图,据图可知: (1)、在℃时,A与B的溶解度相同.(2)、20℃时,50g水中加入30gA,所得溶液质量为(3)、若A 物质中混有少量B,用法可提纯A.14. 将150g20%的NaCl溶液稀释成15%的NaCl溶液,需加水mL(水的密度为1g/cm3),在用量筒量取水的体积时,若采用如图所示的方法读数(其他操作都正确),则所配得溶液中溶质的质量分数15%(填“大于”或“小于”或“等于”)
(1)、在℃时,A与B的溶解度相同.(2)、20℃时,50g水中加入30gA,所得溶液质量为(3)、若A 物质中混有少量B,用法可提纯A.14. 将150g20%的NaCl溶液稀释成15%的NaCl溶液,需加水mL(水的密度为1g/cm3),在用量筒量取水的体积时,若采用如图所示的方法读数(其他操作都正确),则所配得溶液中溶质的质量分数15%(填“大于”或“小于”或“等于”) 15. 某同学测得由MgSO4和MgS组成的混合物中氧元素质量分数为37%,则混合物中镁元素质量分数为 .
15. 某同学测得由MgSO4和MgS组成的混合物中氧元素质量分数为37%,则混合物中镁元素质量分数为 .
16. 知A为一种氯化物,B为一种钠盐,C为一种碱,如图表示的是A、B、C的溶液两两间反应的实验现象,根据有关现象完成各题: (1)、写出A,B,C的化学式A , B , C .(2)、写出B与C反应的化学方程式: .(3)、A溶液不能用铁桶盛装的原因是(用化学方程式表示).
(1)、写出A,B,C的化学式A , B , C .(2)、写出B与C反应的化学方程式: .(3)、A溶液不能用铁桶盛装的原因是(用化学方程式表示).三、实验探究题
-
17. 实验是科学探究的重要会途径,请回答以下有关化学实验的问题.(1)、实验室里可用浓盐酸与MnO2在加热条件下反应制取氯气,氯气能溶于水,密度比空气大,则制取和收集氯气的装置分别是和 .
 (2)、某兴趣小组设计的趣味实验装置如图2所示,其中A,B为未膨胀的气球,C为玻璃管,D为胶头滴管,用气密性良好的该装置分别进行甲、乙两组实验,实验量均把胶头滴管中的溶液足量加入锥形瓶中,并轻轻振荡,请填写如表:
(2)、某兴趣小组设计的趣味实验装置如图2所示,其中A,B为未膨胀的气球,C为玻璃管,D为胶头滴管,用气密性良好的该装置分别进行甲、乙两组实验,实验量均把胶头滴管中的溶液足量加入锥形瓶中,并轻轻振荡,请填写如表:锥形瓶中的物质
胶头滴管中
的物质
气球(A,B)的变化
有关反应的化学方程式
甲
CO2
浓NaOH溶液
乙
A气球胀大,
B气球无明显变化
 18. 达州某中学的化学兴趣小组的同学利用如图所示装置测定Fe2O3样品中Fe2O3质量分数,(样品中杂质不反应),回答下列问题.
18. 达州某中学的化学兴趣小组的同学利用如图所示装置测定Fe2O3样品中Fe2O3质量分数,(样品中杂质不反应),回答下列问题.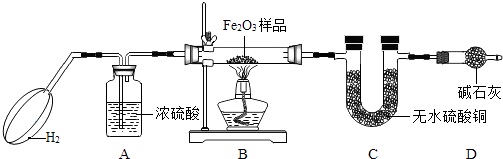 (1)、实验开始时,挤压气球并持续一段时间,其目的是(2)、装置A的作用是 , 装置C中的现象是(3)、反应前准确称得样品Fe2O3质量为5g,完全反应后装置C质量增加了1.35g,则样品中Fe2O3的质量分数为(4)、若省去D装置,则实验测得的样品中Fe2O3质量分数会(填“偏大”或“偏小”或“不变”)
(1)、实验开始时,挤压气球并持续一段时间,其目的是(2)、装置A的作用是 , 装置C中的现象是(3)、反应前准确称得样品Fe2O3质量为5g,完全反应后装置C质量增加了1.35g,则样品中Fe2O3的质量分数为(4)、若省去D装置,则实验测得的样品中Fe2O3质量分数会(填“偏大”或“偏小”或“不变”)四、计算题
-
19. 取12g石灰石(主要成分是CaCO3 , 杂质不溶于水,也不反应)放入烧杯中,向其中加入100g稀盐酸,二者恰好完全反应,反应结束后,烧杯中剩余物质的总质量为107.6g(气体的溶解忽略不计),求所得的溶液中溶质的质量分数.(结果保留一位小数)