人教版化学九年级下册第八单元课题2 金属的化学性质 同步训练
试卷更新日期:2017-12-05 类型:同步测试
一、单选题
-
1. 从化学的角度对下列诗句、成语等进行解释,其中不正确的是( )A、“遥知不是雪,为有暗香来”﹣﹣分子在不停地运动 B、“点石成金”﹣﹣化学反应改变了元素种类 C、“真金不怕火炼”﹣﹣金(Au)的化学性质不活泼 D、“釜底抽薪”(釜:烹煮食物的容器.薪:柴禾)﹣﹣破坏了燃烧的条件2. 下列关于金属的说法中,不正确的是( )A、铜有良好的导电性,常用于制作导线 B、所有的金属都能与稀盐酸反应 C、铁制品在干燥的空气中不易生锈 D、不锈钢具有较强的耐腐蚀性,可用于制作医疗器械3. 关于化学反应类型说法正确的是( )A、有单质生成的反应是分解反应 B、两种化合物之间的反应是复分解反应 C、元素存在形态发生改变的反应是置换反应 D、化合反应中生成物的物质的质量可能等于反应物的物质的质量和4. 关于下列实验现象,描述错误的是( )A、光亮的铜丝放入稀硫酸中,溶液变为蓝色,产生大量气泡 B、镁条在空气中剧烈燃烧,发出耀眼的白光,生成白色固体 C、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 D、氢气在空气中燃烧,产生淡蓝色火焰,放出大量的热5. 英国化学家亨利•卡文迪许是燃素说的信仰者.1766年,他用铁、锌、锡等六种金属与稀硫酸、稀盐酸作用制得“可燃空气”.并将其表示为:

用所学化学知识判断.下列说法正确的是( )
A、“可燃空气”是从金属中分解出来的 B、上述六种金属包括铜 C、“可燃空气”可以用排水集气法收集 D、上述反应属于复分解反应6. 某黑色固体粉末可能是Fe、FeO、CuO和C中的一种或几种.取黑色粉末,加入一定量的稀硫酸,待充分反应后过滤,得到滤液和滤渣,在滤液中插入一根洁净的铁丝.有关说法正确的是( )A、若滤液呈浅绿色,则原黑色固体粉末中一定有Fe B、若铁丝表面只有红色固体析出,则滤渣中一定无CuO C、若铁丝表面无明显现象,则滤渣中最多有四种物质 D、若铁丝表面只有气泡产生,则滤液中溶质一定有H2SO4和FeSO47. 将一定质量的铁粉和氧化铜粉末投入到一定质量的稀硫酸中,充分反应后过滤,得到滤液M和滤渣N,下列有关说法:①滤液M中一定含有硫酸铁,可能含有硫酸和硫酸铜;
②在滤液M中放入一块刚打磨过的锌片,一定有置换反应发生;
③向滤渣N中滴加稀硫酸.可能有气泡产生;
④当滤液M中含有硫酸铜时,滤渣N中一定没有氧化铜
其中一定正确的说法是( )
A、①② B、②③ C、③④ D、①④8. 下列反应属于置换反应的是( )A、2CO+O2 2CO2 B、H2CO3 H2O+CO2↑ C、NaOH+HCl═NaCl+H2O D、2Al+6HCl═2AlCl3+3H2↑9. 下图是自来水消毒过程中发生反应的微观示意图,下列说法正确的是( )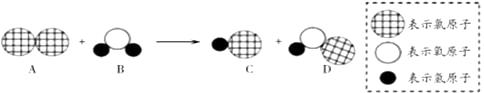 A、该反应属于置换反应 B、参加反应的 A,B 两物质质量比为 1:1 C、该反应中涉及两种氧化物 D、反应前后氯元素的化合价发生了改变10. 在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,充分反应后过滤,滤液仍为蓝色,滤渣中所含物质不可能的情况是( )A、可能有银和铜,没有锌 B、可能只有银,没有铜和锌 C、一定有银,可能有铜和锌 D、一定有银、没有锌,可能有铜11. 有X、Y、Z三种金属,其中Y能与稀硫酸反应产生氢气,而X、Z不能与稀硫酸反应;将Z浸入X的盐溶液中,Z的表面有X析出,则X、Y、Z的金属活动性由强到弱的顺序是( )A、X、Y、Z B、Y、Z、X C、Y、X、Z D、Z、X、Y12. 向盛有氯化亚铁和氯化铜混合溶液的烧杯中加入一定量的锌粉,充分反应后,得到固体M和溶液N.下列叙述错误的是( )A、锌有剩余时,M中一定有Fe、Cu和Zn B、锌有剩余时,N中一定没有FeCl2和CuCl2 C、锌无剩余时,M中一定有Cu、可能有Fe D、锌无剩余时,N中一定有ZnCl2和FeCl213. 向一定量硝酸银和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图所示.下列说法正确的是( )
A、该反应属于置换反应 B、参加反应的 A,B 两物质质量比为 1:1 C、该反应中涉及两种氧化物 D、反应前后氯元素的化合价发生了改变10. 在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,充分反应后过滤,滤液仍为蓝色,滤渣中所含物质不可能的情况是( )A、可能有银和铜,没有锌 B、可能只有银,没有铜和锌 C、一定有银,可能有铜和锌 D、一定有银、没有锌,可能有铜11. 有X、Y、Z三种金属,其中Y能与稀硫酸反应产生氢气,而X、Z不能与稀硫酸反应;将Z浸入X的盐溶液中,Z的表面有X析出,则X、Y、Z的金属活动性由强到弱的顺序是( )A、X、Y、Z B、Y、Z、X C、Y、X、Z D、Z、X、Y12. 向盛有氯化亚铁和氯化铜混合溶液的烧杯中加入一定量的锌粉,充分反应后,得到固体M和溶液N.下列叙述错误的是( )A、锌有剩余时,M中一定有Fe、Cu和Zn B、锌有剩余时,N中一定没有FeCl2和CuCl2 C、锌无剩余时,M中一定有Cu、可能有Fe D、锌无剩余时,N中一定有ZnCl2和FeCl213. 向一定量硝酸银和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图所示.下列说法正确的是( )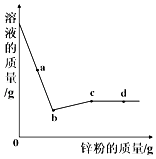 A、a点所得固体为银和铁 B、b点所得溶液中的溶质为硝酸银、硝酸亚铁和硝酸锌 C、c点所得溶液中的溶质为硝酸亚铁和硝酸锌 D、d点所得固体为银、铁和锌14. 图像能正确反映对应变化关系的是( )A、向一定量的MnO2中加入H2O2溶液
A、a点所得固体为银和铁 B、b点所得溶液中的溶质为硝酸银、硝酸亚铁和硝酸锌 C、c点所得溶液中的溶质为硝酸亚铁和硝酸锌 D、d点所得固体为银、铁和锌14. 图像能正确反映对应变化关系的是( )A、向一定量的MnO2中加入H2O2溶液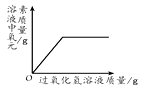 B、向黄铜粉末(锌铜混合物)中加稀盐酸
B、向黄铜粉末(锌铜混合物)中加稀盐酸 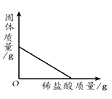 C、红磷在盛有空气的密闭容器中燃烧
C、红磷在盛有空气的密闭容器中燃烧 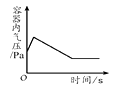 D、加热一定量的氯酸钾和二氧化锰固体混合物
D、加热一定量的氯酸钾和二氧化锰固体混合物 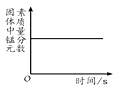
二、填空题
-
15. 在做金属化学性质探究实验时:
①已知金属A和B能够发生如下反应:Zn+ACl2=ZnCl2+A B+ZnCl2=BCl2+Zn判断Zn、A、B三种 金属的活动性由强到弱依次是 .
②某同学不小心把实验后的铁钉和铜丝倒入含有稀硫酸的废液缸中,发现有气泡产生,用化学方程式解释产生气泡的原因 .
16. 铝在空气中能与氧气反应生成一层致密的氧化铝(Al2O3)薄膜,该反应的化学方程式为 , 反应的基本类型是 . 将打磨过的铝丝浸入硫酸铜溶液中,该反应的化学方程式为 .17. 向AgNO3、Cu(NO3)2、Mg(NO3)2混合液中,加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,无气体生成,则滤出的固体中一定含有 , 滤液中一定含有的阳离子是。
18. 将足量的稀盐酸加入一定量的铁、铜混合物中,写出其中反应的化学方程式 . 图7是实验过程生成气体或剩余固体的质量随反应时间的变化关系,其中表示正确的是(填标号). 19. 在实验课中,各小组作了如下实验:
19. 在实验课中,各小组作了如下实验:实验编号
1
2
3
4
实验操作
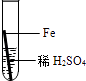
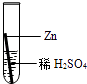
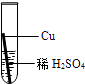
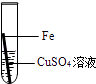
实验后,同学们按老师要求将废液都倒在指定的大烧杯中,小科猜想该烧杯中的废液可能有硫酸铜、硫酸锌、硫酸亚铁…,应该可以从中提炼出铁和铜.经思考后,他设计了如图所示的实验,并设法使滤液甲和乙所含的溶质相同.
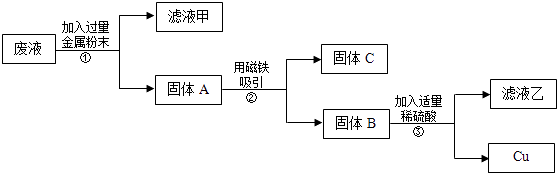
则固体C是 , 操作③的名称是 , 实验中所加的过量金属粉末是 .
三、综合题
-
20. 我国古代的物质文明华夏民族在认识、改造和应用物质方面有着辉煌的历史.
①东晋《抱扑子》中记载:“以曾青涂铁,铁赤色如铜”(“曾青”即硫酸铜溶液).
②战国《周礼》中记载;“煤饼烧砺房成灰”(“砺房”即牡砺壳,主要成分是碳酸钙).将“灰”溶于水可制得沤浸树皮脱胶的碱液.
③元代《庚道集》中记载:“点铜戍银”(即单质锏与砷熔合形成银白色的物质).
请运用你学过的化学知识回答下列问题;
(1)、在①~③中,发生了化学变化的是(填编号)其中发生分解反应的化学方程式为 .(2)、①中发生变化的化学方程式为 , 该反应中发生有效的相互作用而促使变化发生的微粒是(写出微粒符号) .(3)、②中“灰”溶于水的变化中,其能量的转化形式是 .(4)、③中的“银”是否属于合金? .21. A~I为初中化学常见的物质,它们之间的转化关系如图1所示(只略去反应①的部分产物).其中B是紫红色金属,D、F为黑色固体,H是实验室中最常见的无色无味液体.请回答:
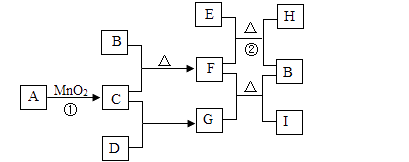 (1)、若A在常温下为液体,则A的化学式为 , 反应①的基本反应类型是 .(2)、在金属活动性顺序中,B位于铁的(填“前面”或“后面”)。(3)、G的化学式为 , 它不具有的性质有(填字母)。
(1)、若A在常温下为液体,则A的化学式为 , 反应①的基本反应类型是 .(2)、在金属活动性顺序中,B位于铁的(填“前面”或“后面”)。(3)、G的化学式为 , 它不具有的性质有(填字母)。A.酸性 B.还原性 C.毒性 D.助燃性
四、实验探究题
-
22. 利用下图装置进行实验(两支玻璃管内径相同).实验前K1、K2、K3均已关闭.
实验装置
【实验1】制备气体
【实验2】测定空气中氧气含量
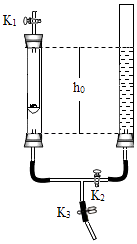
左管中带孔的燃烧匙盛有足量锌粒,右管盛有稀硫酸
Ⅰ.打开K1和K2 , 使反应发生
Ⅱ.在K1的导管口处收集气体
Ⅲ.…
左管中燃烧匙盛有足量白磷,右管盛有水
Ⅰ.光照引燃白磷
Ⅱ.待白磷熄灭,冷却,打开K2 , 至液面不再变化,右管中液体的高度为h1
(1)、实验1:锌与稀硫酸反应的化学方程式为;为使反应停止,Ⅲ中的操作是 .(2)、实验2:打开K2 , 右管中液面下降,原因是;计算空气中氧气体积分数的表达式为(用h0、h1表示).五、计算题
-
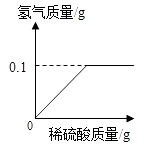
23. 为研究黄铜(铜锌合金)的组成,某学习小组称取该样品10g,向其中逐滴加稀硫酸至刚好不再产生气体为止.生成的气体与所用硫酸溶液的质量关系如图所示,请计算:10g样品中铜的质量是多少克?
-