初中科学浙教版 八年级上册 第一章 第6节 物质的分离同步练习
试卷更新日期:2024-08-14 类型:同步测试
一、单选题
-
1. 自来水厂对水进行净化处理时,最合理的步骤是 ( )A、过滤、沉淀、消毒 B、沉淀、消毒、过滤 C、消毒、沉淀、过滤 D、沉淀、过滤、消毒2. 下列混合物的分离不能达到目的的是( )A、海水淡化得到淡水——蒸馏 B、泥水除去泥沙——过滤 C、分离食盐和糖——加水溶解并过滤 D、海水中提取食盐——蒸发结晶3. 粗盐提纯实验中不需要使用的仪器是( )A、蒸发皿 B、试管 C、酒精灯 D、玻璃棒4. 我国西南地区的旱灾提醒人们应合理使用水资源。下列说法不正确的是( )A、灾区饮用水源应尽量远离人畜生活区 B、水质浑浊时可加入明矾使杂质沉降除去 C、饮用水H2O和消毒剂过氧化氢H2O2都由氢元素和氧元素组成 D、干冰能用于人工降雨的原因是干冰与云发生化学反应生成水5. 用如图。所示的简易净水器处理浑浊的河水,下面分析正确的是( )
 A、该净水器能杀菌消毒 B、净化后的水属于纯净物 C、活性炭的主要作用是吸附 D、该净水器能将硬水变为软水6. 下列关于粗盐提纯实验操作要领,其中错误的是( )A、溶解、过滤和蒸发时都要用到玻璃棒 B、引流的玻璃棒应该靠在三层滤纸的一边 C、漏斗中的滤纸的边缘要低于漏斗的边缘 D、蒸发结晶食盐时,一直要加热到水分完全蒸干7. 从混有少量硝酸钾的食盐晶体中提取较纯的食盐,可供选择的实验步骤有:①在较高的温度下制成该晶体的饱和溶液;②在常温下制成该晶体的饱和溶液;③升高溶液温度不断蒸发水分,直到大量固体析出;④降温至有较多量晶体析出;⑤过滤。正确的操作步骤是( )A、①④⑤ B、①④ C、②③ D、②③⑤8. 向分别盛有40g硝酸钾和40g氯化钠的烧杯里,各加入100g100℃的热水,充分搅拌。根据溶解度表中相关数据分析,下列说法正确的是( )
A、该净水器能杀菌消毒 B、净化后的水属于纯净物 C、活性炭的主要作用是吸附 D、该净水器能将硬水变为软水6. 下列关于粗盐提纯实验操作要领,其中错误的是( )A、溶解、过滤和蒸发时都要用到玻璃棒 B、引流的玻璃棒应该靠在三层滤纸的一边 C、漏斗中的滤纸的边缘要低于漏斗的边缘 D、蒸发结晶食盐时,一直要加热到水分完全蒸干7. 从混有少量硝酸钾的食盐晶体中提取较纯的食盐,可供选择的实验步骤有:①在较高的温度下制成该晶体的饱和溶液;②在常温下制成该晶体的饱和溶液;③升高溶液温度不断蒸发水分,直到大量固体析出;④降温至有较多量晶体析出;⑤过滤。正确的操作步骤是( )A、①④⑤ B、①④ C、②③ D、②③⑤8. 向分别盛有40g硝酸钾和40g氯化钠的烧杯里,各加入100g100℃的热水,充分搅拌。根据溶解度表中相关数据分析,下列说法正确的是( )温度/℃
0
20
40
60
80
100
溶解度/g
氯化钠
35.7
36.0
36.6
37.3
38.4
39.8
硝酸钾
13.3
31.6
63.9
110
169
246
A、均能形成100℃时氯化钠和硝酸钾的饱和溶液 B、将上述2只烧杯内的物质在100℃时各自蒸发掉50g水,有晶体析出的是硝酸钾 C、将上述2只烧杯内的物质降温至20℃时,析出晶体较多的是氯化钠 D、当硝酸钾中含有少量氯化钠时,要从中得到纯净的硝酸钾,可采用降温结晶的方法9. 下列实验操作,错误的是( )A、取用固体药品 B、倾倒液体药品
B、倾倒液体药品  C、过滤泥浆水
C、过滤泥浆水  D、蒸发食盐水
D、蒸发食盐水  10. 下列关于水体净化的说法中,正确的是( )A、在自来水厂的水净化过程中,常需要通入氯气,杀死水中的微生物 B、蒸馏法是物理变化过程,是利用物质的溶解性不同而进行分离 C、沉淀法、过滤法等净化方法都是利用物质的化学性质 D、将自来水进行充分的过滤,就可以得到纯净的水11. 下表为氢氧化钙在不同温度时的溶解度。下列有关说法正确的是( )
10. 下列关于水体净化的说法中,正确的是( )A、在自来水厂的水净化过程中,常需要通入氯气,杀死水中的微生物 B、蒸馏法是物理变化过程,是利用物质的溶解性不同而进行分离 C、沉淀法、过滤法等净化方法都是利用物质的化学性质 D、将自来水进行充分的过滤,就可以得到纯净的水11. 下表为氢氧化钙在不同温度时的溶解度。下列有关说法正确的是( )温度℃
0
10
20
30
40
50
60
70
溶解度/g
0.185
0.176
0.165
0.153
0.141
0.138
0.116
0.106
A、氢氧化钙的溶解度随着温度的升高而增大 B、30℃时,氢氧化钙饱和溶液的溶质质量分数为 C、20℃时,将1g氢氧化钙投入到99g水中,充分反应后,所得溶液的质量为100g D、将40℃时氢氧化钙的饱和溶液降温至20℃,所得溶液的溶质质量分数不变12. 下列混合物的分离方法不正确的是( )A、泥沙和食盐(溶解和过滤) B、水和酒精的混合物(蒸馏) C、硝酸钾中混有少量食盐(降温结晶) D、汽油和水(过滤)13. 科学家用石墨烯膜制成“筛子”,可以筛掉盐类物质。当海水流过该膜时,构成氯化钠的微粒因为被水分子包裹而不能通过,而独立的水分子却能通过(如图QM-3)。下列关于石墨烯膜“筛掉”氯化钠的说法错误的是( ) A、该过程属于物理变化 B、该过程可应用于海水淡化 C、“筛掉”氯化钠的过程类似于过滤操作 D、“筛掉”氯化钠后的海水溶质质量分数增大14. 如图是利用海水提取粗盐的过程,下列说法中正确的是( )
A、该过程属于物理变化 B、该过程可应用于海水淡化 C、“筛掉”氯化钠的过程类似于过滤操作 D、“筛掉”氯化钠后的海水溶质质量分数增大14. 如图是利用海水提取粗盐的过程,下列说法中正确的是( ) A、海水进入贮水池,海水中不含有杂质 B、在蒸发池中,海水中水的质量逐渐减少 C、析出晶体后的母液是氯化钠的不饱和溶液 D、在蒸发池中,海水中的氯化钠质量逐渐增加15. 如图所示为三种实验操作,下列说法正确的是( )
A、海水进入贮水池,海水中不含有杂质 B、在蒸发池中,海水中水的质量逐渐减少 C、析出晶体后的母液是氯化钠的不饱和溶液 D、在蒸发池中,海水中的氯化钠质量逐渐增加15. 如图所示为三种实验操作,下列说法正确的是( ) A、进行如图甲所示的过滤操作,可从食盐溶液中获得食盐固体 B、进行如图乙所示的蒸发操作,当蒸发皿中出现较多固体时停止加热 C、进行如图丙所示的蒸馏操作,冷凝管管进出水的方向是a进b出 D、在粗盐提纯实验中,需要用到图示甲、乙、丙三种操作16. 硝酸钾的溶解度随温度升高而增大。如图是有关硝酸钾溶液的实验操作及变化情况。下列说法正确的是( )
A、进行如图甲所示的过滤操作,可从食盐溶液中获得食盐固体 B、进行如图乙所示的蒸发操作,当蒸发皿中出现较多固体时停止加热 C、进行如图丙所示的蒸馏操作,冷凝管管进出水的方向是a进b出 D、在粗盐提纯实验中,需要用到图示甲、乙、丙三种操作16. 硝酸钾的溶解度随温度升高而增大。如图是有关硝酸钾溶液的实验操作及变化情况。下列说法正确的是( )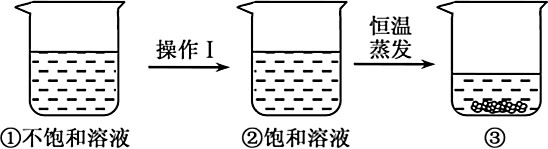 A、操作Ⅰ一定是降温 B、操作Ⅰ一定是加溶质 C、①与③的溶质质量一定相等 D、②与③的溶质质量分数一定相等
A、操作Ⅰ一定是降温 B、操作Ⅰ一定是加溶质 C、①与③的溶质质量一定相等 D、②与③的溶质质量分数一定相等二、填空题
-
17. 小明同学得到了如下关于A、B的两种固体物质的溶解度表:
温度(℃)
0
10
20
30
40
溶解度(g)
A
35
35.5
36
36.5
37
B
6
10
18
36.5
50
(1)、若将B物质从溶液中结晶析出,宜采用的方法是:。(2)、我国有许多盐碱湖,湖中溶有大量的氯化钠和碳酸钠,那里的人们“冬天捞碱,夏天晒盐”。据此你认为表中(填“A”或“B”)物质的溶解度与氯化钠相似。18. 海水淡化可采用膜分离技术。如图一所示,对淡化膜右侧的海水加压,在其左侧得到淡水。其原理是海水中的水分子可以透过淡化膜,而其他各种离子不能透过。请回答: (1)、采用膜分离技术淡化海水的原理,与化学实验中常见的操作相似。(2)、对淡化膜右侧的海水加压后,海水中溶质的质量分数会(选填增大、减小或不变)。(3)、海水中含有大量的氯化钠,图二是氯化钠的溶解度曲线,据此可知盐场从海水中得到食盐晶体利用的方法是结晶(填降温或蒸发)。19. 目前我县里的学校都安装了直饮水机,其工作过程如上图所示。
(1)、采用膜分离技术淡化海水的原理,与化学实验中常见的操作相似。(2)、对淡化膜右侧的海水加压后,海水中溶质的质量分数会(选填增大、减小或不变)。(3)、海水中含有大量的氯化钠,图二是氯化钠的溶解度曲线,据此可知盐场从海水中得到食盐晶体利用的方法是结晶(填降温或蒸发)。19. 目前我县里的学校都安装了直饮水机,其工作过程如上图所示。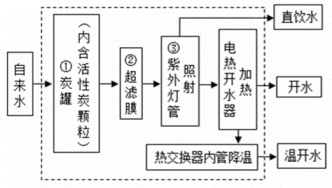 (1)、①的作用是____.A、杀菌消毒 B、吸附杂质 C、蒸馏 D、过滤(2)、直饮水机使用方便:只要将它与自来水管网对接,截留清除水中的有害物质(如细菌等)便得到直饮水,直饮水属于(选填“混合物”或“纯净物”).20. 向50mL水(密度为1g/mL)中溶解一定量固体的操作如下,请你根据如图实验现象和溶解度曲线回答。
(1)、①的作用是____.A、杀菌消毒 B、吸附杂质 C、蒸馏 D、过滤(2)、直饮水机使用方便:只要将它与自来水管网对接,截留清除水中的有害物质(如细菌等)便得到直饮水,直饮水属于(选填“混合物”或“纯净物”).20. 向50mL水(密度为1g/mL)中溶解一定量固体的操作如下,请你根据如图实验现象和溶解度曲线回答。
①A、B、C中一定是饱和溶液的是 , 一定是不饱和溶液的是;(填字母)
②当x=g时,B中恰好没有固体剩余;
③硝酸钾从溶液中析出晶体常用方法.
21. t℃时,将一定量的某物质的溶液分成三等份,分别加热,再降温到t℃。已知从三份溶液中蒸发掉的溶剂质量分别为10g、20g、30g,析出的晶体质量分别为 ag、bg、cg,则a、b、c三者之间的等量关系为。三、实验探究题
-
22. 从自然界中获得的粗盐,含有较多的杂质,需要精制。为了除去粗盐中泥沙等不溶性杂质,设计了如图所示的 A、B、C 三个步骤。
 (1)、B 步骤称为。(2)、B、C 两个步骤中玻璃棒各自的作用分别是和。(3)、C 步骤中, 当蒸发皿内出现较多固体时,应该____(填字母)。A、移去酒精灯,停止搅拌 B、移去酒精灯,用玻璃棒继续搅拌 C、继续加热蒸干水分,再移去酒精灯(4)、提纯含少量泥沙的粗盐,一般经过以下操作流程:
(1)、B 步骤称为。(2)、B、C 两个步骤中玻璃棒各自的作用分别是和。(3)、C 步骤中, 当蒸发皿内出现较多固体时,应该____(填字母)。A、移去酒精灯,停止搅拌 B、移去酒精灯,用玻璃棒继续搅拌 C、继续加热蒸干水分,再移去酒精灯(4)、提纯含少量泥沙的粗盐,一般经过以下操作流程:
操作⑤是图甲中的哪个步骤(填“字母”)。
23. 某学习小组开展了“制作蔗糖”的项目化学习,步骤分成甘蔗擦成渣一压汁一熬制一结晶等。小明在制作过程中取了少量熬制中的蔗糖不饱和溶液来做测试,过程如下:
(1)、要除去压汁后蔗料(即蔗汁和蔗渣的固液混合物)中的蔗渣,可采用的实验操作是。(2)、小明用熬制中的蔗糖不饱和溶液通过的方法配制热的蔗糖饱和溶液。(3)、小明用得到的蔗糖想制作一个棒棒糖,小明将蔗糖加入热水中,用筷子稍作搅拌,观察到杯底还留有蔗糖固体,接着就进行过滤等后续操作,5天后却没有制得棒棒糖,杯中也没有晶体析出。棒棒糖制作失败的原因:最初配制的蔗糖溶液是溶液(选填“饱和”或“不饱和”)。(4)、小明总结了失败的原因后,进行了更改如图所示,为了加快制作棒棒糖的速度,让烧杯中的蔗糖快速析出,他是如何操作。____(可多选) A、烧杯内加入适量冰块 B、烧杯中加入适量氢氧化钠固体 C、烧杯内加入适量食盐 D、烧杯内加入适量硝酸铵固体24. 某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,用所得的精盐配制50g5%的氯化钠溶液。
A、烧杯内加入适量冰块 B、烧杯中加入适量氢氧化钠固体 C、烧杯内加入适量食盐 D、烧杯内加入适量硝酸铵固体24. 某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,用所得的精盐配制50g5%的氯化钠溶液。实验一:下图是同学们做粗盐提纯实验的操作示意图。请回答下列问题:
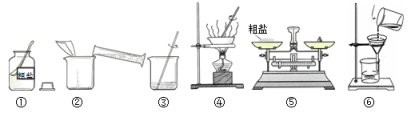 (1)、
(1)、实验一:下图是同学们做粗盐提纯实验的操作示意图。请回答下列问题:
操作③中用玻璃棒搅拌的作用是; (2)、粗盐提纯的操作顺序为(填操作序号)、称量精盐并计算产率。(3)、操作④中,当观察到时,停止加热;(4)、实验二:用提纯得到的精盐配制了50g5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有(填序号)。
(2)、粗盐提纯的操作顺序为(填操作序号)、称量精盐并计算产率。(3)、操作④中,当观察到时,停止加热;(4)、实验二:用提纯得到的精盐配制了50g5%的氯化钠溶液。经检测,溶质质量分数偏小,其原因可能有(填序号)。①氯化钠固体仍然不纯
②称量精盐时所用砝码生锈(实际质量比所标要大)
③量取水时,仰视读数
④装瓶时,有少量溶液洒出
25. 关于“水的净化”回答下列问题: (1)、图甲的操作中玻璃棒的作用是 , 实验结束时,小和同学发现滤液是浑浊的,导致这种现象的原因可能是(选填序号)。
(1)、图甲的操作中玻璃棒的作用是 , 实验结束时,小和同学发现滤液是浑浊的,导致这种现象的原因可能是(选填序号)。①滤纸没有紧贴漏斗内壁
②液体液面高于滤纸边缘
③滤纸单层的一边破损
④漏斗下端未紧靠烧杯内壁
⑤滤液中仍有可溶性物质未除去
(2)、小和同学改进实验后将浑浊的河水用图甲所示的装置进行净化,净化后得到的清澈的水是(填“纯净物”或“混合物”)。在该装置中,其漏斗中滤纸的放置方向应为(填序号)。(3)、图乙进行的是蒸馏操作,烧瓶中放入一些碎瓷片的目的是 , 冷凝管中冷水应该是从进入(填“a”或“b”)。(4)、小和同学选取下列实验方法分离物质,将分离方法的字母填在横线上。a.降温结晶
b.蒸发结晶
c.蒸馏法
d.过滤法
①分离饱和食盐水与沙子的混合物。
②除去氯化钠溶液中的水分。
③分离四氯化碳(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
④从含硝酸钾和氯化钠的混合液中分离出硝酸钾。
26. 思维模型是依据事物发展内在规律所建立的解决问题的基本框架,能引导有序思维、增进深度理解、促进问题解决。小李建构了“混合物提纯”的思维模型: (1)、【初步理解】根据混合物组份的性质差异,获得混合物中目标组份。
(1)、【初步理解】根据混合物组份的性质差异,获得混合物中目标组份。
海水淡化是将海水中的盐与水分开,常压加热蒸馏法是其中的一种:常压下将海水加热形成水蒸气,再液化得到淡水的过程。从建模角度分析,海水加热形成水蒸气属于上述模型中的(选填“分离转移”或“反应转化”)。
(2)、【探究本质】根据组份的性质差异,选择合适方法,实现物质提纯。从含少量氯化钠的硝酸钾固体中提纯硝酸钾,是通过溶解、蒸发浓缩、冷却结晶、过滤、洗涤、干燥实现的。其中“冷却结晶”操作将硝酸钾晶体从饱和溶液中分离出来,是根据硝酸钾的性质,“蒸发”操作中使用玻璃棒的作用是。
(3)、【融合创新】依据科学原理,融合技术与工程,形成新颖而有价值的解决实际问题的方案。常压加热蒸馏法,能耗大、成本高。小李查阅资料获知,现在世界上的许多大型海水淡化工厂,都已经采用低压加热蒸馏法,请解释其蕴含的科学道理。
27. 粗盐的精制一般要经过以下操作流程:
请回答
(1)、操作④的名称是。(2)、操作⑤中除用到三脚架、玻璃棒、蒸发皿外,还需要用到等仪器(写一种)。(3)、若黑色代表泥沙,这操作④后展开滤纸,看到的情况最接近图中的。 (4)、实验结束后称量获得的精盐,若结果偏大,原因是____(填字母)。A、食盐没有全部溶解即过滤 B、蒸发时,食盐飞溅剧烈 C、蒸发后所得精盐很潮湿 D、蒸发皿内的精盐未全部转移到称量纸上28. 第十七届西博会“舞动的水滴展”在西湖水面上举行。展览主角五个“大水滴”代表浙江五水共治,呼吁珍惜水资源,热爱自然。
(4)、实验结束后称量获得的精盐,若结果偏大,原因是____(填字母)。A、食盐没有全部溶解即过滤 B、蒸发时,食盐飞溅剧烈 C、蒸发后所得精盐很潮湿 D、蒸发皿内的精盐未全部转移到称量纸上28. 第十七届西博会“舞动的水滴展”在西湖水面上举行。展览主角五个“大水滴”代表浙江五水共治,呼吁珍惜水资源,热爱自然。 (1)、大水滴漂浮在水面上时,它受到浮力(选填“大于”、“等于”或“小于”)它的重力。五水共治的一项重要工作是“抓节水”,请你谈谈日常节约用水的方法(写出一点)。(2)、“治污水”是五水共治的另一项重要工作为了防止水污染,你认为下列措施中可行的是____。A、不任意排放生活污水 B、禁止使用农药和化肥 C、及时拧紧水龙头 D、牲畜粪便适当处理后再施用(3)、水的循环利用是“抓节水”的一个重要举措。下列几个步骤可将河水转化为饮用水:
(1)、大水滴漂浮在水面上时,它受到浮力(选填“大于”、“等于”或“小于”)它的重力。五水共治的一项重要工作是“抓节水”,请你谈谈日常节约用水的方法(写出一点)。(2)、“治污水”是五水共治的另一项重要工作为了防止水污染,你认为下列措施中可行的是____。A、不任意排放生活污水 B、禁止使用农药和化肥 C、及时拧紧水龙头 D、牲畜粪便适当处理后再施用(3)、水的循环利用是“抓节水”的一个重要举措。下列几个步骤可将河水转化为饮用水:①化学沉降(用明矾)
②消毒杀菌(用漂白粉)
③自然沉降
④加热煮沸
以上处理过程最合理的顺序是。