专题六 分子、原子、离子、元素、同位素--浙教版科学八年级下册期末复习卷
试卷更新日期:2024-06-05 类型:复习试卷
一、选择题
-
1. 二氧化碳和一氧化碳分子中都含有氧原子和碳原子,但是二氧化碳和一氧化碳的化学性质完全不同,出现这一现象的主要原因是( )A、构成分子的原子种类和数目不同 B、构成分子的原子大小不同 C、构成分子的原子种类相同但数目不同 D、构成分子的原子种类不同2. 乙烯是脐橙等水果的环保催熟气体。乙烯的分子结构如图所示,则下列说法正确的是( )
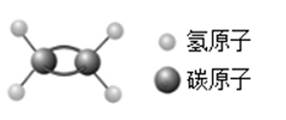 A、保持乙烯化学性质的微粒是乙烯分子 B、乙烯参与化学反应时,乙烯分子保持不变 C、乙烯分子由碳元素和氢元素组成 D、1个乙烯分子中含有2个氢分子3. 下列关于分子、原子、离子的说法中,正确的是( )A、分子的质量一定比原子大 B、原子是不能再分的粒子 C、原子得失电子后形成离子 D、分子、原子能构成物质,离子不能4. 图示是水分子分解示意图。图中
A、保持乙烯化学性质的微粒是乙烯分子 B、乙烯参与化学反应时,乙烯分子保持不变 C、乙烯分子由碳元素和氢元素组成 D、1个乙烯分子中含有2个氢分子3. 下列关于分子、原子、离子的说法中,正确的是( )A、分子的质量一定比原子大 B、原子是不能再分的粒子 C、原子得失电子后形成离子 D、分子、原子能构成物质,离子不能4. 图示是水分子分解示意图。图中 表示氧原子,
表示氧原子, 表示氢原子,
表示氢原子, 表示水分子,
表示水分子, 表示氧分子,
表示氧分子, 表示氢分子。从水分子分解示意图获得的信息中错误的是( )
表示氢分子。从水分子分解示意图获得的信息中错误的是( )
 A、分子由原子构成 B、原子是化学变化中的最小粒子 C、反应前后元素的种类和原子的个数都不会发生改变 D、一个水分子由一个氧元素和2个氢元素构成5. 下列关于分子和原子的说法,正确的是( )A、分子能直接构成物质,而原子不能 B、分子质量一定比原子大 C、在化学反应中,分子可分,原子不可分 D、分子间有空隙,而原子间无空隙6.
A、分子由原子构成 B、原子是化学变化中的最小粒子 C、反应前后元素的种类和原子的个数都不会发生改变 D、一个水分子由一个氧元素和2个氢元素构成5. 下列关于分子和原子的说法,正确的是( )A、分子能直接构成物质,而原子不能 B、分子质量一定比原子大 C、在化学反应中,分子可分,原子不可分 D、分子间有空隙,而原子间无空隙6.下列表示氢气和氧气发生的化学反应,下列说法中正确的是
 A、分子是化学变化中的最小粒子 B、每个氢分子由2个氢原子构成 C、每个水分子是由2个氢分子和1个氧分子构成 D、化学反应前后原子数和分子数均不发生变化7. 分子和原子的主要区别是()A、分子是构成物质的微粒,原子不是构成物质的微粒 B、分子质量都大于原子质量 C、分子永恒运动,原子在分子中是不运动的 D、分子在化学反应中可分,原子在化学反应中不能再分8. 2020年12月17日,嫦娥五号返回器携带月壤样品回到地球。月壤中蕴含He-3,它被认为是解决未来能源问题的重要物质之一。地球上的氦元素主要以He-4形式存在,He-4原子核内有2个质子和2个中子,下列说法正确的是( )A、 He-3原子核中有2个中子 B、He-3原子核外有3个电子 C、He-3和He-4是同位素原子 D、He-3和He-4的原子质量相同9.
A、分子是化学变化中的最小粒子 B、每个氢分子由2个氢原子构成 C、每个水分子是由2个氢分子和1个氧分子构成 D、化学反应前后原子数和分子数均不发生变化7. 分子和原子的主要区别是()A、分子是构成物质的微粒,原子不是构成物质的微粒 B、分子质量都大于原子质量 C、分子永恒运动,原子在分子中是不运动的 D、分子在化学反应中可分,原子在化学反应中不能再分8. 2020年12月17日,嫦娥五号返回器携带月壤样品回到地球。月壤中蕴含He-3,它被认为是解决未来能源问题的重要物质之一。地球上的氦元素主要以He-4形式存在,He-4原子核内有2个质子和2个中子,下列说法正确的是( )A、 He-3原子核中有2个中子 B、He-3原子核外有3个电子 C、He-3和He-4是同位素原子 D、He-3和He-4的原子质量相同9.科学家发现一种新元素。该元素原子核外电子数为117,中子数为174,相对原子质量为291,元素名称Ununseptium,符号Uus。请模仿甲,将该元素对应信息编写到图乙中相应位置,“①”处应填( )
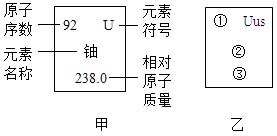 A、291 B、174 C、117 D、5710. 4月12日,2023中国茶叶大会暨第十七届新昌大佛龙井茶文化节在新昌开幕。茶叶中含有茶氨酸(C7H14O3N2)、儿茶素(C14H16O6)、咖啡碱(C8H10O2N4)、钾、镁、锌、硒、钙等多种成分,常饮有明目、利尿、降脂等功效;下列相关知识中正确的是( )
A、291 B、174 C、117 D、5710. 4月12日,2023中国茶叶大会暨第十七届新昌大佛龙井茶文化节在新昌开幕。茶叶中含有茶氨酸(C7H14O3N2)、儿茶素(C14H16O6)、咖啡碱(C8H10O2N4)、钾、镁、锌、硒、钙等多种成分,常饮有明目、利尿、降脂等功效;下列相关知识中正确的是( ) A、 C、H、O、N这些元素之间最根本的区别是质子数不同 B、钾、镁、锌、硒、钙都以单质的形式存在于茶叶中 C、茶氨酸和咖啡碱都是由C、H、O、N这四种元素组成的混合物 D、茶氨酸中含有7个C原子、14个H原子、3个O原子、2个N原子11. 碳—14是碳的一种具放射性的同位素原子,其相对原子质量为14。如图为碳—14原子的结构示意图,由图可知碳—14原子( )
A、 C、H、O、N这些元素之间最根本的区别是质子数不同 B、钾、镁、锌、硒、钙都以单质的形式存在于茶叶中 C、茶氨酸和咖啡碱都是由C、H、O、N这四种元素组成的混合物 D、茶氨酸中含有7个C原子、14个H原子、3个O原子、2个N原子11. 碳—14是碳的一种具放射性的同位素原子,其相对原子质量为14。如图为碳—14原子的结构示意图,由图可知碳—14原子( )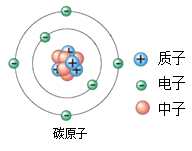 A、含有14个质子 B、含有6个中子 C、核电荷数为6 D、质子数和中子数相等12. 日本政府计划在2023年春季将福岛核废水排入海里,核废水中含有大量的氚。氚一旦进入人体可能会对人造成辐射损害。氢原子和氚原子结构如图所示,下 列说法正确的是( )
A、含有14个质子 B、含有6个中子 C、核电荷数为6 D、质子数和中子数相等12. 日本政府计划在2023年春季将福岛核废水排入海里,核废水中含有大量的氚。氚一旦进入人体可能会对人造成辐射损害。氢原子和氚原子结构如图所示,下 列说法正确的是( )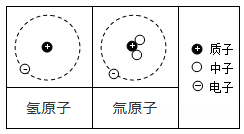 A、氚原子与氢原子的核外电子数相同 B、氚原子与氢原子的核电荷数不同 C、氚与氢元素不属于同种元素 D、氚原子与氢原子相对原子质量相同
A、氚原子与氢原子的核外电子数相同 B、氚原子与氢原子的核电荷数不同 C、氚与氢元素不属于同种元素 D、氚原子与氢原子相对原子质量相同二、填空题
-
13. 人类对原子结构的认识经历了一个相当长的时期,一代代科学家不断地发现和提出新的原子结构模型。请回答:(1)、以下是科学家及其提出的原子结构假设模型(如图所示),按照原子结构模型建立的先后顺排列为(填图中序号)。
①
 ②
② ③
③ ④
④ (2)、2022年4月26日,我国首次国产化碳—14批量生产在中核集团秦山核电站启动。下列模型能表示碳—14(有6个质子,8个中子)原子结构的是______(填字母编号)。A、
(2)、2022年4月26日,我国首次国产化碳—14批量生产在中核集团秦山核电站启动。下列模型能表示碳—14(有6个质子,8个中子)原子结构的是______(填字母编号)。A、 B、
B、 C、
C、 D、
D、 14. 读图回答下列问题。
14. 读图回答下列问题。 (1)、甲醛分子中有种原子;1个甲烷分子中有个原子;(2)、比较氢分子(或氧分子)与水分子,可得出的结论是。(3)、比较过氧化氢和水分子、乙炔分子和甲烷分子,可得出的结论是。
(1)、甲醛分子中有种原子;1个甲烷分子中有个原子;(2)、比较氢分子(或氧分子)与水分子,可得出的结论是。(3)、比较过氧化氢和水分子、乙炔分子和甲烷分子,可得出的结论是。三、解答题
-
15. 1910年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。实验结果发现:绝大多数α粒子仍沿原来方向前进,有少数发生了偏转,并且极少数α粒子的偏转超过90°,甚至几乎达到180°像是被金箔弹了回来。(1)、若原子内质量、正电荷分布均匀,则极少数α粒子(填“会”或“不会”)发生大角度散射。卢瑟福所说的“原子的绝大部分质量集中到了一个很小的结构上”,这个“很小的结构”指的是。(2)、1μm金箔包含了3000层金原子,绝大多数α粒子穿过后方向不变说明 (填字母,下同)。A、原子的质量是均匀分布的 B、原子内部绝大部分空间是空的(3)、科学家对原子结构的探究经历了三个过程,通过α粒子散射实验,你认为原子结构为以下的。
 16. 1989年世界卫生组织把铝列为食品污染源之一,每人每日的摄入量控制在0.004g以下。若在1kg米面食品中加入明矾2g(明矾的化学式为KAl(SO4)2•12H2O,相对分子质量为474),请回答下列问题:(1)、人从食物中摄入的铝指的是____________(填字母)。A、铝元素 B、铝单质 C、铝合金 D、只有明矾(2)、明矾中各元素的质量比K∶Al∶S∶O∶H=;铝元素的质量分数为(计算结果精确到0.1%)。(3)、如果某人一天吃了100g上述面食品,通过计算说明其摄入的铝的量是否超过安全摄入量?17. 1911年著名物理学家卢瑟福等人为探索原子的内部结构进行了如下实验,他们用一束质量远大于电子的高速运动的α粒子轰击金箔,发现:“大多数α粒子能穿过金箔,一小部分发生偏转,少数被反弹回来”。回答下列问题。(1)、1个α粒子由两个中子和两个质子构成,则α粒子带电(填“正”或“负”)(2)、1个α粒子与一个He-4原子构成上的差别是。(3)、根据实验现象中α粒子“大多数”与“极少数”的对比分析,你能想象出关于Au原子结构的结论是。18. 人类在探索物质世界和微观世界的历史长河中,充满了智慧。请你回答相关问题。(1)、下面的科学家中最早发现电子的是 (填字母)。A、道尔顿 B、汤姆森 C、卢瑟福 D、门捷列夫(2)、原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,科学家都运用了来表达他们的理论成果。(3)、碳一12、碳一13、碳一14都是碳元素的原子,它们的主要差别在于。(4)、人们很早就意识到物质都是由几种亘古不变的基本成分“元素”组成的。如图是两个微粒的结构模型示意图,这两个微粒是否属于同种元素?你的观点及依据是。
16. 1989年世界卫生组织把铝列为食品污染源之一,每人每日的摄入量控制在0.004g以下。若在1kg米面食品中加入明矾2g(明矾的化学式为KAl(SO4)2•12H2O,相对分子质量为474),请回答下列问题:(1)、人从食物中摄入的铝指的是____________(填字母)。A、铝元素 B、铝单质 C、铝合金 D、只有明矾(2)、明矾中各元素的质量比K∶Al∶S∶O∶H=;铝元素的质量分数为(计算结果精确到0.1%)。(3)、如果某人一天吃了100g上述面食品,通过计算说明其摄入的铝的量是否超过安全摄入量?17. 1911年著名物理学家卢瑟福等人为探索原子的内部结构进行了如下实验,他们用一束质量远大于电子的高速运动的α粒子轰击金箔,发现:“大多数α粒子能穿过金箔,一小部分发生偏转,少数被反弹回来”。回答下列问题。(1)、1个α粒子由两个中子和两个质子构成,则α粒子带电(填“正”或“负”)(2)、1个α粒子与一个He-4原子构成上的差别是。(3)、根据实验现象中α粒子“大多数”与“极少数”的对比分析,你能想象出关于Au原子结构的结论是。18. 人类在探索物质世界和微观世界的历史长河中,充满了智慧。请你回答相关问题。(1)、下面的科学家中最早发现电子的是 (填字母)。A、道尔顿 B、汤姆森 C、卢瑟福 D、门捷列夫(2)、原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,科学家都运用了来表达他们的理论成果。(3)、碳一12、碳一13、碳一14都是碳元素的原子,它们的主要差别在于。(4)、人们很早就意识到物质都是由几种亘古不变的基本成分“元素”组成的。如图是两个微粒的结构模型示意图,这两个微粒是否属于同种元素?你的观点及依据是。