专题九 酸、碱、盐--2023-2024学年浙教版科学中考专题突破
试卷更新日期:2024-05-21 类型:三轮冲刺
一、选择题
-
1. 取稀盐酸与氢氧化钠反应后的溶液进行实验,下列能说明两者恰好完全反应的是( )A、滴入硫酸铜溶液,生成蓝色沉淀 B、滴入酚酞试液,溶液显无色 C、加入氧化铜粉末,溶液变蓝色 D、测得溶液中与的个数比为1:12. 为研究稀硫酸的化学性质,某小组如图所示进行实验,充分反应后,只有试管甲中无固体剩余。下列说法不正确的是()
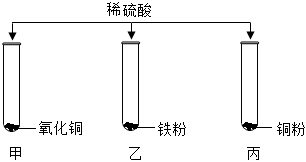 A、甲中发生的反应是CuO+H2SO4═CuSO4+H2O B、试管乙反应后中有黑色固体剩余 C、乙和丙可证明铁的金属活动性比铜强 D、实验结束后,将三支试管中的剩余物倒入废液缸中,充分混合后过滤,取少量滤渣,向其中滴加稀硫酸,有气泡产生。则过滤后得到的滤渣的成分是铁3. 如图是一种简易的自动化彩色喷泉实验装置。注射器中是滴有紫包菜汁的氢氧化钠溶液(pH=10),小药瓶中充演氯化氢气体(极易溶于水)。实验开始时推动注射器使少量溶液进人小药瓶,然后松开手,可以观察到注射器活塞向左移动,小药瓶中出现了美丽的彩色喷泉。已知紫包菜汁的变色范围如表所示,则以下说法错误的是()
A、甲中发生的反应是CuO+H2SO4═CuSO4+H2O B、试管乙反应后中有黑色固体剩余 C、乙和丙可证明铁的金属活动性比铜强 D、实验结束后,将三支试管中的剩余物倒入废液缸中,充分混合后过滤,取少量滤渣,向其中滴加稀硫酸,有气泡产生。则过滤后得到的滤渣的成分是铁3. 如图是一种简易的自动化彩色喷泉实验装置。注射器中是滴有紫包菜汁的氢氧化钠溶液(pH=10),小药瓶中充演氯化氢气体(极易溶于水)。实验开始时推动注射器使少量溶液进人小药瓶,然后松开手,可以观察到注射器活塞向左移动,小药瓶中出现了美丽的彩色喷泉。已知紫包菜汁的变色范围如表所示,则以下说法错误的是()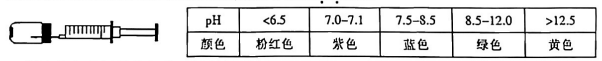 A、滴有紫包菜汁的氢氧化钠溶液呈绿色 B、小药瓶中液体颜色变化依次为:粉红色→紫色→蓝色→绿色 C、液体颜色为粉红色时小药瓶中所含的溶质是NaCl D、紫包菜汁可以用做酸碱指示剂4. 为了探究酸碱中和反应是否放热,某同学设计了如图所示的实验装置(夹持等固定装置图略),针对该实验目的,下列评价或改进,错误的是( )
A、滴有紫包菜汁的氢氧化钠溶液呈绿色 B、小药瓶中液体颜色变化依次为:粉红色→紫色→蓝色→绿色 C、液体颜色为粉红色时小药瓶中所含的溶质是NaCl D、紫包菜汁可以用做酸碱指示剂4. 为了探究酸碱中和反应是否放热,某同学设计了如图所示的实验装置(夹持等固定装置图略),针对该实验目的,下列评价或改进,错误的是( )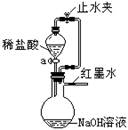 A、若观察到红墨水向右移,则说明该实验一定有放热现象 B、为了使实验现象更明显,可改用氢氧化钠固体 C、在打开活塞a之前应先打开橡皮管上的止水夹 D、为了使实验更具有说服力,可用氢氧化钾溶液再次实验5. 为了研究稀硫酸的性质,小金设计了如图所示实验。分别将过量的稀硫酸滴入盛有Zn粒、Fe2O3粉末、Cu(OH)2固体和Ba(NO3)2溶液的4支试管中。关于实验现象和分析正确的是( )
A、若观察到红墨水向右移,则说明该实验一定有放热现象 B、为了使实验现象更明显,可改用氢氧化钠固体 C、在打开活塞a之前应先打开橡皮管上的止水夹 D、为了使实验更具有说服力,可用氢氧化钾溶液再次实验5. 为了研究稀硫酸的性质,小金设计了如图所示实验。分别将过量的稀硫酸滴入盛有Zn粒、Fe2O3粉末、Cu(OH)2固体和Ba(NO3)2溶液的4支试管中。关于实验现象和分析正确的是( ) A、反应后4支试管中均得到无色溶液 B、Fe2O3粉末与稀硫酸反应会生成FeSO4 C、反应后的物质全部倒进废液缸不再发生新的反应 D、改成稀盐酸进行实验,实验现象都与稀硫酸相同6. 为测定一瓶久置的氢氧化钠溶液中碳酸钠的质量分数,小金进行了如下探究:取该溶液50g于锥形瓶中,向锥形瓶中滴加一定浓度的稀盐酸。实验测得锥形瓶中溶液的总质量与加入稀盐酸的质量关系如图所示,下列说法错误的是( )
A、反应后4支试管中均得到无色溶液 B、Fe2O3粉末与稀硫酸反应会生成FeSO4 C、反应后的物质全部倒进废液缸不再发生新的反应 D、改成稀盐酸进行实验,实验现象都与稀硫酸相同6. 为测定一瓶久置的氢氧化钠溶液中碳酸钠的质量分数,小金进行了如下探究:取该溶液50g于锥形瓶中,向锥形瓶中滴加一定浓度的稀盐酸。实验测得锥形瓶中溶液的总质量与加入稀盐酸的质量关系如图所示,下列说法错误的是( ) A、m1的值无法确定 B、理论上稀盐酸的溶质质量分数可以求解 C、加入m1g稀盐酸后,才开始产生气泡 D、该方法测得的碳酸钠质量分数可能偏小7. 奥运五环的蓝、黄、黑、绿和红色象征欧、亚、非、大洋、美五大洲和全世界的运动员在奥运会上相聚一堂。若要用化学试剂给如下有凹槽的塑料奥运五环加上颜色(注:所给试剂恰好完全反应或完全溶解,凹槽可盛放溶液),你认为合理的是( )
A、m1的值无法确定 B、理论上稀盐酸的溶质质量分数可以求解 C、加入m1g稀盐酸后,才开始产生气泡 D、该方法测得的碳酸钠质量分数可能偏小7. 奥运五环的蓝、黄、黑、绿和红色象征欧、亚、非、大洋、美五大洲和全世界的运动员在奥运会上相聚一堂。若要用化学试剂给如下有凹槽的塑料奥运五环加上颜色(注:所给试剂恰好完全反应或完全溶解,凹槽可盛放溶液),你认为合理的是( ) A、用铜粉末和稀硫酸给蓝环上色 B、用铁粉和稀盐酸给黄色环上色 C、用氧化铁和稀盐酸给绿环上色 D、用氢氧化钠和酚酞给红环上色8. 小敏在吃皮蛋时尝到了涩味。为找到去除涩味的方法,小敏查阅资料发现皮蛋制作时需要用到“灰料”进行腌制。“灰料”的制作方法是将一定比例的生石灰,纯碱以及食盐混合,并加水调至糊状。根据上述信息分析,以下选项正确的是( )A、“灰料”中的生石灰和纯碱分别是Ca(OH)2和Na2CO3 B、“灰料”的制作过程中只涉及了复分解反应 C、“灰料”溶液中可能含有Na+ , Cl- , OH- , Ca2+ , CO32- D、皮蛋沾点食醋再吃,可缓解皮蛋的涩味9. 如图所示,小乐在实验室分别完成①②两个实验后,依次将①②反应后的废液缓慢倒入同一洁净的废液缸,当②的废液倒入时,观察到废液缸中先有气泡产生,然后又出现了白色沉淀。则下列分析错误的是( )
A、用铜粉末和稀硫酸给蓝环上色 B、用铁粉和稀盐酸给黄色环上色 C、用氧化铁和稀盐酸给绿环上色 D、用氢氧化钠和酚酞给红环上色8. 小敏在吃皮蛋时尝到了涩味。为找到去除涩味的方法,小敏查阅资料发现皮蛋制作时需要用到“灰料”进行腌制。“灰料”的制作方法是将一定比例的生石灰,纯碱以及食盐混合,并加水调至糊状。根据上述信息分析,以下选项正确的是( )A、“灰料”中的生石灰和纯碱分别是Ca(OH)2和Na2CO3 B、“灰料”的制作过程中只涉及了复分解反应 C、“灰料”溶液中可能含有Na+ , Cl- , OH- , Ca2+ , CO32- D、皮蛋沾点食醋再吃,可缓解皮蛋的涩味9. 如图所示,小乐在实验室分别完成①②两个实验后,依次将①②反应后的废液缓慢倒入同一洁净的废液缸,当②的废液倒入时,观察到废液缸中先有气泡产生,然后又出现了白色沉淀。则下列分析错误的是( ) A、若向①反应后的废液中滴加紫色石蕊试液,石蕊试液会变红 B、若向②反应后的废液中滴加无色酚酞试液,酚酞试液会变红 C、废液缸中最终的废液里一定含氯离子,一定不含氢离子 D、废液缸中最终的废液里一定含钠离子,一定不含钙离子10. 某黑色固体粉末可能是Fe、CuO、C中一种或几种.为了探究其成分,小明同学按照
A、若向①反应后的废液中滴加紫色石蕊试液,石蕊试液会变红 B、若向②反应后的废液中滴加无色酚酞试液,酚酞试液会变红 C、废液缸中最终的废液里一定含氯离子,一定不含氢离子 D、废液缸中最终的废液里一定含钠离子,一定不含钙离子10. 某黑色固体粉末可能是Fe、CuO、C中一种或几种.为了探究其成分,小明同学按照如图所示流程进行了实验。关于该实验有以下说法:
①若溶液甲呈浅绿色,则原黑色固体粉末中一定含有Fe;
②若步骤Ⅱ中无明显现象,则固体乙中最多只能有三种物质;
③若步骤Ⅱ中有气泡产生,则固体乙中一定有Fe;
④若步骤Ⅱ中有红色固体析出,则固体乙中一定无CuO;
⑤固体乙呈红色,则原固体中一定含有Fe和CuO。
以上说法中正确的是( )
 A、①⑤ B、②③ C、①④ D、①②
A、①⑤ B、②③ C、①④ D、①②二、实验探究题
-
11. 实验小组同学向盛有2mL稀硫酸的试管中加入2mL氢氧化钠溶液,未观察到明显现象。
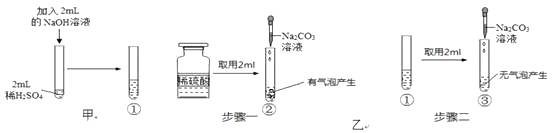
【提出问题】两者是否发生了化学反应?
【实验探究】将盛有上述实验混合液的试管标为①,如图甲。
小华:测得实验所用稀硫酸的pH<7,试管①中溶液pH>7。于是得出结论:。
小敏:取两支试管,编号为②和③,分别加入稀硫酸和试管①中溶液各2mL,逐滴滴加Na2CO3溶液至过量,实验过程与现象如图乙,由此他得出了与小华一样的实验结论。
【反思评价】小军认为小敏在实验设计中存在不够严密的地方,请帮他指出:。
【交流讨论】试管③中的溶液中有哪些溶质?同学们分析了两位同学的实验过程,一致认为没有H2SO4 , 其理由是。在此基础上,同学们提出了二种推理:
推理1:含有Na2SO4、Na2CO3和NaOH 推理2:含有Na2SO4、Na2CO3
正确的是推理(选填“1”或“2”)。
12. 科学兴趣小组进行了如图所示实验,他们观察到U型管左侧产生白色沉淀,右侧产生气泡。实验后,充分振荡U形管,发现管内仍有白色固体残留,将U形管内的白色物质过滤后,他们对滤液成分进行了进一步探究。
 (1)、【问题】滤液中可能含有哪些溶质?
(1)、【问题】滤液中可能含有哪些溶质?【猜想】猜想一:溶质为NaCl;猜想二:溶质为NaCl和BaCl2;猜想三:溶质为NaCl、BaCl2、HCl;猜想四:溶质为;
(2)、【分析】根据已学知识,可判断猜想三是不合理的,理由是;(3)、【实验】接着他们取部分滤液于试管中,向其中滴加少量的Na2SO4溶液,观察到无明显现象。为验证猜想,他们进一步实验,往试管中继续滴加稀HCl,若观察到 , 则你的猜想是正确的。
【交流】在确定化学反应后所得溶液中溶质成分时,除了考虑生成物外,还需要考虑反应物是否有剩余。13. 《天工开物》中有“煤饼烧石成灰”的记载(文中的“石”指石灰石),拓展课上,小康对其展开如下探究:如图甲所示,先利用煤气灯(煤气的主要成分是CO)煅烧石灰石,然后完成后续操作;最后又补充做了如图乙所示实验。
观察到的现象:①烧杯内壁上的澄清石灰水变浑浊;
②试管A中无色酚酞试液变红,试管B中无色酚酞试液不变色。
(1)、能作为石灰石发生化学变化的证据是现象(选填“①”“②”或“①和②”)。(2)、继续向试管A上层清液中逐滴滴加稀盐酸,至红色恰好褪去。轻轻晃动试管A,溶液自下而上又变为红色,此时试管A红色溶液中一定存在的溶质有:(除指示剂外)。
(3)、为检验图甲所示实验中的石灰石是否完全分解,小康同学取一定量煅烧后产物于试管中,向其中先加入适量的水,再加入少量稀盐酸溶液,发现无气泡产生,说明石灰石已经完全分解。你认为该结论合理吗?请做出判断并说明理由:。三、填空题
-
14. “天宫课堂”上航天员做的泡腾片实验,让同学们再次感受到科学的魅力。泡腾片中含有碳酸钠或碳酸氢钠等物质,科学兴趣小组决定对碳酸钠和碳酸氢钠溶液的酸碱度及性质进行探究。
 (1)、用pH试纸测得等浓度的碳酸氢钠溶液pH为9,碳酸钠溶液pH为11。请写出pH试纸的正确使用方法: 。(2)、向碳酸钠溶液中滴加几滴无色酚酞试液,观察到试液变成色。(3)、向盛有碳酸钠溶液的烧杯中,逐滴加入一定浓度的稀盐酸并充分搅拌,测得pH变化与时间的关系如图所示。d点溶液中的溶质为。15. 化学兴趣小组同学欲除去固体氢氧化钠中混有的氯化钙。设计实验方案如图,请依据实验回答问题,
(1)、用pH试纸测得等浓度的碳酸氢钠溶液pH为9,碳酸钠溶液pH为11。请写出pH试纸的正确使用方法: 。(2)、向碳酸钠溶液中滴加几滴无色酚酞试液,观察到试液变成色。(3)、向盛有碳酸钠溶液的烧杯中,逐滴加入一定浓度的稀盐酸并充分搅拌,测得pH变化与时间的关系如图所示。d点溶液中的溶质为。15. 化学兴趣小组同学欲除去固体氢氧化钠中混有的氯化钙。设计实验方案如图,请依据实验回答问题, (1)、写出加过量Na2CO3 , 溶液所发生的反应方程式 。(2)、写出操作A的名称 。(3)、分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果(选填“增大”、“不变”,“减少”)。16. 如图甲所示,烧杯中为一定量的碳酸钙和稀盐酸反应后的溶液,用胶头滴管逐滴滴入Na2CO3溶液,并用pH传感器测得烧杯内溶液的pH变化如图乙所示。
(1)、写出加过量Na2CO3 , 溶液所发生的反应方程式 。(2)、写出操作A的名称 。(3)、分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果(选填“增大”、“不变”,“减少”)。16. 如图甲所示,烧杯中为一定量的碳酸钙和稀盐酸反应后的溶液,用胶头滴管逐滴滴入Na2CO3溶液,并用pH传感器测得烧杯内溶液的pH变化如图乙所示。 (1)、胶头滴管逐滴滴入Na2CO3溶液的过程中,烧杯中可观察到的实验现象是。(2)、当加入amLNa2CO3溶液时,烧杯内溶液中的溶质是。17. 某小组同学通过如下四组实验对稀硫酸部分化学性质进行验证:
(1)、胶头滴管逐滴滴入Na2CO3溶液的过程中,烧杯中可观察到的实验现象是。(2)、当加入amLNa2CO3溶液时,烧杯内溶液中的溶质是。17. 某小组同学通过如下四组实验对稀硫酸部分化学性质进行验证:①Mg和稀硫酸;②MgO和稀硫酸;③Ba(NO3)2溶液和稀硫酸;④NaOH溶液和稀硫酸。实验结束后将所有反应后的溶液混合进行了如图操作,请分析并回答下列问题:
 (1)、实验④NaOH溶液和稀硫酸混合后无明显现象,再将打磨过的铁丝浸入该实验后的溶液中,仍无明显现象,据此(选填“能”或“不能”)验证NaOH溶液和H2SO4发生了反应。(2)、实验结束后进行的操作①的名称为(3)、滤液b的成分中一定含有(用化学式表示)。18. 实验室有失去标签的三瓶无色溶液:H2SO4溶液、NaOH溶液和KNO3溶液,要求只用无色酚酞一种试剂鉴别它们。请完成如下实验:(1)、取少量三种溶液分别加到A、B、C三支试管中,各滴入1~2滴无色酚酞试液,观察到A试管中的溶液变成红色。则A试管中的是溶液。(2)、任取剩余两种溶液中的一种,滴入上述试验后的A试管中,若观察到A试管中的溶液 , 则滴入的是溶液。
(1)、实验④NaOH溶液和稀硫酸混合后无明显现象,再将打磨过的铁丝浸入该实验后的溶液中,仍无明显现象,据此(选填“能”或“不能”)验证NaOH溶液和H2SO4发生了反应。(2)、实验结束后进行的操作①的名称为(3)、滤液b的成分中一定含有(用化学式表示)。18. 实验室有失去标签的三瓶无色溶液:H2SO4溶液、NaOH溶液和KNO3溶液,要求只用无色酚酞一种试剂鉴别它们。请完成如下实验:(1)、取少量三种溶液分别加到A、B、C三支试管中,各滴入1~2滴无色酚酞试液,观察到A试管中的溶液变成红色。则A试管中的是溶液。(2)、任取剩余两种溶液中的一种,滴入上述试验后的A试管中,若观察到A试管中的溶液 , 则滴入的是溶液。