2024年中考化学三轮冲刺专项训练--金属、酸、碱、盐
试卷更新日期:2024-05-20 类型:三轮冲刺
一、选择题
-
1. 我国的矿物种类比较齐全,储量很丰富,但是矿物不能再生。下列能保护金属资源的是( )A、废旧金属不需要回收利用 B、矿物资源无限,可以任意开采 C、寻找金属代用品 D、将铁钉放置于潮湿的空气中2. 化学实验操作要科学规范。下列实验操作正确的是( )A、称量NaOH固体
 B、稀释浓硫酸
B、稀释浓硫酸 C、加热液体
C、加热液体 D、测定溶液pH
D、测定溶液pH 3. 走近千年文物,人们发现青铜器在含有Cl-的环境中易生成CuCl,随着环境条件的变化而发生锈蚀,锈层物质成分示意图如图所示。下列叙述错误的是( )
3. 走近千年文物,人们发现青铜器在含有Cl-的环境中易生成CuCl,随着环境条件的变化而发生锈蚀,锈层物质成分示意图如图所示。下列叙述错误的是( ) A、铜绿中含有Cu、H、O、C四种元素 B、CuCl与O2、H2O发生化合反应生成Cu2(OH)3Cl C、青铜器在锈蚀的过程中铜元素的化合价升高 D、在干燥、无氧的环境中有利于青铜器的保护4. 下列图像能正确反映对应关系的是( )A、高温条件下木炭还原CuO
A、铜绿中含有Cu、H、O、C四种元素 B、CuCl与O2、H2O发生化合反应生成Cu2(OH)3Cl C、青铜器在锈蚀的过程中铜元素的化合价升高 D、在干燥、无氧的环境中有利于青铜器的保护4. 下列图像能正确反映对应关系的是( )A、高温条件下木炭还原CuO B、pH=12的Ca(OH)2溶液中加水稀释
B、pH=12的Ca(OH)2溶液中加水稀释 C、向等质量的铁粉和锌粉中加入足量等浓度的稀硫酸
C、向等质量的铁粉和锌粉中加入足量等浓度的稀硫酸 D、用等质量的KClO3在有无催化剂并加热的条件下制氧气
D、用等质量的KClO3在有无催化剂并加热的条件下制氧气 5. 用下列各组物质进行实验。能验证Mg、Ag、Cu三种金属活动性强弱的是A、Mg、Ag、Cu、稀硫酸 B、Mg、Ag、溶液 C、Ag、Cu、溶液 D、Ag、溶液、溶液6. 如图实验中有关说法不正确的是( )
5. 用下列各组物质进行实验。能验证Mg、Ag、Cu三种金属活动性强弱的是A、Mg、Ag、Cu、稀硫酸 B、Mg、Ag、溶液 C、Ag、Cu、溶液 D、Ag、溶液、溶液6. 如图实验中有关说法不正确的是( ) A、甲:利用红磷燃烧实验验证质量守恒定律,燃烧时气球胀大不会影响实验 B、乙:根据实验现象呼出气体中木条熄灭可证明呼出气体中的二氧化碳含量比空气中高 C、丙:检查装置气密性时,看到导管口有气泡冒出,说明气密性良好 D、丁:稀释浓硫酸时,玻璃棒不断搅拌的目的是使热量迅速散失7. 如图图像与实验设计对应正确的有( )
A、甲:利用红磷燃烧实验验证质量守恒定律,燃烧时气球胀大不会影响实验 B、乙:根据实验现象呼出气体中木条熄灭可证明呼出气体中的二氧化碳含量比空气中高 C、丙:检查装置气密性时,看到导管口有气泡冒出,说明气密性良好 D、丁:稀释浓硫酸时,玻璃棒不断搅拌的目的是使热量迅速散失7. 如图图像与实验设计对应正确的有( )图像




实验设计
向未经打磨的铝片中滴加适量稀盐酸
向一定量氢氧化钡溶液中加入稀硫酸至过量
向等质量的和中分别加入足量等浓度的稀硫酸
常温下向溶液中不断加入水稀释
A、1项 B、2项 C、3项 D、4项8. 下列实验方案中,实验设计能达到实验目的的是( )方案
实验目的
实验设计
A
探究稀盐酸与氢氧化钠溶液是否恰好完全反应
向反应后所得的溶液中滴加硝酸银溶液
B
鉴别氯化钡、硫酸钾、碳酸钾、稀盐酸四种溶液
将组内物质相互混合,观察现象
C
除去CuCl2溶液中少量的FeCl2
加入足量的铜粉,过滤
D
分离NaCl、CaCl2溶液
加适量Na2CO3溶液,过滤、洗涤
A、A B、B C、C D、D9. 下列有关实验现象描述正确的是( )A、向硝酸钡溶液中滴加稀盐酸产生白色沉淀 B、打开浓硫酸的瓶塞,瓶口有白雾冒出 C、硫在氧气中燃烧发出明亮的蓝紫色火焰 D、铁在氧气中燃烧生成四氧化三铁10. 下列离子能在pH=11的溶液中大量共存的是( )A、K+、Na+、、OH- B、K+、H+、Cl-、 C、H+、Ba2+、Cl-、 D、K+、、、11. 下列实验操作不能达到实验目的是( )选项
实验目的
实验操作
A
鉴别NaOH和NaCl两种固体
分别加入少量水溶解
B
除去NaCl溶液中少量Na2SO4
先加入Ba(NO3)2溶液,后过滤
C
除去H2中少量的水蒸气
将混合气体通过装有浓硫酸的洗气瓶
D
鉴别化肥KCl和NH4Cl
取样与熟石灰混合研磨,闻气味
A、A B、B C、C D、D12. 向硝酸银、硝酸铜的混合溶液中加入一定质量锌粉,充分反应后过滤,得到滤渣 A 和滤液 B.将滤渣 A 加入适量稀硫酸中,有气泡产生。以下对滤渣 A 和滤液 B 的成分的判断,合理的( )A、滤液 B 中的溶质是 Zn(NO3)2 B、滤液 B 中的溶质是 Zn(NO3)2 和 Cu(NO3)2 C、滤渣 A 是 Cu 和 Zn D、滤渣 A 是 Ag 和 Zn13. 对下列事实的解释不合理的是( )A、铁和钢的性能不同——含碳量不同 B、镁原子和镁离子化学性质不同——最外层电子数不同 C、粗盐提纯得到精盐的产率偏高一一蒸发时未用玻璃棒搅拌 D、将糖水密封放置,温度不变,蔗糖与水不会分离——溶液具有稳定性14. 元素化合价和物质类别是认识物质的两个重要维度。如下图为硫元素“价类二维图”。下列说法错误的是( ) A、物质A在空气中燃烧产生微弱的淡蓝色火焰 B、物质B可形成酸雨 C、实验室中常用物质D的浓溶液干燥氨气 D、E点表示的物质可能是15. 下列图像能正确反映其对应关系的是 ( )
A、物质A在空气中燃烧产生微弱的淡蓝色火焰 B、物质B可形成酸雨 C、实验室中常用物质D的浓溶液干燥氨气 D、E点表示的物质可能是15. 下列图像能正确反映其对应关系的是 ( ) A、水通电分解产生氢气和氧气 B、一定质量的碳在密闭容器中燃烧 C、向等质量等浓度的稀盐酸中加入足量的锌粉和铁粉 D、某温度时,向一定质量的饱和石灰水中加入少量生石灰16. 某同学在探究酸碱盐反应实验时,向硫酸铜和硫酸混合液中逐渐加入 20%的氢氧化钠溶液,所得溶液质量与所加氢氧化钠溶液的关系如图所示。下列说法错误的是 ( )
A、水通电分解产生氢气和氧气 B、一定质量的碳在密闭容器中燃烧 C、向等质量等浓度的稀盐酸中加入足量的锌粉和铁粉 D、某温度时,向一定质量的饱和石灰水中加入少量生石灰16. 某同学在探究酸碱盐反应实验时,向硫酸铜和硫酸混合液中逐渐加入 20%的氢氧化钠溶液,所得溶液质量与所加氢氧化钠溶液的关系如图所示。下列说法错误的是 ( ) A、M点的溶质为硫酸铜、硫酸钠和硫酸 B、原混合溶液中含硫酸的质量为9.8g C、b点溶液中含一种溶质,其质量为14.2g D、ab段溶液质量上升变缓的原因是反应过程中有沉淀生成17. 科学思维是化学学习要养成的核心素养之一。下列说法不正确的是 ( )A、比较:金刚石和石墨的组成元素相同,故两者的物理性质相同 B、分类:煤、石油和天然气属于化石燃料,是不可再生能源 C、分析:碳可用于冶金工业,因为单质碳具有还原性 D、推理:氢氧化钠溶液能使无色酚酞溶液变红,故氢氧化钡溶液也能使酚酞溶液变红18. 推理是化学学习中常用的思维方法,下列推理正确的是 ( )A、分子、原子均不带电,所以不带电的粒子一定是分子或原子 B、中和反应生成了盐和水,所以酸与碱反应生成盐和水的反应一定是中和反应 C、溶液是均一的、稳定的混合物,所以均一的、稳定的液体一定是溶液 D、活泼金属能与酸反应产生气泡,所以能与酸反应产生气泡的固体一定是活泼金属19. 如图中A、B、C、D是两圆相交的部分,表示指示剂与酸、碱溶液作用时所显示的颜色,则其中表示错误的是( )
A、M点的溶质为硫酸铜、硫酸钠和硫酸 B、原混合溶液中含硫酸的质量为9.8g C、b点溶液中含一种溶质,其质量为14.2g D、ab段溶液质量上升变缓的原因是反应过程中有沉淀生成17. 科学思维是化学学习要养成的核心素养之一。下列说法不正确的是 ( )A、比较:金刚石和石墨的组成元素相同,故两者的物理性质相同 B、分类:煤、石油和天然气属于化石燃料,是不可再生能源 C、分析:碳可用于冶金工业,因为单质碳具有还原性 D、推理:氢氧化钠溶液能使无色酚酞溶液变红,故氢氧化钡溶液也能使酚酞溶液变红18. 推理是化学学习中常用的思维方法,下列推理正确的是 ( )A、分子、原子均不带电,所以不带电的粒子一定是分子或原子 B、中和反应生成了盐和水,所以酸与碱反应生成盐和水的反应一定是中和反应 C、溶液是均一的、稳定的混合物,所以均一的、稳定的液体一定是溶液 D、活泼金属能与酸反应产生气泡,所以能与酸反应产生气泡的固体一定是活泼金属19. 如图中A、B、C、D是两圆相交的部分,表示指示剂与酸、碱溶液作用时所显示的颜色,则其中表示错误的是( )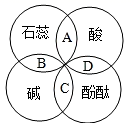 A、紫色 B、蓝色 C、红色 D、无色20. 向装有50g稀硫酸的小烧杯中,不断慢慢滴加10%的Ba(OH)2溶液至过量.小烧杯中有关量的变化情况见下图.其中肯定不正确的是( )A、
A、紫色 B、蓝色 C、红色 D、无色20. 向装有50g稀硫酸的小烧杯中,不断慢慢滴加10%的Ba(OH)2溶液至过量.小烧杯中有关量的变化情况见下图.其中肯定不正确的是( )A、 B、
B、 C、
C、 D、
D、 21. 下列物质间的转化,通过一步化学反应不能实现的是( )A、Fe→Cu→Ag B、CaCO3→CaO→Ca(OH)2 C、H2→H2O→O2 D、NaCl→NaNO3→Na2SO422. 现有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并放出氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化。根据以上实验事实可知,X、Y、Z的金属活动性顺序是( )A、X>Y>Z B、Y>X>Z C、X>Z>Y D、Z>Y>X23. 下列实验方案不能达到实验目的是( )A、鉴别碳酸钙和氢氧化钙分别加一定量的氯化铵,研磨闻气味 B、除去KCl中的K2CO3加过量的稀盐酸溶液,过滤后蒸发结晶 C、分离KCl和MnO2混合物:加入足量水溶解,过滤,洗涤,干燥 D、检验CO气体中是否混有CO2:将气体通入澄清石灰水,观察是否变浑浊24. 向装有一定量硝酸亚铁和硝酸银混合溶液的试管中,缓慢加入锌粉,充分反应。下列关于试管中物质的变化关系图错误的是( )A、
21. 下列物质间的转化,通过一步化学反应不能实现的是( )A、Fe→Cu→Ag B、CaCO3→CaO→Ca(OH)2 C、H2→H2O→O2 D、NaCl→NaNO3→Na2SO422. 现有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并放出氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化。根据以上实验事实可知,X、Y、Z的金属活动性顺序是( )A、X>Y>Z B、Y>X>Z C、X>Z>Y D、Z>Y>X23. 下列实验方案不能达到实验目的是( )A、鉴别碳酸钙和氢氧化钙分别加一定量的氯化铵,研磨闻气味 B、除去KCl中的K2CO3加过量的稀盐酸溶液,过滤后蒸发结晶 C、分离KCl和MnO2混合物:加入足量水溶解,过滤,洗涤,干燥 D、检验CO气体中是否混有CO2:将气体通入澄清石灰水,观察是否变浑浊24. 向装有一定量硝酸亚铁和硝酸银混合溶液的试管中,缓慢加入锌粉,充分反应。下列关于试管中物质的变化关系图错误的是( )A、 B、
B、 C、
C、 D、
D、 25. “证据推理与模型认知”是化学学科核心素养的重要组成部分,以下推理正确的是( )A、中和反应生成盐和水,所以生成盐和水的反应都是中和反应 B、单质只含有一种元素,所以只含有一种元素的物质一定是单质 C、燃烧都伴随有发光放热现象,所以有发光放热现象的一定是燃烧 D、NaOH、Ca(OH)2等碱溶液都能使酚酞试液变红,所以使酚酞试液变红的一定是碱性溶液26. 某化学兴趣小组为探究铝、铜、银三种金属的活动性顺序,利用实验室中的相关药品设计了如下实验方案(实验用到的三种金属丝均已打磨干净):①稀盐酸、铝、铜、银②硫酸铜溶液、铝、银③硫酸铝溶液、硝酸银溶液、铜④硫酸铝溶液、铜、银⑤硝酸银溶液、铝、铜。其中能验证铝、铜、银金属活动性顺序的是( )A、②③⑤ B、①②③ C、③④⑤ D、①②④27. 取等质量的Na2CO3和NaHCO3固体分别置于两个体积相同的密闭容器中,分别一次性加入等浓度等体积的过量稀硫酸,用压强传感器测得两容器内压强随时间的变化关系如图所示。下列说法正确的是( )
25. “证据推理与模型认知”是化学学科核心素养的重要组成部分,以下推理正确的是( )A、中和反应生成盐和水,所以生成盐和水的反应都是中和反应 B、单质只含有一种元素,所以只含有一种元素的物质一定是单质 C、燃烧都伴随有发光放热现象,所以有发光放热现象的一定是燃烧 D、NaOH、Ca(OH)2等碱溶液都能使酚酞试液变红,所以使酚酞试液变红的一定是碱性溶液26. 某化学兴趣小组为探究铝、铜、银三种金属的活动性顺序,利用实验室中的相关药品设计了如下实验方案(实验用到的三种金属丝均已打磨干净):①稀盐酸、铝、铜、银②硫酸铜溶液、铝、银③硫酸铝溶液、硝酸银溶液、铜④硫酸铝溶液、铜、银⑤硝酸银溶液、铝、铜。其中能验证铝、铜、银金属活动性顺序的是( )A、②③⑤ B、①②③ C、③④⑤ D、①②④27. 取等质量的Na2CO3和NaHCO3固体分别置于两个体积相同的密闭容器中,分别一次性加入等浓度等体积的过量稀硫酸,用压强传感器测得两容器内压强随时间的变化关系如图所示。下列说法正确的是( ) A、曲线a表示Na2CO3与稀硫酸反应过程中压强随时间的变化关系 B、反应过程中两容器内溶液的pH均逐渐减小 C、反应结束后,两容器中H2SO4的质量相等,Na2SO4的质量也相等 D、反应结束后,向两容器中加入过量BaCl2溶液,产生沉淀的质量相等28. 为确定某溶液中含有以下离子H+、Mg2+、Ba2+、Cl-、 、 中的几种,进行了以下实验:
A、曲线a表示Na2CO3与稀硫酸反应过程中压强随时间的变化关系 B、反应过程中两容器内溶液的pH均逐渐减小 C、反应结束后,两容器中H2SO4的质量相等,Na2SO4的质量也相等 D、反应结束后,向两容器中加入过量BaCl2溶液,产生沉淀的质量相等28. 为确定某溶液中含有以下离子H+、Mg2+、Ba2+、Cl-、 、 中的几种,进行了以下实验:①经测定,溶液pH=1;
②取部分未知溶液加入过量NaOH溶液,有白色沉淀产生;
③取②中部分溶液加入Na2CO3溶液,无明显现象。
分析上述实验,下面对溶液中含有离子的判断,正确的是( )
A、一定含有H+、Mg2+、Ba2+、Cl-、 B、一定含有H+、Mg2+、Cl- , 一定不含有 C、一定含有H+、Ba2+ , ,一定不含有Cl- D、一定含有H+、Mg2+ , 可能同时含有Cl-、29. 有一包白色粉末,可能含有Na2CO3、Na2SO4、K2SO4、NaCl、Ba(OH)2中的一种或几种,为了探究其成分,实验过程如图所示:
关于该实验的说法正确的是( )
A、步骤Ⅱ中沉淀部分溶解,则原白色粉末一定有Ba(OH)2、Na2CO3、K2SO4 B、步骤Ⅱ中沉淀部分溶解,则原白色粉末的组成可能有5种情况 C、步骤Ⅱ中沉淀全部溶解,则原白色粉末一定有Ba(OH)2、Na2CO3 , 可能有NaCl D、步骤Ⅱ中沉淀不溶解,则原白色粉末一定有K2SO4 , 一定没有Na2CO330. 有一包白色粉末,可能由NaCl、、、NaOH、中的一种或几种组成,为确定其成分,进行如下实验:①取一定量的白色粉末加入足量水,得到无色溶液。
②向①所得溶液中加入过量Ba(OH)2溶液,产生白色沉淀,过滤,往沉淀中加入足量稀硝酸,沉淀部分溶解。
③往②滤液中先加入几滴无色酚酞溶液,溶液变红,然后加入过量稀盐酸,再滴入几滴硝酸银溶液,产生白色沉淀。
下列关于该白色粉末成分的判断,正确的是( )
A、一定含有、一定没有 , 可能含有NaOH、NaCl B、一定含有、、 , 一定没有 , 可能含有NaCl C、一定含有、、NaCl,一定没有 , 可能含有NaOH D、一定含有、、NaOH、NaCl,一定没有