重庆市潼南区2024年中考化学一模试题
试卷更新日期:2024-05-14 类型:中考模拟
一、单选题(本大题包括16个小题,每小题2分,共32分)每小题只有一个选项符合题意。
-
1. 中华文明源远流长,《天工开物》所述下列过程,主要由化学变化引起的是( )A、棉纱织布 B、烧草成灰 C、伐木制舟 D、海水晒盐2. 下列是生活中常见的几种物质,其中属于溶液的是( )A、汽水 B、冰水 C、酒精 D、牛奶3. “绿色发展”、“低碳生活”等理念逐渐深入人心。下列做法与该理念不相符的是( )A、植树造林增加绿化 B、废旧电池回收处理 C、污水经过处理后排放 D、提倡使用一次性纸杯4. 下列关于氧气的说法正确的是( )A、植物的光合作用会消耗氧气 B、液氧可用作火箭燃料 C、空气中氧气的质量分数为21% D、氧气使食物腐烂是缓慢氧化5. 规范严谨是实验安全和成功的保障。下列实验操作正确的是( )A、连接仪器
 B、铁在氧气中燃烧
B、铁在氧气中燃烧 C、添加酒精
C、添加酒精 D、制取氧气
D、制取氧气 6. 对于下列事实的微观解释错误的是( )A、变瘪的乒乓球放入热水中能鼓起来——分子的体积变大 B、一滴水中约有1.67×1021个水分子——分子的体积非常小 C、切开成熟的菠萝蜜能闻到浓浓的香味——分子在不断地运动 D、6000L氧气加压后可装入40L的钢瓶——分子间的间隔变小7. 下列化学符号中数字“2”表示的意义正确的是( )A、2Ca:2个钙元素 B、2Fe3+:2个亚铁离子 C、CO2:二氧化碳中含有2个氧原子 D、Mg2+:1个镁离子带2个单位正电荷8. 下列对实验现象的描述错误的是( )A、硫在氧气中燃烧产生蓝紫色火焰 B、镁片与稀盐酸剧烈反应并放出热量 C、铁丝在氧气中燃烧生成四氧化三铁 D、铜丝插入硝酸银溶液中溶液变为蓝色9. 人体缺碘会引起甲状腺肿大。下图为碘元素在元素周期表中的相关信息及碘原子的原子结构示意图,下列说法不正确的是( )
6. 对于下列事实的微观解释错误的是( )A、变瘪的乒乓球放入热水中能鼓起来——分子的体积变大 B、一滴水中约有1.67×1021个水分子——分子的体积非常小 C、切开成熟的菠萝蜜能闻到浓浓的香味——分子在不断地运动 D、6000L氧气加压后可装入40L的钢瓶——分子间的间隔变小7. 下列化学符号中数字“2”表示的意义正确的是( )A、2Ca:2个钙元素 B、2Fe3+:2个亚铁离子 C、CO2:二氧化碳中含有2个氧原子 D、Mg2+:1个镁离子带2个单位正电荷8. 下列对实验现象的描述错误的是( )A、硫在氧气中燃烧产生蓝紫色火焰 B、镁片与稀盐酸剧烈反应并放出热量 C、铁丝在氧气中燃烧生成四氧化三铁 D、铜丝插入硝酸银溶液中溶液变为蓝色9. 人体缺碘会引起甲状腺肿大。下图为碘元素在元素周期表中的相关信息及碘原子的原子结构示意图,下列说法不正确的是( )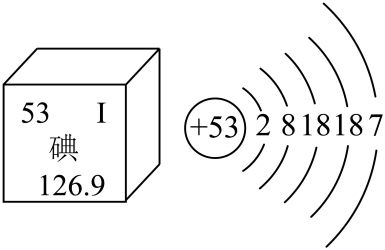 A、碘原子的质子数为53 B、碘的相对原子质量为126.9 C、碘元素和氯元素位于同一周期 D、碘原子在化学反应中容易得到电子10. 春季是感冒的高发季节,对乙酰氨基苯酚(C8H9NO2)是速效感冒胶囊的有效成分之一。下列说法正确的是( )A、是一种氧化物 B、相对分子质量为151g C、氢元素
A、碘原子的质子数为53 B、碘的相对原子质量为126.9 C、碘元素和氯元素位于同一周期 D、碘原子在化学反应中容易得到电子10. 春季是感冒的高发季节,对乙酰氨基苯酚(C8H9NO2)是速效感冒胶囊的有效成分之一。下列说法正确的是( )A、是一种氧化物 B、相对分子质量为151g C、氢元素 质量分数最大
D、含碳、氢、氮、氧四种元素
11. 在2022年夏季的重庆山火扑灭中,“灭火弹”发挥了重要作用。灭火时,将其投入火场,它能迅速释放出超细干粉,覆盖在可燃物表面,使火熄灭。下列对此灭火原理分析正确的是( )
质量分数最大
D、含碳、氢、氮、氧四种元素
11. 在2022年夏季的重庆山火扑灭中,“灭火弹”发挥了重要作用。灭火时,将其投入火场,它能迅速释放出超细干粉,覆盖在可燃物表面,使火熄灭。下列对此灭火原理分析正确的是( ) A、移走可燃物 B、隔绝氧气 C、降低可燃物的着火点 D、降低温度至可燃物着火点以下12. 下列有关二氧化碳的实验描述正确的是( )A、用块状石灰石与稀硫酸制取CO2 B、CO2能使石蕊溶液变为红色 C、用点燃的方法除去CO2中的CO D、用燃着的木条检验CO213. 工业上用黑钨矿冶炼钨的原理中涉及如下反应:。下列有关该反应的说法不正确的是( )A、氢气具有还原性 B、属于置换反应 C、反应后钨元素的化合价降低 D、WO3发生氧化反应14. 如图是一种煤深加工的化学反应微观示意图。下列说法正确的是( )
A、移走可燃物 B、隔绝氧气 C、降低可燃物的着火点 D、降低温度至可燃物着火点以下12. 下列有关二氧化碳的实验描述正确的是( )A、用块状石灰石与稀硫酸制取CO2 B、CO2能使石蕊溶液变为红色 C、用点燃的方法除去CO2中的CO D、用燃着的木条检验CO213. 工业上用黑钨矿冶炼钨的原理中涉及如下反应:。下列有关该反应的说法不正确的是( )A、氢气具有还原性 B、属于置换反应 C、反应后钨元素的化合价降低 D、WO3发生氧化反应14. 如图是一种煤深加工的化学反应微观示意图。下列说法正确的是( ) A、图中只有一种单质 B、生成的丙和丁的分子个数比为2:3 C、反应前后分子、原子都不变 D、物质丁中碳、氢元素的质量比为1:415. 战国所著《周礼》中记载沿海古人“煤饼烧蛎房成灰”(“蛎房”即牡蛎壳),并把这种灰称为“蜃”,“蜃”的主要成分为氧化钙。下列有关说法错误的是( )A、煤是不可再生能源 B、烧蛎房成灰时发生分解反应 C、石灰水中的溶质是氧化钙 D、“蜃”与水混合后温度会升高16. 下列图象能正确反映对应变化关系的是( )
A、图中只有一种单质 B、生成的丙和丁的分子个数比为2:3 C、反应前后分子、原子都不变 D、物质丁中碳、氢元素的质量比为1:415. 战国所著《周礼》中记载沿海古人“煤饼烧蛎房成灰”(“蛎房”即牡蛎壳),并把这种灰称为“蜃”,“蜃”的主要成分为氧化钙。下列有关说法错误的是( )A、煤是不可再生能源 B、烧蛎房成灰时发生分解反应 C、石灰水中的溶质是氧化钙 D、“蜃”与水混合后温度会升高16. 下列图象能正确反映对应变化关系的是( )



A.电解水
B.向接近饱和的溶液中加入硝酸钾
C.向等质量的镁、锌粉中分别加入足量的稀硫酸
D.气体溶解度与温度和压强的关系
A、A B、B C、C D、D二、填空题(本大题包括5个小题,共21分)
-
17. 用化学用语填空。(1)、两个氢分子(2)、2个硝酸根离子。(3)、画出镁原子的结构示意图。(4)、氯化钠溶液中的带电微粒有。18. 随着经济的发展,能源与环境成为人们日益关注的问题。(1)、目前,人类以化石燃料为主要能源,常见的化石燃料有煤、石油、。(2)、在汽油中加入适量乙醇作为汽车燃料,可在一定程度上减少汽车尾气的污染,乙醇在空气中完全燃烧的化学方程式为。(3)、在汽车尾气管上安装净化装置,可使尾气中的CO和NO在催化剂的表面发生反应,生成CO2和—种单质气体,反应的化学方程式为。(4)、火箭发动机常以煤油作燃料,若15.6kg煤油完全燃烧生成了48.4kg CO2和21.6kg H2O。煤油中一定含有的元素是(填元素符号)。(5)、开发利用新能源是未来能源发展的必然趋势,不少家庭已经开始使用太阳能热水器,除太阳能外,下列能源也属于新能源的是____。A、焦炭 B、柴油 C、风能 D、核能19. 生活中常用的清洗剂有洗涤剂、洁厕灵、炉具清洁剂等,请回答:
清洗剂类别
洗洁精
洁厕灵
84消毒液
污渍爆炸盐
主要成分
表面活性剂
盐酸
次氯酸钠(NaClO)
过碳酸钠
(1)、使用洗洁精清洗餐具上的油污,是因为它具有功能。(2)、污渍爆炸盐溶于水后生成Na2CO3和H2O2 , 将爆炸盐溶于水后,再加入少量二氧化锰,会产生大量气泡,写出产生该气体的化学方程式。(3)、洁厕灵与“84消毒液”两种清洁剂不能混用,混用会发生如下反应: , 推测X的化学式为。20. 仰望星空走向深蓝,我国航天航海技术不断迈向新征程。由所学知识填空:(1)、长征五号运载火箭使用液氢和液氧作推进剂。①火箭中的燃料燃烧时的化学方程式为:。
②液氢作为火箭发射的燃料,其主要优点为(填序号)。
A.制取成本低
B.贮存方便
C.燃烧产物无污染
(2)、我国首艘国产航空母舰“山东舰”已交接入列。①制造航母使用大量的钢铁,工业上用赤铁矿冶炼铁的化学方程式为。
②航母外壳用涂料覆盖,是为了防止钢铁材料与接触而锈蚀。
③航母使用了高锰钢(含有锰元素),已知锰(Mn)的活动性位于镁和锌之间。为了探究Mn、Fe、Cu三种金属的活动性顺序,下列不能达到实验目的的是(填序号)。
A.铁丝、铜丝、MnSO4
B.铁丝、MnSO4溶液、CuSO4溶液
C.锰丝、铜丝、FeSO4溶液
D.锰丝、铁丝、铜丝、稀硫酸
21. 如图是a、b、c三种物质的溶解度曲线,据图回答下列问题。 (1)、P点的含义。(2)、t1℃时,把20ga放入50g水中,充分搅拌,所得溶液的质量是g。(3)、欲使a物质的溶液从M点转化为N点,可采取的措施是。(4)、t3℃时a、b、c三种物质的饱和溶液各100g,分别降温到℃时,所得溶液中溶剂的质量由大到小依次为。
(1)、P点的含义。(2)、t1℃时,把20ga放入50g水中,充分搅拌,所得溶液的质量是g。(3)、欲使a物质的溶液从M点转化为N点,可采取的措施是。(4)、t3℃时a、b、c三种物质的饱和溶液各100g,分别降温到℃时,所得溶液中溶剂的质量由大到小依次为。三、实验题(本大题包括2个小题,共11分)
-
22. 设计对比实验是化学研究常用的方法。
 (1)、实验Ⅰ能形成溶液的是(填“①”或“②”)试管。(2)、实验Ⅱ中镁与盐酸反应的化学方程式为 , 通过对比(填“能”或“不能”)比较镁和铝的活动性。(3)、实验Ⅲ通过对比可探究铁生锈的条件,试管a、b中蒸馏水需要煮沸并冷却的原因是;试管c棉花中包裹氯化钙的作用是。23. 农业生产上常用质量分数为16%的氯化钠溶液选种。在化学实验课上,两位同学用如下两种不同的方法,配制100g溶质质量分数为16%的氯化钠溶液。
(1)、实验Ⅰ能形成溶液的是(填“①”或“②”)试管。(2)、实验Ⅱ中镁与盐酸反应的化学方程式为 , 通过对比(填“能”或“不能”)比较镁和铝的活动性。(3)、实验Ⅲ通过对比可探究铁生锈的条件,试管a、b中蒸馏水需要煮沸并冷却的原因是;试管c棉花中包裹氯化钙的作用是。23. 农业生产上常用质量分数为16%的氯化钠溶液选种。在化学实验课上,两位同学用如下两种不同的方法,配制100g溶质质量分数为16%的氯化钠溶液。方法一:用固体氯化钠和水配制100g16%的氯化钠溶液。
方法二:用溶质质量分数为20%的氯化钠溶液(密度为1.148)加水稀释得到100g16%的氯化钠溶液。根据下图回答问题。
 (1)、方法一中量取水时应选择(填“10”“50”或“100”)mL量筒。溶解时玻璃棒的作用是。下列错误操作可能导致溶质质量分数小于16%的是。(填序号)
(1)、方法一中量取水时应选择(填“10”“50”或“100”)mL量筒。溶解时玻璃棒的作用是。下列错误操作可能导致溶质质量分数小于16%的是。(填序号)①所称取的氯化钠固体不纯
②量取水时仰视读数
③向烧杯中倒水溶解时部分水洒出
④装瓶时部分溶液洒出
(2)、方法二中一般不会用到上述仪器中的(填仪器序号),量取20%的氯化钠溶液时,若俯视读数,则稀释后所得溶液的溶质质量分数会(填“偏小”、“偏大”或“无影响”)。(3)、将配制好的氯化钠溶液装入容器中,密封好并贴上标签。请填写如图标签的有关内容。
四、计算题(本大题包括1个小题,共6分)
-
24. 黄铜(铜、锌合金)常被用于制造阀门、水管、空调内外机连接管和散热器等,为测定某黄铜样品中铜的质量分数,某同学取10.6克黄铜样品放入盛有196克稀硫酸的烧杯中,恰好完全反应,测得烧杯中剩余物质的总质量为206.4克。试计算:(1)、生成氢气的质量。(2)、该黄铜样品中铜的质量。(3)、反应后溶液中溶质的质量分数(计算结果保留0.1%)。