河南省洛阳市汝阳县2024年中考化学第一次模拟考试试题
试卷更新日期:2024-05-14 类型:中考模拟
一、选择题(14分)
-
1. 某研究小组利用月季花完成“自制酸碱指示剂”的学习项目,下列过程中主要发生化学变化的是( )A、捣烂叶片 B、酒精浸泡 C、纱布过滤 D、酸碱检验2. 下列图标表示我国“国家节水标志”的是( )A、
 B、
B、 C、
C、 D、
D、 3. 下列基本实验操作正确的是( )A、
3. 下列基本实验操作正确的是( )A、 取用固体药品
B、
取用固体药品
B、 闻气体的气味
C、
闻气体的气味
C、 蒸发食盐水
D、
蒸发食盐水
D、 熄灭酒精灯
4. KMnO4是实验室制取氧气的重要物质,其中锰元素的化合价为( )A、+3 B、+5 C、-4 D、+75. 大蒜素(C6H10S2O)有较强的抗菌作用,易挥发。新鲜大蒜头中的蒜氨酸(C6H11NSO3)受撞击后,转化为大蒜素。下列有关大蒜素和蒜氨酸的说法正确的是( )A、两者组成元素种类相同 B、大蒜素中碳、氢元素质量比为3:5 C、挥发性是大蒜素的化学性质 D、17.7g蒜氨酸中含有硫元素质量为3.2g6. 下列说法正确的是( )A、碳-12原子和碳-13原子的中子数相同 B、KMnO4和K2MnO4中有相同的原子团 C、Fe2+和Fe3+都属于铁元素,核外电子数不同 D、
熄灭酒精灯
4. KMnO4是实验室制取氧气的重要物质,其中锰元素的化合价为( )A、+3 B、+5 C、-4 D、+75. 大蒜素(C6H10S2O)有较强的抗菌作用,易挥发。新鲜大蒜头中的蒜氨酸(C6H11NSO3)受撞击后,转化为大蒜素。下列有关大蒜素和蒜氨酸的说法正确的是( )A、两者组成元素种类相同 B、大蒜素中碳、氢元素质量比为3:5 C、挥发性是大蒜素的化学性质 D、17.7g蒜氨酸中含有硫元素质量为3.2g6. 下列说法正确的是( )A、碳-12原子和碳-13原子的中子数相同 B、KMnO4和K2MnO4中有相同的原子团 C、Fe2+和Fe3+都属于铁元素,核外电子数不同 D、 和
和  化学性质相同
7. 下列反应中,不属于置换反应的是( )A、CO+CuOCu+CO2 B、 C、2Mg+CO2 C+2MgO D、8. X, Y, Z, W四种元素的质子数如图所示。下列说法正确的是( )
化学性质相同
7. 下列反应中,不属于置换反应的是( )A、CO+CuOCu+CO2 B、 C、2Mg+CO2 C+2MgO D、8. X, Y, Z, W四种元素的质子数如图所示。下列说法正确的是( ) A、Z是地壳中含量最多的元素 B、W原子的最外层电子数是第1层的2倍 C、X、Z均能与Y形成两种不同的化合物 D、Y与W原子化学性质都不稳定,都容易得电子形成稳定结构9. 一定条件下,甲、乙、丙、丁四种物质在密闭容器中发生反应,测得反应前后各物质的质量如下表所示。下列说法正确的是( )
A、Z是地壳中含量最多的元素 B、W原子的最外层电子数是第1层的2倍 C、X、Z均能与Y形成两种不同的化合物 D、Y与W原子化学性质都不稳定,都容易得电子形成稳定结构9. 一定条件下,甲、乙、丙、丁四种物质在密闭容器中发生反应,测得反应前后各物质的质量如下表所示。下列说法正确的是( )物质
甲
乙
丙
丁
反应前质量/g
26
8
2
4
反应后质量/g
1
M
16
15
A、丁一定是化合物 B、反应中的甲和丁的质量变化比为 C、乙可能是该反应的催化剂 D、该反应属于化合反应10. 20℃时,食盐的溶解度是36g,将40g食盐放入100g水中,所得溶液的质量为( )A、40g B、140g C、136g D、100g11. 将盐酸溶液加水稀释后,下列关于该溶液的变化情况描述正确的是( )A、溶液的酸性增强 B、溶液中溶质的质量分数增大 C、溶液的pH增大 D、溶质质量增大12. 下列有关化学用语的表述正确的是( )A、表示3个氮元素 B、碳酸根离子: C、的名称:氯化镁 D、氧化铝的化学式:13. 下列反应中属于中和反应的是( )A、CO2+2NaOH=Na2CO3 B、H2SO4+CuO=CuSO4+H2O C、H2SO4+Mg(OH)2=MgSO4+H2O D、2HCl+CaCO3=CaCl2+H2O+CO2↑14. 某金属混合物由Mg、Al、Zn、Fe四种金属中的两种组成。4g该金属混合物与足量的盐酸充分反应,得到0.2g氢气,则该金属混合物的组成不可能是( )A、Mg和Al B、Fe和Al C、Fe和Mg D、Mg和Zn二、填空题(16分)
-
15. 在空气中含量最高且化学性质不活泼的气体是;地壳中含量最高的金属元素是;保持物质化学性质的最小微粒是。16. 盐酸中的溶质是 , 溶剂是 , 向盐酸溶液中滴加石蕊试液,溶液变色。17. 预防新冠肺炎,做好消毒至关重要。体积分数为75%的酒精是常用的消毒剂,在配制时发现75mL的酒精和25mL的水混合后体积小于100mL,原因是 , 喷洒后,室内充满刺激性气味,请从微观角度分析其原因。18. 固体氢氧化钠暴露在空气中容易吸收水分,表面潮湿并逐渐溶解,这种现象叫做 , 因此,氢氧化钠可用作某些气体的;同时氢氧化钠还会吸收空气中的二氧化碳而变质,原因是(用化学方程式表示)。19. 发明了联合制碱法并为我国制碱工业作出杰出贡献的科学家是 , 制的“碱”的化学式为。20. 如图所示是初中化学常见物之间的转化关系(部分物质和反应条件已经略去)。已知A、B、C中均含有同一种元素,A是纯碱,C是难溶性盐且其相对分子质量为100。C的化学式为 , B的一种用途是 , A→C的化学方程式为。

三、简答题(共10分)
-
21. 如图为模拟炼铁的微型装置。请回答:
 (1)、写出A处发生反应的化学方程式。(2)、描述B处的现象。(3)、C处还需放置一个气囊,作用是?22. 金属活动性顺序在工农业生产和科学研究中有重要应用.(1)、铝比较活泼,为什么铝制品却有很好的抗腐蚀性能?(2)、农业上不能用铁制容器配制农药波尔多液(含硫酸铜),请用化学方程式解释.23. 向一定量久置的氢氧化钠溶液中,逐滴滴加稀盐酸,部分反应物与生成物之间的质量关系如图所示,请根据图示回答:
(1)、写出A处发生反应的化学方程式。(2)、描述B处的现象。(3)、C处还需放置一个气囊,作用是?22. 金属活动性顺序在工农业生产和科学研究中有重要应用.(1)、铝比较活泼,为什么铝制品却有很好的抗腐蚀性能?(2)、农业上不能用铁制容器配制农药波尔多液(含硫酸铜),请用化学方程式解释.23. 向一定量久置的氢氧化钠溶液中,逐滴滴加稀盐酸,部分反应物与生成物之间的质量关系如图所示,请根据图示回答: (1)、氢氧化钠溶液是否变质:;说明理由:。(2)、写出a点对应的溶液中溶质的成分:。24. 学了酸的化学性质,某同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。
(1)、氢氧化钠溶液是否变质:;说明理由:。(2)、写出a点对应的溶液中溶质的成分:。24. 学了酸的化学性质,某同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。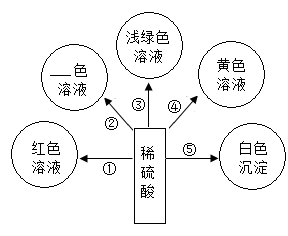 (1)、若用Cu(OH)2实现②,会得到色溶液。(2)、若想实现③,得到浅绿色溶液,可选用的单质是。(3)、若选用BaCl2溶液实现⑤,此反应的化学方程式为。
(1)、若用Cu(OH)2实现②,会得到色溶液。(2)、若想实现③,得到浅绿色溶液,可选用的单质是。(3)、若选用BaCl2溶液实现⑤,此反应的化学方程式为。四、综合应用题(10分)
-
25. 酸、碱、盐在生产和生活中有广泛的应用。(1)、焙制糕点所用发酵粉中含有碳酸氢钠,其俗名为(填字母代号)。
a.纯碱 b.烧碱 c.苏打 d.小苏打
(2)、如图是氢氧化钠溶液与硫酸反应时溶液pH变化的示意图。
①根据图示判断,该实验是将(填“氢氧化钠溶液”或“硫酸”)滴加到另一种溶液中。
②滴入溶液体积为V2mL时,溶液中的溶质为。
(3)、测定pH最简单的方法是使用。我们将pH值的降雨称为酸雨。(4)、服用含有氢氧化铝[Al(OH)3]的药物可以治疗胃酸过多症,反应的方程式为。稀释浓硫酸的方法。(5)、为测定某石灰石样品中碳酸钙的质量分数,称取10g石灰石(杂质不参加反应)放入烧杯中,加入100g稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为106.7g(气体的溶解忽略不计)。请计算该样品中碳酸钙的质量分数。